
科目: 來源: 題型:
【題目】五種短周期元素X、Y、Z、M、W的原子序數與其常見化合價的關系如圖所示,下列關系不正確的是( )
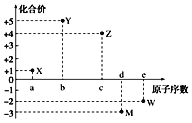
A.元素X可能為鋰
B.原子半徑大小:r(M)>r(W)
C.X2W中各原子均達到8電子穩定結構
D.元素氣態氫化物的穩定性:Y>M
查看答案和解析>>
科目: 來源: 題型:
【題目】氯水中含有多種成分,因而具有多種性質,根據新制氯水分別與如圖四種物質發生的反應填空(a、b、c、d、e中重合部分代表物質間反應,且氯水足量)。
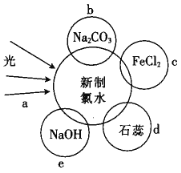
(1)氯水中含有的粒子有![]() 、
、![]() 、______、
、______、![]() 、
、![]() 、______、
、______、![]() 七種。
七種。
(2)久置的氯水變為_____________,原因是___________________________(用化學反應方程式表示)。
(3)b過程中的離子方程式是_______________________。
(4)e過程中所發生的主要反應的化學方程式為____________________________。
(5)能證明氯水具有漂白性的是______________________(填“a”“b”“c”或“d”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】碳熱還原氯化法從鋁土礦中煉鋁具有步驟簡單、原料利用率高等優點,其原理如下:
Ⅰ.Al2O3(s) + AlCl3(g) + 3C(s) ![]() 3AlCl(g) + 3CO(g) – 1486 kJ
3AlCl(g) + 3CO(g) – 1486 kJ
Ⅱ.3AlCl(g) ![]() 2Al(l) + AlCl3(g) + 140 kJ
2Al(l) + AlCl3(g) + 140 kJ
(1)寫出反應Ⅰ的化學平衡常數表達式K=_____________,升高溫度,K_______(填增大、減小、不變)。
(2)寫出反應Ⅱ達到平衡狀態的一個標志_________________________________;結合反應Ⅰ、Ⅱ進行分析,AlCl3在煉鋁過程中的作用可以看作___________。
(3)將1mol氧化鋁與3mol焦炭的混合物加入2L反應容器中,加入2mol AlCl3氣體,在高溫下發生反應Ⅰ。若5min后氣體總質量增加了27.6g,則AlCl的化學反應速率為_________ mol/(L·min)。
(4)Na2O2具有很強的氧化性。少量Na2O2與FeCl2溶液能發生反應:____Na2O2+ FeCl2+___H2O→____Fe(OH)3↓+_____FeCl3+____NaCl;已知FeCl2前面系數為6,配平上述化學方程式,并標出電子轉移方向和數目________________。此反應中被還原的元素是____________,氧化產物是__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】海水中含有豐富的資源,其中包括鈉離子、氯離子、鎂離子等。
(1)氯元素位于元素周期表第________列,寫出氯原子的最外層電子排布式________________, 最外層電子所占據的軌道數為________ 個,氯原子核外共有________種能量不同的電子。
(2)列舉能說明Mg的金屬性比Na弱的一個實驗事實__________________。
(3)相同壓強下,部分元素氟化物的熔點見下表:
氟化物 | NaF | MgF2 | SiF4 |
熔點/℃ | 1266 | 1534 | 183 |
試解釋上表中熔點SiF4遠低于NaF的原因_________________________
(4)氨水是實驗室最常用的弱堿,向滴有少量酚酞試液的稀氨水,加入少量的NH4AC晶體,若觀察到________________則可證明一水合氨是弱電解質。請再提出一個能證明一水合氨是弱電解質的實驗方案 ______________________________________
(5)向鹽酸中滴加氨水至過量,該過程所發生反應的離子方程式為___________________
在滴加的整個過程中離子濃度大小關系可能正確的是(______)
a.c(C1-)=c(NH4+)>c(H+)=c(OH-) b.c(C1-)>c(NH4+)= c(OH-) >c(H+)
c.c(NH4+)>c(OH-)>c(C1-)>c(H+) d.c(OH-)>c(NH4+)>c(H+)>c(C1-)
查看答案和解析>>
科目: 來源: 題型:
【題目】掌握化學的基本概念和研究方法才能學好化學。按要求回答下列問題:
(1)下列是對堿、酸、鹽、氧化物的分類列表:
堿 | 酸 | 鹽 | 氧化物 | |
第一組 |
|
|
|
|
第二組 |
|
|
|
|
第三組 |
|
|
|
|
表中每組均有物質分類錯誤,三組中對應分類錯誤的物質分別是_________、_________、_________。(填化學式)
(2)![]() 固體不能導電,而
固體不能導電,而![]() 溶液可以導電,原因是_________________________。
溶液可以導電,原因是_________________________。
(3)依據下列兩個反應,按要求填空。
Ⅰ.![]()
Ⅱ.![]()
反應Ⅰ和反應Ⅱ中,![]() 只作氧化劑的反應是________(填“Ⅰ”或“Ⅱ”);反應Ⅱ中,每生成標準狀況下
只作氧化劑的反應是________(填“Ⅰ”或“Ⅱ”);反應Ⅱ中,每生成標準狀況下![]() ,反應中轉移________
,反應中轉移________![]() 電子;
電子;![]() 和
和![]() 都能使澄清石灰水變渾濁,請設計一種方法檢驗
都能使澄清石灰水變渾濁,請設計一種方法檢驗![]() 、
、![]() 混合氣體中的
混合氣體中的![]() :_____________。
:_____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】化合物H是一種藥物合成中間體,其合成路線如下:
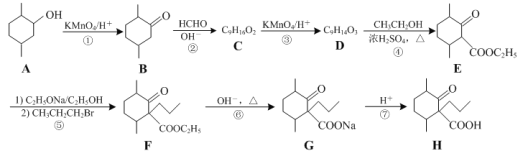
(1)A→B的反應的類型是____反應。
(2)化合物H中所含官能團的名稱是______。
(3)化合物C的結構簡式為____。B→C反應時會生成一種與C互為同分異構體的副產物,該副產物的結構簡式為____。
(4)D的一種同分異構體同時滿足下列條件,寫出該同分異構體的結構簡式:____。
①能發生水解反應,所得兩種水解產物均含有3種化學環境不同的氫;
②分子中含有六元環,能使溴的四氯化碳溶液褪色。
(5)已知:![]()
![]() CH2ClCH2OH。寫出以環氧乙烷(
CH2ClCH2OH。寫出以環氧乙烷(![]() )、
)、![]() 、乙醇和乙醇鈉為原料制備
、乙醇和乙醇鈉為原料制備 的合成路線流程圖____。(無機試劑任用,合成路線流程圖示例見本題題干)
的合成路線流程圖____。(無機試劑任用,合成路線流程圖示例見本題題干)
查看答案和解析>>
科目: 來源: 題型:
【題目】在恒溫條件下將一定量X和Y的混合氣體通入一容積為2L的密閉容器中,X和Y兩物質的濃度隨時間變化情況如圖。

(1)該反應的化學方程式為(反應物或生成物用符號X、Y表示):_________________________。
(2)a、b、c、d四個點中,表示化學反應處于平衡狀態的點是________________。
素材1:某溫度和壓強下,2L容器中,發生反應2SO2+O2![]() 2SO3,不同時間點測得密閉體系中三種物質的物質的量如下:
2SO3,不同時間點測得密閉體系中三種物質的物質的量如下:

素材2:反應在不同條件下進行時SO2的轉化率:(SO2的轉化率是反應的SO2占起始SO2的百分數,SO2的轉化率越大,化學反應的限度越大)

根據以上的兩個素材回答問題:
(3)根據素材1中計算20~30s期間,用二氧化硫表示的化學反應平均速率為________。
(4)根據素材2中分析得到,提高該化學反應限度的途徑有_______________。
(5)根據素材1、素材2中分析得到,要實現素材1中SO2的轉化率需控制的反應具體條件是__________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】我國每年產生的廢舊鉛蓄電池約330萬噸。從含鉛廢料(含PbSO4、PbO2、PbO等)中回收鉛,實現鉛的再生,意義重大。一種回收鉛的工藝流程如下:
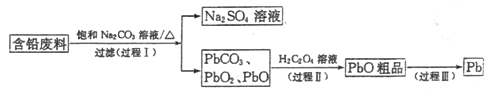
(1)鉛蓄電池放電時,PbO2作____極。
(2)過程I,已知:PbSO4、PbCO3的溶解度(20℃)見圖l;Na2SO4、Na2CO3的溶解度見如圖。
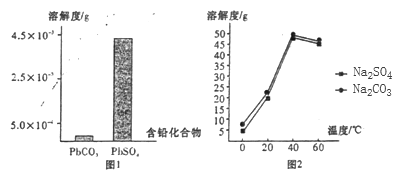
①根據圖l寫出過程I的離子方程式:__________。
②生產過程中的溫度應保持在40℃,若溫度降低,PbSO4的轉化速率下降。根據如圖,解釋可能原因:
i.溫度降低,反應速率降低; ii.______________(請你提出一種合理解釋)。
(3)①過程Ⅱ,發生反應2PbO2+H2C2O4=2PbO+H2O2+2CO2↑。實驗中檢測到有大量O2放出,推測PbO2氧化了H2O2,通過實驗證實了這一推測。實驗方案是___________。
(已知:PbO2為棕黑色固體;PbO為橙黃色固體)
②寫出H2O2的電子式__________。
(4)過程Ⅲ,將PbO粗品溶解在HCl和NaCl的混合溶液中,得到含Na2PbCl4的電解液,電解Na2PbCl4溶液,生成Pb,如圖。
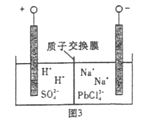
①陰極的電極反應式是____________。
②電解一段時間后,PbCl42-濃度極大下降,為了恢復其濃度且實現物質的循環利用,陰極區采取的方法是_______。
(5)如果用鉛蓄電池作電源電解飽和食鹽水制取Cl2,已知某鉛蓄電池中硫酸溶液的體積為0.8L,電解其按硫酸濃度為4.5mol/L,當制得26.88L Cl2時(指在標準狀況下),求理論上電解后電池中硫酸溶液的濃度為________ mol·L-1。(假設電解前后硫酸溶液的體積不變)
查看答案和解析>>
科目: 來源: 題型:
【題目】某工業廢玻璃粉末含SiO2、Fe2O3、CeO2、FeO等。某課題小組設計如下工藝流程對資源進行回收,得到Ce(OH)4和硫酸鐵銨礬。
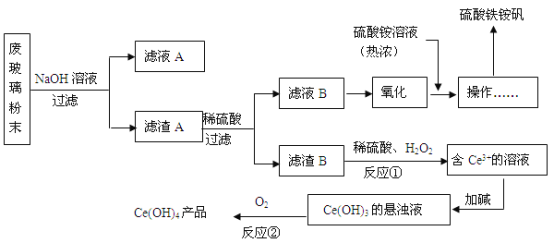
已知:CeO2不溶于稀硫酸;酸性條件下,Ce3+易水解,Ce4+有較強氧化性。
(1)硫酸鐵銨礬可凈水,其原理是(寫離子方程式)________________________________。
(2)濾液A的主要成分_______________(填寫化學式)。
(3)反應①的離子方程式是_____________________________。
(4)反應②的化學反應方程式是__________________________。
(5)已知制硫酸鐵銨礬晶體[Fe2(SO4) 3·(NH4) 2SO4·24H2O,式量964]的產率為80%,若加入13.2g (NH4) 2SO4(式量132),可制得晶體的質量是_________。
(6)化合物HT可作為萃取劑能將鈰離子從水溶液中萃取出來,過程表示為:
Ce2(SO4)3(水層)+ 6HT(有機層)![]() 2CeT3 (有機層)+3H2SO4(水層)
2CeT3 (有機層)+3H2SO4(水層)
分液得到CeT3(有機層),再加入H2SO4 獲得較純的含Ce3+的水溶液。可選擇硫酸作反萃取劑的原因是___(從平衡移動角度回答)。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列指定反應的離子方程式正確的是
A.石灰水中加入過量小蘇打溶液:![]()
B.將銅絲插入足量濃硝酸中:![]()
C.將SO2通入少量氨水中:![]()
D.用雙氧水從酸化的海帶灰浸出液中提取碘:![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com