
科目: 來源: 題型:
【題目】脫水環化是合成生物堿類天然產物的重要步驟,某生物堿V合成路線如圖:

(1)Ⅳ中官能團的名稱___;反應①的反應類型為___。
(2)反應②的化學方程式__。
(3)Ⅰ和Ⅲ在濃硫酸催化加熱時反應的化學方程式___。
(4)下列說法正確的是___。
A.Ⅰ和Ⅴ均屬于芳香烴 B.Ⅱ能發生銀鏡反應
C.Ⅱ能與4molH2發生加成反應 D.反應③屬于酯化反應
(5)A的結構簡式__。
(6)Ⅵ與Ⅰ互為同分異構體,Ⅵ遇FeCl3發生顯色反應,其苯環上的一氯代物只有2種。寫出滿足上述條件的Ⅵ的結構簡式___。
(7)一定條件下,化合物Ⅶ(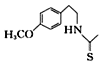 )也能發生類似反應④的環化反應,Ⅶ的環化產物的結構簡式___。
)也能發生類似反應④的環化反應,Ⅶ的環化產物的結構簡式___。
查看答案和解析>>
科目: 來源: 題型:
【題目】氨的催化氧化是工業制硝酸的重要反應:4NH3+5O2![]() 4NO+6H2O,對于該反應判斷正確的是
4NO+6H2O,對于該反應判斷正確的是
A. 氧氣被還原B. 該反應是置換反應
C. 氨氣是氧化劑D. 若有17 g氨參加反應,反應中轉移10 mol電子
查看答案和解析>>
科目: 來源: 題型:
【題目】煤燃燒排放的煙氣中含有SO2,易形成酸雨、污染大氣。有效去除和利用SO2是環境保護的重要議題。
(1)雙堿法洗除SO2。NaOH溶液![]() Na2SO3溶液
Na2SO3溶液
①上述過程生成Na2SO3的離子方程式為_________。
②雙堿法洗除SO2的優點為_________。
(2)NaClO2氧化法吸收SO2。向NaClO2溶液中通入含有SO2的煙氣,反應溫度為323 K,反應一段時間。
①隨著吸收反應的進行,吸收劑溶液的pH逐漸_________(填“增大”“不變”或“減小”)。
②如果采用NaClO替代NaClO2,也能得到較好的煙氣脫硫效果。吸收等量的SO2,所需NaClO的物質的量是NaClO2的_________倍。
(3)SO2的利用。生產焦亞硫酸鈉(Na2S2O5),通常是由NaHSO3過飽和溶液經結晶脫水制得。利用煙道氣中的SO2生產Na2S2O5的工藝如下:
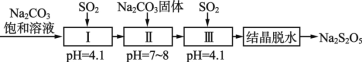
①Ⅰ中反應的化學方程式為___________。
②若Ⅲ中通入SO2不足,結晶脫水得到的Na2S2O5中混有的主要雜質是_______(填化學式)。
③工藝中加入Na2CO3固體,并再次充入SO2的目的是_________。
查看答案和解析>>
科目: 來源: 題型:
【題目】甲胺(CH3NH2)是合成太陽能敏化劑的原料。一定溫度下,在三個體積均為2.0 L的恒容密閉容器中按不同方式投入反應物,發生反應CH3OH(g)+NH3(g) CH3NH2(g)+H2O(g),測得有關實驗數據如下:
容器編號 | 溫度/K | 起始物質的量(mol) | 平衡物質的量mol | ||||
CH3OH | NH3 | CH3NH2 | H2O | CH3NH2 | H2O | ||
I | 530 | 0.40 | 0.40 | 0 | 0 | 0.30 | |
II | 530 | 0.80 | 0.80 | 0 | 0 | ||
III | 500 | 0 | 0 | 0.20 | 0.20 | 0.16 | |
下列說法正確的是( )
A. 正反應的平衡常數K(Ⅰ)=K(Ⅱ)<K(Ⅲ)
B. 達到平衡時,體系中c(CH3OH)關系:2c(CH3OH,Ⅰ)>c(CH3OH,Ⅱ)
D. 530K時,若起始向容器Ⅰ中充入CH3OH 0.10 mol、NH3 0.15 mol、CH3NH2 0.10 mol、H2O 0.10 mol,則反應將向逆反應方向進行
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,向20 mL 0.2 mol·L-1 H2A溶液中滴加0.2 mol·L-1 NaOH溶液,有關微粒的物質的量變化如圖,根據圖示判斷,下列說法錯誤的是( )
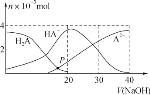
A.在P點時,c(H2A)+c(HA-)+c(A2-)+c(OH-)=c(Na+)+c(H+)
B.當V(NaOH)=20 mL時,c(OH-)=c(H+)+c(HA-)+2c(H2A)
C.當V(NaOH)=30 mL時,2c(Na+)=3[c(HA-)+c(A2-)+c(H2A)]
D.當V(NaOH)=40 mL時,c(Na+)>c(A2-)>c(HA-)>c(H2A)>c(OH-)>c(H+)
查看答案和解析>>
科目: 來源: 題型:
【題目】28g CO氣體在1mol的氧氣中燃燒后,所得的氣體通過足量Na2O2固體中充分反應后,下列說法不正確的是( )
A. CO與氧氣反應,只消耗了0.5mol氧氣
B. 充分反應后Na2O2固體質量增加了28 g
C. 通過以上兩步反應后余下氧氣物質的量為0.5mol
D. 若2gH2替代 28g的CO發生上述反應,則Na2O2固體質量增加了2g
查看答案和解析>>
科目: 來源: 題型:
【題目】分子式為![]() 的有機物A有下列變化:
的有機物A有下列變化:

其中B、C的相對分子質量相等,下列有關說法錯誤的是( )
A.C和E互為同系物
B.符合題目條件的A共有4種
C.D既能發生氧化反應,又能發生還原反應
D.符合題目條件的B共有4種
查看答案和解析>>
科目: 來源: 題型:
【題目】NA為阿伏加德羅常數的值,下列說法正確的是( )
A.lmolC3H8O分子中含有共價鍵數目為11NA
B.一定條件下,將2.8gN2與足量氫氣充分反應,得到氨氣分子數目等于0.2NA
C.標準狀況下,22.4LSO2和SO3的混合物,含硫原子的數目為NA
D.15g14C16O中含有的質子數目為8NA
查看答案和解析>>
科目: 來源: 題型:
【題目】某小組以CoCl2·6H2O、NH4Cl、H2O2、濃氨水為原料,在活性炭催化下,合成了橙黃色晶體X。為測定其組成,進行如下實驗。
①氨的測定:精確稱取wgX,加適量水溶解,注入如圖所示的三頸瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸氣,將樣品液中的氨全部蒸出,用V1mLc1mol·L-1的鹽酸標準溶液吸收。蒸氨結束后取下接收瓶,用c2mol·L-1NaOH標準溶液滴定過剩的HCl,到終點時消耗V2mLNaOH溶液。
②氯的測定:準確稱取樣品X,配成溶液后用AgNO3標準溶液滴定,K2CrO4溶液為指示劑,至出現淡紅色沉淀不再消失為終點(Ag2CrO4為磚紅色)。回答下列問題:
(1)裝置中安全管的作用原理是___。
(2)用NaOH標準溶液滴定過剩的HCl時,應使用___式滴定管,可使用的指示劑為___。
(3)樣品中氨的質量分數表達式為___。

(4)測定氨前應該對裝置進行氣密性檢驗,若氣密性不好測定結果將___(填“偏高”或“偏低”)。
(5)滴定終點時,若溶液中c(Ag+)=2.0×10-5mol·L-1,c(CrO42-)為___mol·L-1。
(已知:Ksp(Ag2CrO4)=1.12×10-12)
(6)X的化學為[Co(NH3)6]Cl3。制備X的反應化學方程式為___。
查看答案和解析>>
科目: 來源: 題型:
【題目】碘及其化合物在合成殺菌劑、藥物等方面具有廣泛用途。回答下列問題:
(1)大量的碘富集在海藻中,用水浸取后濃縮,再向濃縮液中加MnO2和H2SO4,即可得到I2,該反應的還原產物為___。
(2)上述濃縮液中含有I-、Cl-等離子,取一定量的濃縮液,向其中滴加AgNO3溶液,當AgCl開始沉淀時,溶液中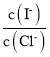 為:___,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
為:___,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)Bodensteins研究了下列反應:2HI(g)H2(g)+I2(g) ΔH=+11kJ·mol-1,
在716K時,氣體混合物中碘化氫的物質的量分數x(HI)與反應時間t的關系如下表:
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根據上述實驗結果,該反應的平衡常數K的計算式為___。若起始時n(HI)=100mol,則過程中需吸收的能量為___kJ。
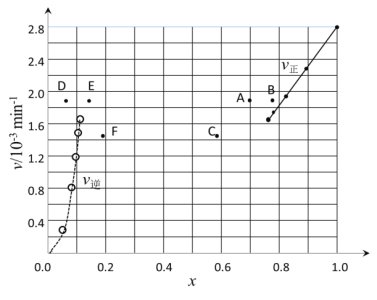
②上述反應中,正反應速率為v正=k正·x2(HI),逆反應速率為v逆=k逆·x(H2)·x(I2),其中k正、k逆為速率常數,則k逆為___(以K和k正表示)。
③由上述實驗數據計算得到v正~x(HI)和v逆~x(H2)的關系可用如圖表示。當升高到某一溫度時,反應重新達到平衡,相應的點分別為___(填字母)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com