
科目: 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是
A.反應5NH4NO3=2HNO3+4N2↑+9H2O,生成22.4LN2時轉移的電子數為3.75NA
B.1 mol濃硫酸與足量Mg完全反應,轉移電子數可能為NA
C.標準狀況下甲烷(CH4)和氧氣(氧氣充足)的混合氣體共22.4L,完全燃燒后產物的分子總數一定為NA
D.10g的D2O中含有的質子數與中子數分別為5NA和4NA
查看答案和解析>>
科目: 來源: 題型:
【題目】下述溶液一定呈酸性的是
A.pH=6.8的溶液
B.滴入酚酞呈無色的溶液
C.室溫時,溶液中的c(H+)=1×10-2 mol·L-1
D.溶液中水電離出的c(H+)=1×10-10 mol·L-1
查看答案和解析>>
科目: 來源: 題型:
【題目】下列離子反應方程式書寫正確的是
A.往稀鹽酸中逐滴加入Na2CO3溶液,開始時:H++CO![]() =HCO
=HCO![]()
B.草酸(H2C2O4,弱酸)溶液中加入酸性KMnO4溶液: 2MnO![]() +5C2O
+5C2O![]() +16H+=2Mn2++10CO2↑+8H2O
+16H+=2Mn2++10CO2↑+8H2O
C.往少量澄清石灰水中加入Ca(HCO3)2溶液: Ca2++OH-+HCO![]() =CaCO3↓+H2O
=CaCO3↓+H2O
D.用HI溶液溶解Fe2O3固體:Fe2O3+6H+=2Fe3++3H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室制備Cl2通常采用如圖所示裝置:

(1)A裝置中發生反應的化學方程式是________;每生成0.5 mol Cl2,被氧化的物質的物質的量是_____mol。
(2)儀器a的名稱是_________;
(3)B裝置中所盛的試劑是________________;
(4)實驗時,通常采用密度為1.19 g/cm3、濃度為36.5%的濃鹽酸。該濃鹽酸的物質的量濃度為________;
(5)將如圖裝置代替裝置D和E,可進行“氯氣與金屬鈉反應”的實驗,以下敘述正確的是________。
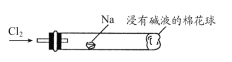
A. 反應生成的大量白煙是氯化鈉晶體
B. 玻璃管尾部塞一團浸有堿液的棉球是用于吸收過量的氯氣,以免其污染空氣
C. 玻璃管中,鈉燃燒時會產生蒼白色火焰
D. 若在棉球外沿滴一滴淀粉碘化鉀溶液,可據其顏色變化判斷氯氣是否被堿液完全吸收
(6)E裝置中發生反應的化學方程式是________________;為驗證E裝置反應后的溶液中存在Cl-,正確的操作是_____________。
查看答案和解析>>
科目: 來源: 題型:
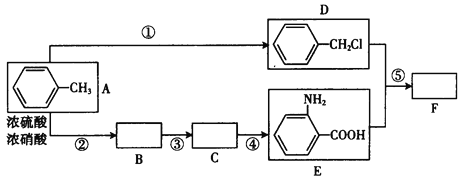
【題目】化合物F是用于制備藥品鹽酸祛炎痛的中間產物,已知其合成路線如下:
Ⅰ.RNH2+![]() CH2Cl
CH2Cl![]() RNHCH2
RNHCH2![]() +HCl(R和
+HCl(R和![]() 代表烴基)
代表烴基)
Ⅱ.苯的同系物易被高錳酸鉀溶液氧化如下:
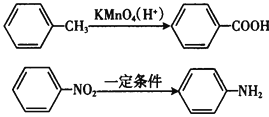
Ⅲ.苯胺具有弱堿性,易氧化。
回答下列問題:
(1)寫出反應①的反應物質和條件_____________,B中所含官能團的名稱_____________,C的結構簡式__________________。
(2)D+E→F的化學方程式:______________。
(3)E的一種同分異構體(對位氨基)在一定條件下,可聚合成熱固性很好的功能高分子,寫出合成此高聚物的化學方程式__________________。
(4)寫出D的含有苯環的同分異構體,已知該核磁共振氫譜圖有3種不同類型的氫原子,峰面積之比為3 :2 :2,則該物質是______________(寫結構簡式)。
(5)反應①~⑤中,屬于取代反應的是(填反應序號)________________,反應③的反應類型_____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】為探究原電池和電解池的工作原理,某研究性小組分別用如圖所示裝置進行實驗。
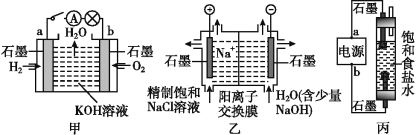
(1)甲裝置中,a電極的反應式為_______________________________________。
(2)乙裝置中,陰極區產物為________和_______。
(3)丙裝置是一種家用環保型消毒液發生器。外接電源a為_______(填“正”或“負”)極,該裝置內,發生的電解方程式為___________________________________、生成消毒液的方程式為________________________________________________________。
(4)若甲裝置作為乙裝置的電源,一段時間后,甲中消耗氣體與乙中產生氣體的物質的量之比為___________(不考慮氣體的溶解)。
(5)某工廠采用電解法處理含Cr2O72-的廢水,耐酸電解槽用鐵板作陰、陽極,槽內盛放含鉻廢水,Cr2O72-被還原成為Cr3+,Cr3+在陰極區生成Cr(OH)3沉淀除去,工作原理如圖:
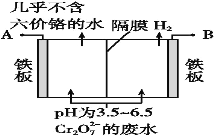
①寫出電解時陽極的電極反應式:______________________________________。
②寫出Cr2O72-被還原為Cr3+的離子方程式:____________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】[2016·新課標I]鍺(Ge)是典型的半導體元素,在電子、材料等領域應用廣泛。回答下列問題:
(1)基態Ge原子的核外電子排布式為[Ar]_______________,有__________個未成對電子。
(2)Ge與C是同族元素,C原子之間可以形成雙鍵、叁鍵,但Ge原子之間難以形成雙鍵或叁鍵。從原子結構角度分析,原因是______________________________。
(3)比較下列鍺鹵化物的熔點和沸點,分析其變化規律及原因______________________________。
GeCl4 | GeBr4 | GeI4 | |
熔點/℃ | 49.5 | 26 | 146 |
沸點/℃ | 83.1 | 186 | 約400 |
(4)光催化還原CO2制備CH4反應中,帶狀納米Zn2GeO4是該反應的良好催化劑。Zn、Ge、O電負性由大至小的順序是______________________________。
(5)Ge單晶具有金剛石型結構,其中Ge原子的雜化方式為_______________,微粒之間存在的作用力是_______________。
(6)晶胞有兩個基本要素:
①原子坐標參數,表示晶胞內部各原子的相對位置。如圖為Ge單晶的晶胞,其中原子坐標參數A為(0,0,0);B為(![]() ,0,
,0,![]() );C為(
);C為(![]() ,
,![]() ,0)。則D原子的坐標參數為_______________。
,0)。則D原子的坐標參數為_______________。

②晶胞參數,描述晶胞的大小和形狀。已知Ge單晶的晶胞參數a=565.76 pm,其密度為_____g·cm3(列出計算式即可)。
查看答案和解析>>
科目: 來源: 題型:
【題目】二草酸合銅酸鉀晶體{K2[Cu(C2O4)2]·2H2O)(相對分子質量為354),微溶于水和酒精,可溶于氨水,在干燥的環境下較為穩定。現以膽礬和草酸(H2C2O4)為原料制備二草酸合銅酸鉀晶體的流程如下:
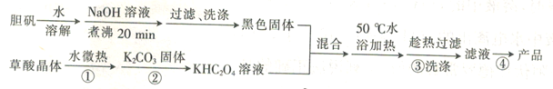
回答下列問題:
(1)K2[Cu(C2O4)2]·2H2O中Cu的化合價為___________。
(2)在常溫下,膽礬溶液與氫氧化鈉溶液反應生成氫氧化銅,當所得溶液的pH=7時,則溶液中c(Cu2+)=_________{已知該溫度下Ksp[Cu(OH)2]=2.2×10-20}。
(3)黑色固體的化學式為__________________,過濾時用到的玻璃儀器有漏斗、__________。
(4)草酸晶體受熱易分解,產物為CO、CO2和H2O,該反應的化學方程式為_____________。
(5)操作④后得到的晶體需用少量酒精洗滌,其目的是_________。
(6)產品的定量準確稱取2.000 g樣品溶于氨水中,并配成250 mL溶液,量取25.00 mL溶液于錐形瓶中,再加入10 mL 3.000 mol·L-1稀硫酸,用0.01000 mol·L-1KMnO4標準液滴定。
①若消耗KMnO4標準液的體積為20.00 mL,則該產品的純度是__________。
②滴定過程中如果盛裝標準液的滴定管沒有潤洗,則測得的結果將_______(填“偏高”或“偏低”或“無影響”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】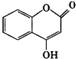 可用來制備抗凝血藥,通過如圖路線合成:
可用來制備抗凝血藥,通過如圖路線合成:
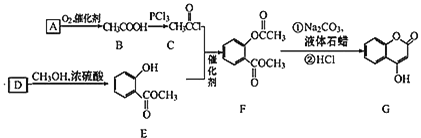
![]() 是一種氣態烴,寫出A的結構簡式 ______ ;
是一種氣態烴,寫出A的結構簡式 ______ ;
![]() 的反應類型是 ______ ;
的反應類型是 ______ ;
![]() 寫出
寫出![]() 的化學方程式 ______ ;
的化學方程式 ______ ;
![]() 下列關于G的說法正確的是 ______
下列關于G的說法正確的是 ______
![]() 能與溴單質反應
能與溴單質反應
![]() 能發生水解反應
能發生水解反應
![]() G最多能和5mol氫氣反應
G最多能和5mol氫氣反應
![]() 分子式是
分子式是![]()
![]() 寫出滿足以下條件的B的同系物所有同分異構體的結構簡式 ______
寫出滿足以下條件的B的同系物所有同分異構體的結構簡式 ______
![]() 分子式為
分子式為![]() 能發生銀鏡反應
能發生銀鏡反應![]() 能發生水解。
能發生水解。
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖所示,是原電池的裝置圖。請回答:
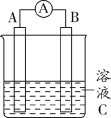
(1)若C為稀H2SO4溶液,電流表指針發生偏轉,B電極材料為Fe且作負極,則A電極上發生的電極反應式為_____________;反應進行一段時間后溶液C的pH將_____(填“升高”“降低”或“基本不變”)。
(2)若需將反應:Cu+2Fe3+=Cu2++2Fe2+設計成如圖所示的原電池裝置,則A(負極)極材料為____,B(正極)極材料為______,溶液C為_______。
(3)CO與H2反應還可制備CH3OH,CH3OH可作為燃料使用,用CH3OH和O2組合形成的質子交換膜燃料電池的結構示意圖如下:
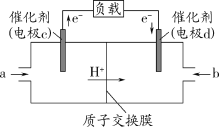
電池總反應為2CH3OH+3O2=2CO2+4H2O,則c電極是____(填“正極”或“負極”),c電極的反應方程式為______________。若線路中轉移2mol電子,則上述CH3OH燃料電池,消耗的O2在標準狀況下的體積為_____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com