
科目: 來源: 題型:
【題目】等質量的兩份鋅粉a和b,分別加入過量的稀硫酸中,a中同時加入少量CuSO4溶液,下列圖中表示其產生H2的總體積(V)與時間(t)的關系正確的是( )
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目: 來源: 題型:
【題目】下列敘述正確的是( )
A.生物質能與氫能均屬于一次能源
B.電解熔融MgCl2可以得到單質Mg和氯氣,該反應是一個放出能量的反應
C.相同狀況下,已知:2SO2+O2![]() 2SO3 ΔH<0,則2SO3
2SO3 ΔH<0,則2SO3![]() 2SO2+O2是一個吸熱反應
2SO2+O2是一個吸熱反應
D.取一定量的Ba(OH)2·8H2O晶體和NH4Cl晶體于燒杯中攪拌,燒杯壁下部變冷,放出的氣體使藍色石蕊試紙變紅
查看答案和解析>>
科目: 來源: 題型:
【題目】在探究新制氯水成分及性質的實驗中,依據下列方法和現象,不能得出相應結論的是
方法 | 現象 | 結論 | |
A | 觀察氯水顏色 | 氯水呈黃綠色 | 氯水中含Cl2 |
B | 向飽和NaHCO3溶液中加入足量氯水 | 有無色氣體產生 | 氯水中含HClO |
C | 向紅色紙條上滴加氯水 | 紅色紙條褪色 | 氯水具有漂白性 |
D | 向FeCl2溶液中滴加氯水 | 溶液變成棕黃色 | 氯水具有氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 來源: 題型:
【題目】現有某稀硫酸和稀硝酸的混合溶液200 mL,將其平均分成兩份。向其中一份中逐漸加入銅粉,最多能溶解9.6 g銅粉;向另一份中逐漸加入鐵粉,產生氣體的量隨鐵粉質量的變化關系如圖所示(假設硝酸的還原產物為NO氣體)。下列分析或結果正確的是
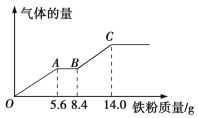
A. 原混合溶液中NO3-的物質的量為0.2 mol
B. OA段產生的是氫氣
C. BC段產生NO
D. 原混合溶液中H2SO4的濃度為1.25mol/L
查看答案和解析>>
科目: 來源: 題型:
【題目】關于化工生產原理的敘述中,不符合目前工業生產實際的是
A.硫酸工業中,三氧化硫在吸收塔內被水吸收制成濃硫酸
B.煉鐵工業中,用焦炭和空氣反應產生的一氧化碳在高溫下還原鐵礦石中的鐵
C.合成氨工業中,用鐵觸媒作催化劑,可提高單位時間氨的產量
D.氯堿工業中,電解槽的陰極區產生NaOH
查看答案和解析>>
科目: 來源: 題型:
【題目】T℃時,有甲、乙兩個密閉容器,甲容器的體積為1 L,乙容器的體積為2 L,分別向甲、乙兩容器中加入6 mol A和3 mol B,發生反應如下:3A(g)+bB(g)![]() 3C(g)+2D(g) ΔH<0;4 min時甲容器內的反應恰好達到平衡,A的濃度為2.4 mol/L,B的濃度為1.8 mol/L;t min時乙容器內的反應達平衡,B的濃度為0.8 mol/L。根據題給信息回答下列問題:
3C(g)+2D(g) ΔH<0;4 min時甲容器內的反應恰好達到平衡,A的濃度為2.4 mol/L,B的濃度為1.8 mol/L;t min時乙容器內的反應達平衡,B的濃度為0.8 mol/L。根據題給信息回答下列問題:
(1)甲容器中反應的平均速率v(B)=____,化學方程式中計量數b=____;
(2)乙容器中反應達到平衡時所需時間t___4min(填“大于”、“小于”或“等于”),原因是_____;
(3)若要使甲、乙容器中B的平衡濃度相等,可以采取的措施是___;
A. 保持溫度不變,增大甲容器的體積至2L
B. 保持容器體積不變,使甲容器升高溫度
C. 保持容器壓強和溫度都不變,向甲中加入一定量的A氣體
D. 保持容器壓強和溫度都不變,向甲中加入一定量的B氣體
(4)寫出平衡常數表達式K=____,并計算在T℃時的化學平衡常數K=____。
查看答案和解析>>
科目: 來源: 題型:
【題目】![]() 與濃硝酸反應生成氮氧化物,這些氮氧化物溶解在
與濃硝酸反應生成氮氧化物,這些氮氧化物溶解在![]() 溶液中生成
溶液中生成![]() 和
和![]() 的混合溶液,反應過程及有關數據如圖所示:
的混合溶液,反應過程及有關數據如圖所示:
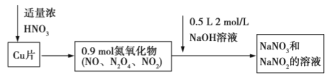
下列有關判斷正確的是( )
A.若![]() 片為
片為![]() ,則生成
,則生成![]()
B.![]() 遇濃硝酸發生鈍化,不可能發生上述反應
遇濃硝酸發生鈍化,不可能發生上述反應
C.標準狀況下收集的氮氧化物為![]()
D.![]() 既是氧化產物,也是還原產物
既是氧化產物,也是還原產物
查看答案和解析>>
科目: 來源: 題型:
【題目】在一定條件下,將![]() 體積NO和
體積NO和![]() 體積O2同時通入倒立于水中且盛滿水的容器中,充分反應后,容器內殘留
體積O2同時通入倒立于水中且盛滿水的容器中,充分反應后,容器內殘留![]() 體積的氣體,該氣體與空氣接觸變為紅棕色,則
體積的氣體,該氣體與空氣接觸變為紅棕色,則![]() 為( )
為( )
A. 3:2 B. 2:3 C. 8:3 D. 3:8
查看答案和解析>>
科目: 來源: 題型:
【題目】現用傳感技術測定噴泉實驗中的壓強變化來認識噴泉實驗的原理。下列說法正確的是

A. 制取氨氣時燒瓶中的固體常用CaO或CaCl2
B. 將濕潤的藍色石蕊試紙置于三頸瓶口,試紙變紅,說明NH3已經集滿
C. 關閉a,將單孔塞(插有吸入水的膠頭滴管)塞緊頸口c,打開b,完成噴泉實驗,電腦繪制三頸瓶內壓強變化曲線如圖2,則E點時噴泉最劇烈
D. 工業上,若出現液氨泄漏,噴稀鹽酸比噴灑NaHCO3溶液處理效果好
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com