
科目: 來源: 題型:
【題目】A、B、C、D、E為短周期元素,A-E原子序數依次增大,質子數之和為40,B、C同周期,A、D同主族,A、C能形成兩種液態化合物A2C和A2C2,E是地殼中含量最多的金屬元素。
(1)E元素在周期表中的位置為__________;B、C的氫化物穩定性強的是________(用化學式表示,下同);B、C、D組成的化合物中含有的化學鍵為_____________
(2)D2C2的電子式是_________,將D的單質投入A2C中,反應后得到一種無色溶液,E的單質在該無色溶液中反應的離子方程式為______________;
(3)元素D的單質在一定條件下,能與A單質化合生成氫化物DA,熔點為800℃。DA能與水反應放出氫氣,化學反應方程式為_____________。
(4)廢印刷電路版上含有銅,以往的回收方法是將其灼燒使銅轉化為氧化銅,再用硫酸溶解。現改用A2C2和稀硫酸浸泡既達到了上述目的,又保護了環境,試寫出反應的化學方程式__________________________
查看答案和解析>>
科目: 來源: 題型:
【題目】華法林(Warfarin)又名殺鼠靈,為心血管疾病的臨床藥物。其合成路線(部分反應條件略去) 如下所示:
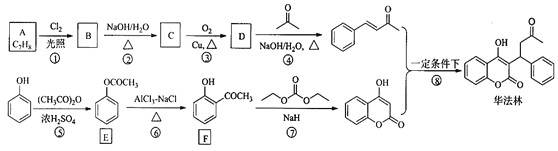
回答下列問題:
(1)A 的名稱為________,E 中官能團名稱為________。
(2)B 的結構簡式為________。
(3)由 C 生成 D 的化學方程式為___________
(4)⑤的反應類型為_________,⑧的反應類型為________。
(5)F 的同分異構體中,同時符合下列條件的同分異構體共有___________種。
a.能與 FeCl3 溶液發生顯色反應 b.含有-CHO
其中核磁共振氫譜為五組峰的結構簡式為___________
查看答案和解析>>
科目: 來源: 題型:
【題目】高鐵酸鉀(K2FeO4)是一種理想的綠色高效水處理劑。某學習小組用下圖所示裝置(夾持儀器已略去)制備KClO溶液,并通過KClO溶液與Fe(NO3)3溶液的反應制備K2FeO4。

查閱資料知K2FeO4的部分性質如下:①可溶于水、微溶于濃KOH溶液;②在0℃~5℃、強堿性溶液中比較穩定;③在Fe3+和Fe(OH)3催化作用下發生分解;④在酸性至弱堿性條件下,能與水反應生成Fe(OH)3和O2。
請回答下列問題:
(1)儀器C和D中都盛有KOH溶液,其中C中KOH溶液的用途是_________________。
(2)Cl2與KOH的濃溶液在較高溫度下反應生成KClO3。為保證反應生成KClO,需要將反應溫度控制在0~5℃下進行,在不改變KOH溶液濃度的前提下,實驗中可以采取的措施是___________。
(3)在攪拌下,將Fe(NO3)3飽和溶液緩慢滴加到KClO飽和溶液中即可制取K2FeO4,寫出該反應的化學方程式____________________________________________;該操作不能將KClO飽和溶液滴加到Fe(NO3)3飽和溶液中,其原因是________________________________________。
(4)制得的粗產品中含有Fe(OH)3、KCl等雜質。一種提純方案為:將一定量的K2FeO4粗產品溶于冷的3 mol·L-1KOH溶液中,用砂芯漏斗過濾,將濾液置于冰水浴中,向濾液中加入飽和KOH溶液,攪拌、靜置,再用砂芯漏斗過濾,晶體用適量乙醇洗滌2~3次后,在真空干燥箱中干燥。
①第一次和第二次過濾得到的固體分別對應的是(填化學式)______________、___________,過濾時不用普通漏斗而采用砂芯漏斗的原因是_____________________。
②晶體用乙醇洗滌的原因是________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】焰色實驗過程中,鉑絲的清洗和灼燒與鉀焰色實驗的觀察兩項操作如圖所示,下列敘述中不正確的是( )

A.每次實驗中都要先將鉑絲灼燒到火焰顏色,再蘸取被檢驗物質
B.鉀的焰色實驗要透過藍色鈷玻璃觀察
C.焰色實驗是某種金屬元素灼燒時所具有的特殊顏色,是化學變化
D.沒有鉑絲可用無銹鐵絲代替進行實驗
查看答案和解析>>
科目: 來源: 題型:
【題目】硒(Se)是人體健康必需的一種微量元素,已知Se的原子結構示意圖如圖:下列說法不正確的是

A. 該原子的質量數為34
B. 該元素處于第四周期第ⅥA族
C. SeO2既有氧化性又有還原性
D. 酸性:H2SO4>H2SeO4
查看答案和解析>>
科目: 來源: 題型:
【題目】2019年新發現的元素鉝(Lv)是116號主族元素,其原子核外最外層電子數是6。下列說法不正確的是 ( )
A.Lv位于第七周期第VIA族B.Lv在同主族元素中金屬性最弱
C.Lv的同位素原子具有相同的電子數D.中子數為177的Lv核素符號為![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】工業上以軟錳礦(主要成分是MnO2,含有SiO2、Fe2O3等少量雜質)為主要原料制備高性能的磁性材料碳酸錳(MnCO3)。其工業流程如下:
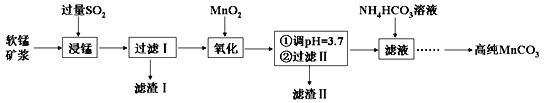
(1)過濾Ⅰ所得濾渣Ⅰ的主要成分為_________(填化學式)。
(2)“氧化”過程中除了發生MnO2與SO2的反應外,還發生另一氧化還原反應,寫出該反應的離子方程式:__________________________。
(3)“浸錳”反應中往往有副產物MnS2O6生成,溫度對“浸錳”反應的影響如右圖所示,為減少 MnS2O6 的生成,“浸錳”的適宜溫度是_______。
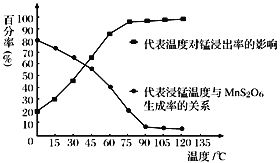
(4)向過濾Ⅱ所得的濾液中加入NH4HCO3 溶液時溫度控制在30-35℃,溫度不宜太高的原因是_______。
(5)加入NH4HCO3溶液后,生成MnCO3沉淀,同時還有CO2氣體生成,寫出反應的離子方程式:_____________。
(6)生成的MnCO3沉淀需經充分洗滌,檢驗洗滌是否完全的方法是______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】A、B、C均為單質,其中A為用途廣泛的金屬單質,B為黃綠色氣體,B與C反應后的產物E溶于水得無色酸性溶液。A、B、C之間的其他反應如圖所示。
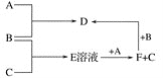
試填空:
(1)寫出下列物質的化學式:
B________,D________,F________。
(2)鑒別D溶液中陽離子的方法是________________________。
(3)寫出下列反應的離子方程式:
①A+E→F+C:____________________________________________________。
②B+F→D:________________________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】CH4和CO2反應可以制造價值更高的化學產品.
(1)250℃時,以鎳合金為催化劑,向4L容器中通入6molCO2、6molCH4,發生反應:CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)平衡體系中各組分的濃度為:
2CO(g)+2H2(g)平衡體系中各組分的濃度為:
物質 | CH4 | CO2 | CO | H2 |
平衡濃度mol/L | 0.5 | 0.5 | 2.0 | 2.0 |
①此溫度下,該反應的平衡常數K=______注明單位.
②已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH1kJmol-1
CO(g)+H2O(g)=CO2(g)+H2(g) ΔH2kJmol-1
2CO(g)+O2(g)=2CO2(g) ΔH3kJmol-1
反應CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)的ΔH=______ kJmol-1
2CO(g)+2H2(g)的ΔH=______ kJmol-1
(2)用Cu2Al2O4做催化劑,一定條件下,發生反應:CO2+CH4![]() CH3COOH,請回答:
CH3COOH,請回答:
①溫度與催化劑的催化效率和乙酸的生成速率如圖250~300℃時,溫度升高而乙酸的生成速率降低的原因是______
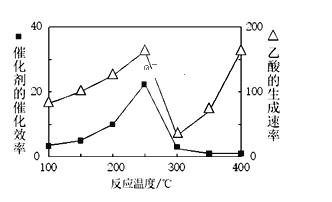
②為提高上述反應CH4的轉化率,可采取的措施有______(寫2種)
③Cu2Al2O4可溶解在稀硝酸中,被氧化的元素為______,每消耗3molCu2Al2O4時被還原的HNO3為______mol
(3)Li2O、Na2O、MgO均能吸收CO2,
①若尋找吸收CO2的其他物質,下列建議合理的是______
a.可在堿性氧化物中尋找
b.可在具有強氧化性的物質中尋找
c.可在ⅠA、ⅡA族元素的氧化物中尋找
②Li4SiO4可用于吸收、釋放CO2,原理是:500℃時, CO2與Li4SiO4接觸生成Li2CO3;平衡后加熱至700℃,反應逆向進行,放出CO2, Li4SiO4再生,該原理的化學方程式______.
查看答案和解析>>
科目: 來源: 題型:
【題目】用來減輕感冒癥狀的布洛芬的結構簡式如圖所示,下列有關說法不正確的是( )
![]()
A.1mol布洛芬能與足量NaHCO3溶液反應最多生成1molCO2
B.布洛芬的分子式為C13H18O2
C.布洛芬苯環上的一溴代物有2種
D.布洛芬與苯甲酸甲酯是同系物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com