
科目: 來源: 題型:
【題目】下列有關說法正確的是( )
A. 實驗室制氫氣,為了加快反應速率,可向稀硫酸中滴加少量硝酸銅溶液
B. 可用勒夏特列原理解釋2NO2(g)![]() N2O4(g)體系加壓后顏色變深
N2O4(g)體系加壓后顏色變深
C. N2(g)+ 3H2(g)![]() 2NH3(g) ΔH<0可通過加壓方式增大其平衡常數
2NH3(g) ΔH<0可通過加壓方式增大其平衡常數
D. 二氧化硫和乙烯兩種氣體分別通入Br2的CCl4溶液,能使溶液褪色的是乙烯氣體
查看答案和解析>>
科目: 來源: 題型:
【題目】SO2、CO、CO2、NOx是對環境影響較大的幾種氣體,對它們的合理控制和治理是優化我們生存環境的有效途徑.

(1)利用電化學原理將CO、SO2轉化為重要化工原料,裝置如圖1所示:
①若A為CO,B為H2,C為CH3OH,則通入CO的為_________極(填“正”或“負”)。
②若A為SO2,B為O2,C為H2SO4,則負極的電極反應式為:___________________________。
(2)碳酸鹽燃料電池,以一定比例Li2CO3和Na2CO3低熔混合物為電解質,操作溫度為650℃,在此溫度下以鎳為催化劑,以煤氣(CO、H2的體積比為1∶1)直接做燃料,其工作原理如圖2所示。
①電池總反應為____________________________________________。
②以此電源電解足量的硝酸銀溶液,若陰極產物的質量為21.6g,電解后溶液體積為2L,溶液的pH約為___________。
(3)某研究小組利用下列裝置用N2O4生產新型硝化劑N2O5。

①現以H2、O2、熔融鹽Na2CO3組成燃料電池,采用電解法制備N2O5,裝置如圖所示,其中Y為CO2。在該電極上同時還引入CO2的目的是__________________________。
②電解過程中,生成N2O5的電極反應方程式為_________________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】A、B、C、X均為中學常見的物質,它們之間有如下轉化關系(反應條件及副產物已略去)。
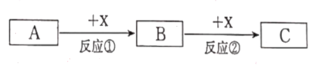
(1)若A和X均為單質,B為可使品紅溶液褪色的氣體,則反應②的化學方程式為____。
(2)若A、B、C為含鈉元素的化合物,X為無色無味氣體,則反應②的化學方程式為______ 。
(3)若A為稀硝酸,B溶液和硫氰酸鉀溶液反應后溶液顯紅色,則反應②的離子方程式為_____。若向C的溶液中加入氫氧化鈉溶液產生白色沉淀,在空氣中迅速變成_____,最后變成_______,白色沉淀發生上述變化的原因 ______(用化學方程式表示)。56 g X與足量的稀硝酸發生反應,被還原的HNO3為__________g。
查看答案和解析>>
科目: 來源: 題型:
【題目】化學電源在日常生活和工業生產中有著重要的應用。
I.如下圖所示,某同學設計了一個燃料電池并探究氯堿工業原理和粗銅的精煉原理,其中乙裝置中X為陽離子交換膜。請按要求回答相關問題
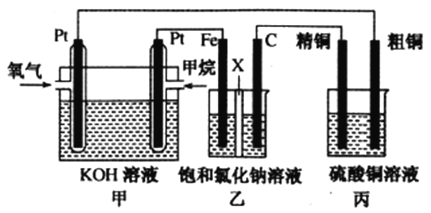
(1)甲烷燃料電池負極反應式是______________________。
(2)石墨(C)極的電極反應式為______________________。
(3)若在標準狀況下,有2.24L氧氣參加反應,則乙裝置中鐵極上生成的氣體體積為___________L;丙裝置中陰極析出銅的質量為___________g,一段時間后燒杯中c(Cu2+)___________(填“增大”、“減小”或“不變”)
Ⅱ.“長征”火箭發射使用的燃料是液態偏二甲肼(C2H8N2),并使用四氧化二氮作為氧化劑,這種組合的兩大優點是,既能在短時間內產生巨大能量將火箭送上太空,產物又不污染空氣(產物都是空氣成分)。某校外研究性學習小組擬將此原理設計為原電池,如圖所示,結合學習過的電化學原理分析其設計方案,回答相關問題:
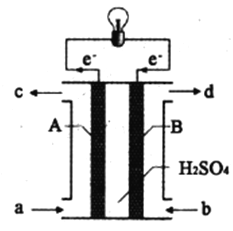
(4)從a口加入___________(填名稱)。H+移動方向是___________(填“A到B”或“B到A”)
(5)A極發生的電極反應式:______________________。
(6)若以該電池為電源用石墨做電極電解200mL0.5mol/L的CuSO4溶液,電解一段時間后,兩極收集到相同體積(相同條件)的氣體,則整個電解過程轉移的電子的數目是___________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某課題組以納米Fe2O3作為電極材料制備鋰離子電池(另一極為金屬鋰和石墨的復合材料),通過在室溫條件下對鋰離子電池進行循環充放電,成功地實現了對磁性的可逆調控(如圖)。下列說法正確的是( )
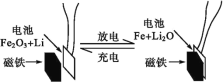
A.放電時,正極的電極反應式為Fe2O3+6Li++6e-=2Fe+3Li2O
B.該電池可以用水溶液作電解質溶液
C.放電時,Fe作電池的負極,Fe2O3作電池的正極
D.充電完成后,電池被磁鐵吸引
查看答案和解析>>
科目: 來源: 題型:
【題目】下列說法或表示法正確的是( )
A.等量的硫蒸氣和硫固體分別完全燃燒,后者放出的熱量多
B.使用催化劑的反應是吸熱反應
C.在稀溶液中:H++OH﹣=H2O ΔH=﹣57.3 kJ·mol-1,若將含 1 molCH3COOH 的醋酸溶液與含 1 mol NaOH 的溶液混合,放出的熱量小于 57.3 kJ
D.在 101 kPa 時,2 g H2 完全燃燒生成液態水,放出 285.8 kJ 熱量,氫氣燃燒的熱化學方程式表示為 2H2(g)+O2(g)=2H2O(l)ΔH=+285.8 kJ·mol-1
查看答案和解析>>
科目: 來源: 題型:
【題目】新型鋅碘液流電池具有能量密度高、循環壽命長等優勢,其工作原理如圖所示。下列說法錯誤的是

A. 放電時電流從石墨電極流向鋅電極
B. 充電時陽極反應式為:3I--2e-=I3-
C. 若將陽離子交換膜換成陰離子交換膜,放電時正負極也隨之改變
D. 放電時左側電解質儲罐中的離子總濃度增大
查看答案和解析>>
科目: 來源: 題型:
【題目】銅板上鐵鉚釘處的吸氧腐蝕原理如圖所示,下列有關說法正確的是
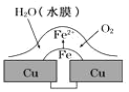
A.陽極電極反應式為:2H++2e→H2↑
B.此過程中電子從 Fe 移向 Cu,鐵鉚釘發生還原反應
C.此過程中銅會被腐蝕,發生氧化反應
D.此過程中鐵做負極,被氧化
查看答案和解析>>
科目: 來源: 題型:
【題目】向20 mL 0.40 mol/L H2O2溶液中加入少量KI溶液:ⅰ.H2O2+I-=H2O+IO﹣;ⅱ.H2O2+IO﹣= H2O+O2↑+ I﹣。H2O2分解反應過程中能量變化和不同時刻測得生成O2的體積(已折算標準狀況)如下。

t/min | 0 | 5 | 10 | 15 | 20 |
V(O2)/mL | 0.0 | 12.6 | 20.16 | 28.0 | 32.7 |
下列判斷不正確的是
A. 從圖中可以看出,KI能增大H2O2的分解速率
B. 反應ⅰ是放熱反應,反應ⅱ是吸熱反應
C. 0~10 min的平均反應速率:v(H2O2)≈9.0×10-3 mol/(L·min)
D. H2O2在反應過程中既體現了氧化性,又體現了還原性
查看答案和解析>>
科目: 來源: 題型:
【題目】在不同電壓下用惰性電極電解飽和NaCl溶液制備少量NaClO,實驗結果如下:
實驗 | ① | ② | ③ |
電壓 | U1 | U2 | U3 |
現象 | a極產生少量氣泡,b極無明顯氣泡 | a極產生較多氣泡,b極產生少量氣泡 | a極產生大量氣泡,b極逸出大量黃綠色氣體 |
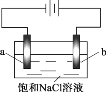
下列分析不正確的是
A. ①、②、③中,a極均發生了還原反應
B. ①、②、③中均能發生Cl2+2NaOH =NaCl+NaClO+H2O
C. 電解時OH- 由b極向a極移動
D. 不宜采用實驗③的電壓制備NaClO
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com