
科目: 來源: 題型:
【題目】以冶銅工廠預處理過的污泥渣(主要成分為 CuO 和 Cu)為原料制備 CuSO45H2O 晶體的流程如下 :
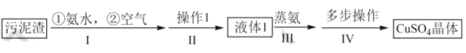
已知:①CuO在氨水作用下可以生成 Cu(NH3)4(OH)2
②CuSO45 H2O 加熱到 4 5℃時開始失水。
請回答:
(1)步驟 l 中,空氣的主要作用是____。
(2)下列關于步驟II說法不正確的是____。
A.操作 1 可選擇傾析法過濾, 玻璃棒的作用是: 先攪拌, 再引流
B.操作 1 應趁熱過濾, 要防止液體 1 中的溶質因冷卻而析出
C.操作 1 為抽濾,在加入需抽濾的物質時,用玻璃棒引流液體, 玻璃棒底端需緊貼在濾紙上
D.抽濾時,布氏漏斗的底部斜口面需正對抽濾瓶的抽氣口處, 是為了提高抽濾的速率
(3)液體 1 通過步驟 III 與步驟IV可得到CuSO45 H2O 晶體 。
①蒸氨過程的生成物均是由兩種元素組成的化合物, 則除氨外其余產物的化學式為_____。
②步驟IV中包含多步操作, 將下列步驟按正確的步驟排序(必要時步驟可重復選)。_____→得到固體物質→ ____ →將液體放于蒸發皿中加熱→ ____→_____→_____→_____ →得到晶體
a.過濾 b.用玻璃棒不斷攪拌溶液 c.用足量稀硫酸溶解固體 d.停止加熱 e.至溶液表面析出晶膜
(4)步驟1中分別選用氨水、氨水-碳酸銨混合溶液氨浸時, 銅元素回收率隨溫度變化如圖所示。
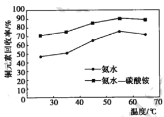
①浸取液為氨水時,反應溫度控制為 55℃,溫度過高銅元素回收率降低的原因是_______。
②浸取液為氨水一碳酸銨混合溶液時,銅元素回收率受溫度影響較小的原因可能是______。
(5)為了提高 CuSO4晶體的產率, 實驗室還采用以下方法: 將CuSO4 溶液轉移至蒸餾燒瓶中, 加入適量冰醋酸, 通過下圖所示的裝置獲取晶體。
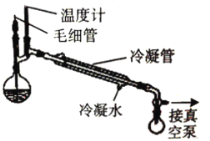
①加入適量乙酸的目的是:_____。
②圖中接真空泵的作用是:______。
查看答案和解析>>
科目: 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列有關敘述不正確的是( )
A. 標準狀況下,1L庚烷完全燃燒所生成的氣態產物的分子數為(7/22.4)NA
B. 1 mol甲基(-CH3)所含的電子總數為9NA
C. 0.5 mol1,3-丁二烯分子中含有碳碳雙鍵數為NA
D. 1 mol碳正離子(CH3+)所含的電子總數為8NA
查看答案和解析>>
科目: 來源: 題型:
【題目】根據已經學過的化學知識,回答下列問題。
I.金屬及其化合物在生產生活中有著廣泛的應用,
(1)胃舒平(主要成分為氫氧化鋁)可用于治療胃酸過多,氫氧化鋁體現_______性;_______(填“能”或“不能”)用氫氧化鈉溶液代替。
(2)將Cu與稀硫酸混合,二者不能反應,滴入H2O2后,溶液很快變成藍色,該反應的化學方程式為____________________________________________。
(3)NaHSO4是一種酸式鹽,寫出NaHSO4在水中的電離方程式_________________________。
II.物質的量是學習化學的基礎。
(1)14.4 g CO和CO2的混合氣體在標準狀況下所占的體積為8.96 L,其中CO的質量為_____。
(2)市售濃H2SO4的質量分數為98%、密度為1.84g/cm3,其濃度為________mol·L-1。
(3)19g某二價金屬的氯化物ACl2中含有0.4mo1Cl-離子,金屬A的相對原子質量是_______。
(4)根據反應14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知當有2.5 mol FeS2參加反應時,被氧化的硫的物質的量為_______mol。
查看答案和解析>>
科目: 來源: 題型:
【題目】氧元素和鹵族元素都能形成多種物質,我們可以利用所學物質結構與性質的相關知識去認識和理解。
(1)COCl2的空間構型為______________,溴的基態原子價電子排布式為_____________。
(2)已知CsICl2不穩定,受熱易分解,傾向于生成晶格能更大的物質,則它按下列_____________(填字母)式發生。
A.CsICl2====CsCl+ICl B.CsICl2====CsI+Cl2
(3)根據表提供的第一電離能數據判斷,最有可能生成較穩定的單核陽離子的鹵素原子是____。
元素 | 氟 | 氯 | 溴 | 碘 |
第一電離能/ (kJ·mol-1) | 1681 | 1251 | 1140 | 1008 |
(4)下列分子既不存在“s-p”σ鍵,也不存在“p-p”π鍵的是__________(填字母)。
A.HCl B.HF C.SO2 D.SCl2
(5)已知ClO2-為“V”形,中心氯原子周圍有4對價層電子。ClO2-中心氯原子的雜化軌道類型為______________,寫出一個與CN—互為等電子體的物質的分子式:______________。
(6)鈣在氧氣中燃燒時得到一種鈣的氧化物晶體,其結構如圖所示,由此可判斷鈣的氧化物的化學式為__________。已知該氧化物的密度是ρg·cm-3,則晶胞內離得最近的兩個鈣離子的間距為_________cm(只要求列算式,不必計算出數值,阿伏加德羅常數的值為NA)。

查看答案和解析>>
科目: 來源: 題型:
【題目】二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑,回答下列問題:
(1)實驗室用NH4Cl、鹽酸、NaClO2(亞氯酸鈉)為原料,通過以下過程制備ClO2:
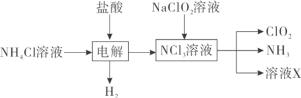
①電解時陽極電極反應式為__________________________。
②除去ClO2中的NH3可選用的試劑是___________(填標號)。
a.水 b.堿石灰 c.濃硫酸 d.飽和食鹽水
(2)用如圖裝置可以測定混合氣中ClO2的含量:
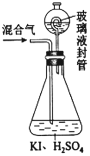
Ⅰ.在錐形瓶中加入足量的碘化鉀,用50mL水溶解后,再加入3mL稀硫酸:
Ⅱ.在玻璃液封裝置中加入水,使液面沒過玻璃液封管的管口;
Ⅲ.將一定量的混合氣體通入錐形瓶中吸收;
Ⅳ.將玻璃液封裝置中的水倒入錐形瓶中:
Ⅴ.用0.1000mol·L-1硫代硫酸鈉標準溶液滴定錐形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示劑顯示終點時共用去20.00mL硫代硫酸鈉溶液。在此過程中:
①錐形瓶內ClO2與碘化鉀反應的離子方程式為______________________。
②玻璃液封裝置的作用是______________________。
③V中加入指示劑,滴定至終點的現象是______________________。
④測得混合氣中ClO2的質量為______g。
⑤某同學用某部分刻度模糊不清的50mL滴定管進行實驗,當滴定管中的液面處于如圖所示的刻度處,則管內液體的體積________(填代號)。
a.等于23.60mL b.等于27.60mL c.小于23.60mL d.大于27.60mL
![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】下圖是用KClO3與濃鹽酸反應制取氯氣的簡易裝置。下列說法正確的是
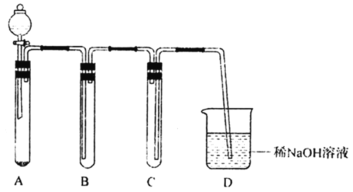
A.A中固體也可以用高錳酸鉀、重鉻酸鉀、二氧化錳等代替
B.裝置A發生反應的方程式為KClO3+6HCl(濃)=3Cl2↑+KCl+3H2O
C.待沒有氣泡產生后,向A中加入足量AgNO3,根據沉淀質量可求出剩余鹽酸的量
D.裝置B盛放的是飽和食鹽水,目的為除去HCl
查看答案和解析>>
科目: 來源: 題型:
【題目】“84消毒液”因1984年北京某醫院研制使用而得名,在2020年抗擊新型冠狀病毒肺炎中被廣泛用于消毒,其有效成分是NaClO。某校化學研究性學習小組在實驗室制備NaClO溶液,并進行性質探究和成分測定。
已知:①室溫下,飽和NaClO溶液pH為11
②25℃時,H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;HClO:Ka=3.0×10-8
I.制備NaClO溶液
該學習小組按下圖裝置進行實驗(部分夾持裝置省去)
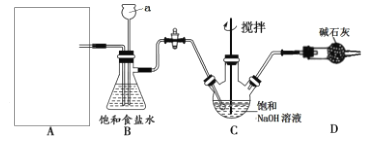
(1)上圖中A為實驗室制備Cl2的發生裝置,可以選用下列圖中_(填代號)裝置,用該裝置制備Cl2反應的化學方程式為__。
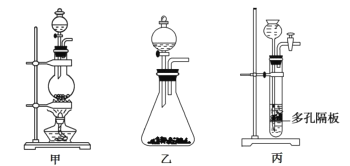
(2)B裝置中儀器a的名稱是____,B裝置可除去氯氣中氯化氫雜質, 此外還有______作用(寫出一點)。
II.NaClO性質探究
按上圖裝置進行實驗,一段時間后,取C瓶中的溶液進行實驗,如下表:
實驗內容 | 實驗現象 | |
實驗l | 取樣,滴加紫色石蕊試液 | 變藍,不褪色 |
實驗2 | 測定溶液的pH | 12 |
(3)C瓶溶液中的溶質除NaCl外,還有______(填化學式)。
(4)將C瓶中NaOH溶液換成NaHCO3溶液,反應一段時間后,取C瓶中的溶液按上表實驗內容進行實驗。現象為:實驗l中紫色石蕊試液立即褪色,實驗2中溶液的pH=7。結合平衡移動原理解釋紫色石蕊試液立即褪色的原因是________。
III.測定C瓶溶液中NaClO含量(單位:g·L-1)
i.取C瓶溶液10.00mL于錐形瓶中,加入適量硫酸酸化,迅速加入過量KI溶液,蓋緊瓶塞并在暗處充分反應。
ii.用0.1000molL-1Na2S2O3標準溶液滴定上述錐形瓶中的溶液至終點,重復操作2~3次,消耗Na2S2O3溶液的平均用量為12.00mL。(已知:I2+2![]() =2I-+
=2I-+![]() )
)
(5)i中主要發生反應的離子方程式為_______,ii中用_______作指示劑。
(6)蓋緊瓶塞并在暗處反應的原因是________。
(7)C瓶溶液中NaClO含量是______g·L-1(保留2位小數)。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列圖象表示的意義與相關的化學反應完全正確的是
A.向FeCl3溶液中不斷加入鐵粉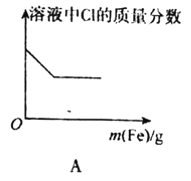
B.Fe(OH)2固體露置在空氣中質量的變化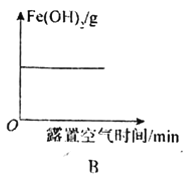
C.25℃時,向Cl2水溶液中通入二氧化硫(生成兩種常見的酸) 
D.向AlCl3溶液中不斷滴入燒堿溶液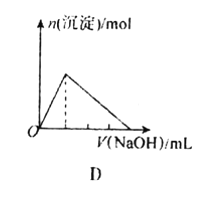
查看答案和解析>>
科目: 來源: 題型:
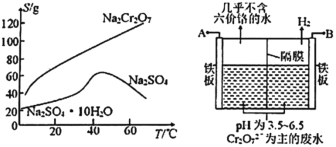
【題目】鉻渣是生產金屬鉻和鉻鹽過程中產生的工業廢渣,其中含有Na2SO4及少量Cr2O72—、Fe3+。從鉻渣中提取Na2SO4的工藝流程:
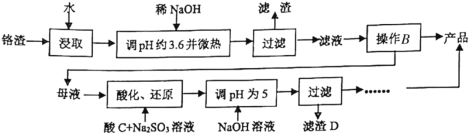
已知:常溫時,Fe3+、Cr3+完全沉淀時c≤1×10-5mol·L-1,Ksp[Fe(OH)3]=4×10-38,Ksp[Cr(OH)3]=6×10-31。
(1)調pH約為3.6目的是_________。
(2)根據下圖溶解度(S)—溫度(T)曲線,判斷操作B為蒸發濃縮、_________________。
(3)“酸化、還原”步驟反應的離子方程式為_______________________________。
(4)濾渣D為________________________(填化學式)。
(5)如圖,某工廠采用電解法處理含鉻廢水,用鐵板作陰陽極,槽中盛放含鉻廢水,A接電源的_______極;陽極區溶液中發生的氧化還原反應為__________________。若不考慮氣體的溶解,當收集到6.72L(標準狀況)的H2時,理論上有___molCr2O72—被還原。
查看答案和解析>>
科目: 來源: 題型:
【題目】利用下列實驗裝置能完成相應實驗的是
選項 | 裝置圖 | 實驗目的 |
A |
| 收集干燥的HCl |
B |
| 除去CO2中含有的少量HCl |
C |
| 收集H2、NH3、CO2、Cl2、HCl、NO、NO2等氣體 |
D |
| 檢查裝置的氣密性 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com