
科目: 來源: 題型:
【題目】(1)以下列出的是一些原子的2p能級和3d能級中電子排布的情況,試判斷哪些違反了泡利原理__________,哪些違反了洪特規則__________。

(2)某元素的激發態(不穩定狀態)原子的電子排布式為1s22s22p63s13p33d2,則該元素基態原子的電子排布式為__________;其最高價氧化物對應水化物的化學式是__________。
(3)將下列多電子原子的原子軌道按軌道能量由低到高順序排列。
①2s ②3d ③4s ④3s ⑤4p ⑥3p
軌道能量由低到高排列順序是__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】能說明SiO2為酸性氧化物的事實為( )
A.SiO2與H2SO4、HNO3不反應B.SiO2+4HF=SiF4↑+2H2O
C.SiO2+2KOH=K2SiO3+H2OD.SiO2+2C![]() Si+2CO↑
Si+2CO↑
查看答案和解析>>
科目: 來源: 題型:
【題目】有機物K是某藥物的合成中間體,其合成路線如圖所示:
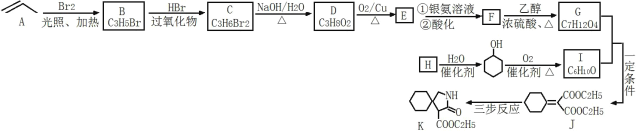
已知:HBr與不對稱烯烴加成時,在過氧化物作用下,則鹵原子連接到含氫較多的雙鍵碳上;
請回答下列問題:
(1)C的化學名稱為____,J中官能團的名稱是____;
(2)H→![]() 的原子利用率為100%,則H的結構簡式為____;
的原子利用率為100%,則H的結構簡式為____;
(3)C→D的化學方程式為____;
(4)E與足量的Ag(NH3)2OH溶液反應的化學方程式為____;
(5)L是G的同分異構體,則滿足下列條件的L的結構簡式為____(任寫一種結構即可)。
①lmol L與足量的NaHCO3溶液反應能生成2molCO2;
②L的核磁共振氫譜有3組峰且峰面積之比為1︰2︰3。
查看答案和解析>>
科目: 來源: 題型:
【題目】氯可形成多種含氧酸鹽,廣泛應用于殺菌、消毒及化工領域。實驗室中利用下圖裝置(部分裝置省略)制備KClO3和NaClO,探究其氧化還原性質。
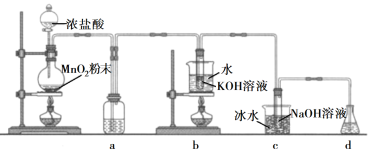
回答下列問題:
(1)盛放MnO2粉末的儀器名稱是________,a中的試劑為________。
(2)b中采用的加熱方式是_________,c中化學反應的離子方程式是________________,采用冰水浴冷卻的目的是____________。
(3)d的作用是________,可選用試劑________(填標號)。
A.Na2S B.NaCl C.Ca(OH)2 D.H2SO4
(4)反應結束后,取出b中試管,經冷卻結晶,________,__________,干燥,得到KClO3晶體。
(5)取少量KClO3和NaClO溶液分別置于1號和2號試管中,滴加中性KI溶液。1號試管溶液顏色不變。2號試管溶液變為棕色,加入CCl4振蕩,靜置后CCl4層顯____色。可知該條件下KClO3的氧化能力____NaClO(填“大于”或“小于")。
查看答案和解析>>
科目: 來源: 題型:
【題目】乙苯是重要的化工原料,利用乙苯為初始原料合成高分子化合物J的流程如圖所示(部分產物及反應條件已略去):

已知:①R1CHO+R2CH2CHO![]() +H2O
+H2O
②
請回答下列問題:
(1)物質B的名稱為____;F的結構簡式為____;
(2)②、③的反應類型分別為____、____;
(3)物質H中官能團的名稱是____;
(4)反應④的化學方程式為____;
(5)與G互為同分異構體,符合下列條件的芳香族化合物共有____種;
ⅰ.遇FeCl3顯紫色
ⅱ.含碳碳叁鍵
(6)參照上述合成路線和信息,設計![]() 、乙醛、苯甲醇為原料合成
、乙醛、苯甲醇為原料合成 的路線(無機試劑任選)____。
的路線(無機試劑任選)____。
查看答案和解析>>
科目: 來源: 題型:
【題目】NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉膠體,選擇適當的試劑和方法從中提純出NaCl晶體。相應的實驗過程如圖:
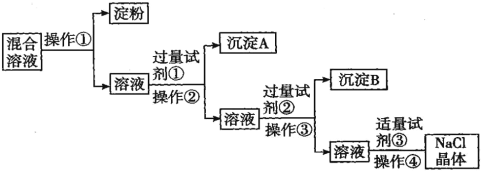
(1)操作①的名稱是___________
(2)試劑①的化學式是____________ 判斷試劑①已過量的方法是:________________________
(3)加入試劑②發生的離子方程式是____________________________________。
(4)操作④的名稱是:_____________
查看答案和解析>>
科目: 來源: 題型:
【題目】三氯乙醛是基本有機合成原料之一,是生產農藥、醫藥的重要中間體。某化學興趣小組設計如圖所示裝置(夾持、加熱儀器略),模擬工業生產進行制備三氯乙醛(CCl3CHO)的實驗。
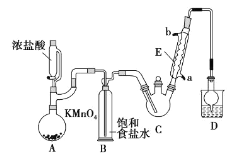
查閱資料,有關信息如下:
①制備反應原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能發生的副反應:C2H5OH+HCl→C2H5Cl+H2O、CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相關物質的相對分子質量及部分物理性質:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相對分子質量 | 46 | 147.5 | 163.5 | 64.5 |
熔點/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸點/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 與水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
回答下列問題:
(1)儀器E的名稱是____,冷凝水的流向是____口進水(填“a”或“b”)。
(2)有同學認為該裝置存在一處缺陷,應在BC之間加一干燥裝置,理由是____。
(3)該裝置C控制反應溫度在70℃左右,可采用____加熱的方法;
(4)裝置D干燥管的作用為____,裝置D燒杯中的試劑是____。
(5)反應結束后,從C中的混合物中分離出Cl3CCOOH的方法是(填名稱)____。
查看答案和解析>>
科目: 來源: 題型:
【題目】電爐加熱時用純O2氧化管內樣品,根據產物的質量確定有機物的組成。如圖1裝置是用燃燒法確定有機物分子式常用的裝置。
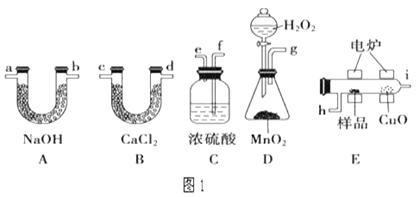
(1)燃燒管中CuO的作用是_____。
(2)若實驗中所取樣品只含C、H、O三種元素中的兩種或三種,準確稱取1.48g樣品,經充分反應后,A管質量增加3.52g,B管質量增加1.8g,則該樣品的實驗式為_____。
(3)用質譜儀測定其相對分子質量,得如圖2所示的質譜圖,則該有機物的相對分子質量為_____。
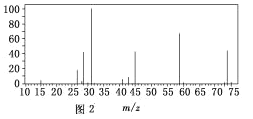
(4)若只根據A的實驗式能否確定其分子式____(填“能”或“不能”)。
(5)該物質的紅外光譜圖如圖3所示,則其結構簡式為____。
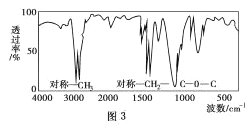
查看答案和解析>>
科目: 來源: 題型:
【題目】氨硼烷(NH3BH3)含氫量高、熱穩定性好,是一種具有潛力的固體儲氫材料。回答下列問題:
(1)H、B、N中,原子半徑最大的是______。根據對角線規則,B的一些化學性質與元素______的相似。
(2)NH3BH3分子中,N—B化學鍵稱為____鍵,其電子對由____提供。氨硼烷在催化劑作用下水解釋放氫氣:3NH3BH3+6H2O=3NH3+![]() +9H2,
+9H2,![]() 的結構如圖所示:
的結構如圖所示: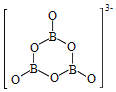 ;在該反應中,B原子的雜化軌道類型由______變為______。
;在該反應中,B原子的雜化軌道類型由______變為______。
(3)NH3BH3分子中,與N原子相連的H呈正電性(Hδ+),與B原子相連的H呈負電性(Hδ-),電負性大小順序是__________。與NH3BH3原子總數相等的等電子體是_________(寫分子式),其熔點比NH3BH3____________(填“高”或“低”),原因是在NH3BH3分子之間,存在____________________,也稱“雙氫鍵”。
(4)研究發現,氦硼烷在低溫高壓條件下為正交晶系結構,晶胞參數分別為a pm、b pm、c pm,α=β=γ=90°。氨硼烷的2×2×2超晶胞結構如圖所示。
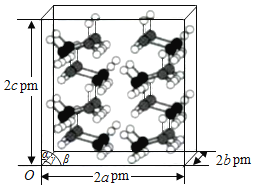
氨硼烷晶體的密度ρ=___________g·cm3(列出計算式,設NA為阿伏加德羅常數的值)。
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖為實驗室制取純凈、干燥的氯氣,并驗證氯氣性質的裝置。其中E瓶放有干燥紅色布條;F中為紅色的銅網,其右端出氣管口放有脫脂棉。
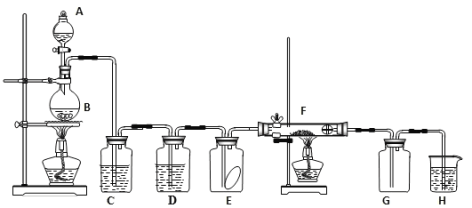
(1)裝置C中盛裝的溶液是____________,D中試劑的作用是____________________。
(2)E中的紅色布條是否褪色?____(填“是”或“否”),寫出F中反應的化學反應方程式:____________________,其反應現象為__________________________。
(3)H中的試劑為___________,用來吸收多余氯氣。工業上常用廉價的石灰乳吸收工業氯氣尾氣制得漂白粉,該反應的化學方程式為_________________________。
(4)8.7gMnO2固體與足量濃鹽酸充分反應,在標準狀況下產生Cl2的體積為_____L;其中被氧化的HCl的物質的量為_______mol。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com