
科目: 來源: 題型:
【題目】分枝酸可用于生化研究。其結構簡式如圖。下列關于分枝酸的敘述正確的是

A. 分子中含有2種官能團
B. 可與乙醇、乙酸反應,且反應類型相同
C. 1mol分枝酸最多可與3molNaOH發生中和反應
D. 可使溴的四氯化碳溶液、酸性高錳酸鉀溶液褪色,且原理相同
查看答案和解析>>
科目: 來源: 題型:
【題目】四種短周期主族元素W、X、Y、Z的原子序數依次增大,W、X的簡單離子具有相同電子層結構,X的原子半徑是短周期主族元素原子中最大的,W與Y同族,Z與X形成的離子化合物的水溶液呈中性。下列說法正確的是( )
A.簡單離子半徑:![]()
B.W與X形成的化合物溶于水后溶液呈堿性
C.氣態氫化物的熱穩定性:![]()
D.最高價氧化物的水化物的酸性:![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】微生物電池是指在微生物的作用下將化學能轉化為電能的裝置,其工作原理如圖所示。下列有關微生物電池的說法錯誤的是( )
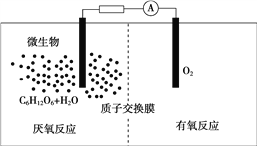
A. 微生物促進了反應中電子的轉移
B. 正極反應中有CO2生成
C. 質子通過交換膜從負極區移向正極區
D. 電池總反應為C6H12O6+6O2===6CO2+6H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】化合物X(只含兩種短周期元素)是一種重要的還原劑。某同學取X做了如下實驗
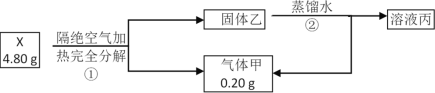
請回答:
(1)X的電子式是____________
(2)固體乙所含元素在元素周期表中的位置____________。
(3)寫出X與水反應的化學方程式____________。
(4)X在無水條件下可作為某些鋼鐵制品的脫銹劑(鐵銹的成分表示為Fe2O3),脫銹過程發生反應的化學方程式____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某同學利用下圖裝置測定CaCO3和稀鹽酸反應的反應速率,開始時電子秤的示數為225.8 g,50 s后示數為223.6 g,則50 s內此反應的平均反應速率v(HCl)為(假定反應過程中溶液體積不變,且藥品足量)( )
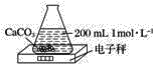
A.0.01 mol·L-1·s-1
B.0.05 mol·L-1·s-1
C.0.02 mol·L-1·s-1
D.0.1 mol·L-1·s-1
查看答案和解析>>
科目: 來源: 題型:
【題目】某學習小組探究潮濕的Cl2與Na2CO3反應的產物,進行如下實驗根據設計要求回答:
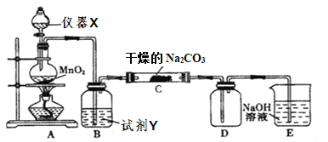
⑴X儀器名稱是____________。
⑵裝置A中發生反應的離子方程式:____________。
⑶B裝置中試劑Y的作用是____________。
⑷下列有關該實驗的說法中,不正確的是____________。
A.如圖組裝好實驗儀器后,要先檢查裝置氣密性,后添加藥品
B.E裝置的作用是吸收尾氣防止污染空氣
C.裝置C中Cl2與Na2CO3以等物質的量反應,且生成的氣體產物僅為Cl2O,可知反應方程式為2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+Cl2O↑
D.試劑Y是濃硫酸,目的是干燥氯氣
⑸設計實驗方案驗證C中生成的固體中存在![]() ____________。
____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】醋酸銅[(CH3COO)2Cu·H2O](其相對式量為200)常用作分析化學的分析試劑,還用作有機合成催化劑、瓷釉顏料等。可以用堿式碳酸銅與醋酸作用來制備。
實驗步驟:
(I)堿式碳酸銅的制備

(Ⅱ)醋酸銅的制備
堿式碳酸銅與醋酸反應制得醋酸銅:
Cu(OH)2·CuCO3+4CH3COOH=2(CH3COO)2Cu·H2O+CO2↑+H2O
將產品堿式碳酸銅放入燒杯內,加入約20mL蒸餾水,加熱攪拌至323K左右,逐滴加入適量醋酸至固體不再溶解,趁熱過濾。濾液在通風櫥下蒸發至原體積的![]() 左右,冷卻至室溫,減壓過濾,用少量蒸餾水洗滌,得(CH3COO)2Cu·H2O產品,稱量,計算產率。
左右,冷卻至室溫,減壓過濾,用少量蒸餾水洗滌,得(CH3COO)2Cu·H2O產品,稱量,計算產率。
回答下列問題:
(1)步驟(ⅰ)將研磨后混合物注入熱水中反應,寫出離子反應方程式______。
(2)堿式碳酸銅的制備需在熱水中進行反應,且溫度需控制在60℃左右,請解釋原因______。
(3)在步驟(ⅰ)與步驟(ⅱ)的實驗過程中,涉及三種固液分離的方法,分別是傾析法過濾、趁熱過濾與減壓過濾,下列裝置中沒有使用到的有______。
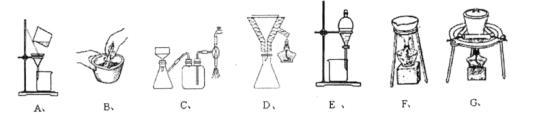
(4)步驟ⅱ中洗滌晶體的具體操作是______。
(5)最終稱量所得的產品為8.0g,則產率為______。
查看答案和解析>>
科目: 來源: 題型:
【題目】下圖是氫氧燃料電池的示意圖,按圖中提示,下列敘述不正確的是( )

A. a電極是負極,b電極是正極
B. a電極的電極反應式為H2-2e-===2H+
C. b電極的電極反應式為4OH--4e-===2H2O+O2↑
D. 氫氧燃料電池不需要將還原劑和氧化劑全部儲藏在電池內
查看答案和解析>>
科目: 來源: 題型:
【題目】300mL某溶液中可能含有Na+、NH4+、Mg2+、Ba2+、CO32-、SO42-、Cl-中的若干種,現將此溶液分成三等份,進行如下實驗:
①向第一份中加入AgNO3溶液,有白色沉淀產生;
②向第二份中加足量KOH溶液并加熱,收集到氣體0.04 mol;(銨鹽與堿共熱可產生氨氣)
③向第三份中加足量BaCl2溶液,得到沉淀6.27g,加入足量鹽酸充分反應后,剩余沉淀2.33g。根據上述實驗,回答下列問題:
(1)實驗③中生成沉淀的離子方程式為________,沉淀溶解的離子方程式為__________。
(2)溶液中一定不存在的離子有_________。
(3)實驗①中加入AgNO3溶液,有沉淀產生,能否說明原溶液中含有Cl-?________(填“能”或“否”)理由是______________。
(4)推斷鈉離子是否存在并說明理由_________。若存在,計算其物質的量的濃度____________(若不存在,此問不作答)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com