
科目: 來源: 題型:
【題目】綠原酸是一種新型高效的酚型天然抗氧化劑,在食品行業有著廣泛的用途。其在酸性條件下發生如下反應,下列有關說法不正確的是
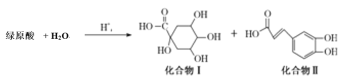
A.上述變化發生取代反應
B.1mol化合物I與足量金屬鈉反應生成標準狀況下氫氣體積為56L
C.1mol化合物II與濃溴水反應時,消耗4molBr2
D.1mol化合物II與足量的Na2CO3反應得到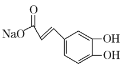
查看答案和解析>>
科目: 來源: 題型:
【題目】NA是阿伏加德羅常數的值,下列說法正確的是
A.1molK2Cr2O7被還原為Cr3+轉移的電子數為3NA
B.0.1molCH4與Cl2在光照下反應生成的CH3Cl分子數為0.1NA
C.0.1molFeCl3完全水解轉化為氫氧化鐵膠體,生成0.1NA個膠粒
D.乙烯和環丙烷組成的42g混合氣體中氫原子的個數為6NA
查看答案和解析>>
科目: 來源: 題型:
【題目】國際貿易可以互通有無,符合國際社會的根本利益,下列貿易商品中,主要成分屬于無機物的是
A.巴西鐵礦砂 | B.沙特石油 | C.俄羅斯天然氣 | D.中國絲綢 |
|
|
|
|
A.AB.BC.CD.D
查看答案和解析>>
科目: 來源: 題型:
【題目】當氨分子中的三個氫原子依次被其它原子或基團取代時,所形成的化合物叫做氨的衍生物。主要有N2H4(肼)、HN3(疊氮化氫,溶于水稱為疊氮酸)、NH2OH(羥胺)。水合肼(N2H4·H2O)是制備疊氮化鈉(NaN3)的原料,而疊氮化鈉又是汽車安全氣囊最理想的氣體發生劑的原料。下面是工業水合肼法制備疊氮化鈉的工藝流程。
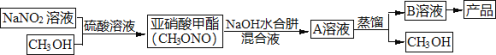
資料:①水合肼有毒且不穩定,具有強還原性和強堿性;
②有關物質的物理性質如下表:
物質 | 甲醇 | 水合肼 | 亞硝酸甲酯 | 疊氮化鈉 |
熔點(℃) | -97 | -40 | -17 | 275(410℃:易分解) |
沸點(℃) | 64.7 | 118.5 | -12 | — |
回答下列問題:
I.合成水合肼。實驗室合成水合肼裝置如下圖所示,NaClO堿性溶液與尿素CO(NH2)2水溶液在400C以下反應一段時間后,再迅速升溫至1100℃繼續反應可以制得水合肼。
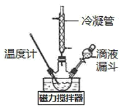
(1)實驗中通過滴液漏斗向三頸瓶中緩慢滴加NaClO堿性溶液,不能反向滴加的原因是______________;制取N2H4H2O的離子方程式為_______________________。
II.制備疊氮化鈉。實驗室可利用下圖中所示的裝置及藥品制備疊氮化鈉。
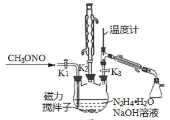
(2)①根據實驗發現溫度在20℃左右反應的轉化率最高,因此可釆取的措施是_______________;流程中蒸餾A溶液時,裝置中旋塞K1、K2、K3的開關情況是_______________________。
②寫出該方法制備疊氮化鈉的化學方程式:________________________。
(3)流程中由B溶液獲得疊氮化鈉產品的實驗步驟為____________________,減壓過濾,晶體用乙醇洗滌23次后,干燥。
(4)化工生產中,多余的疊氮化鈉常使用次氯酸鈉溶液處理,在酸性條件下,二者反應可生成無毒的氣體。若處理6.5gNaN3,理論上需加入0.5molL的NaClO溶液_____________mL。
III.羥胺(NH2OH)是一種還原劑,可以通過下列過程得到:乙烯和N2O4氣體混合后,光照,發生加成反應,得到化合物A。A結構對稱,所有相同元素的原子化學環境相同。A在某濃度的硫酸溶液中回餾,可得到化合物B,同時得到CO和CO2組成的混合氣體(相對氫氣密度為18)。經分析,B為不含碳元素的硫酸鹽,其硫和氧元素的質量分數分別為19.51%和58.54%。若將A換成CH3CH2NO2進行類似的反應,也能得到B,但沒有氣體放出。B在液氨中即得到NH2OH。
(5)NH2OH具有弱堿性,可與酸反應生成鹽,該鹽陽離子的電子式為_______________。
(6)寫出A→B的化學方程式________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖所示的各圖中,表示2A(g)+B(g)2C(g)(△H<0)這個可逆反應的正確圖象為(注:(C)表示C的質量分數,P表示氣體壓強,C表示濃度)
A.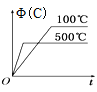 B.
B.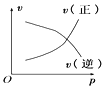 C.
C.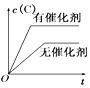 D.
D.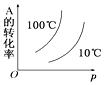
查看答案和解析>>
科目: 來源: 題型:
【題目】已知299 K時,合成氨反應 N2(g ) + 3H2 ( g )![]() 2NH3( g ) △H = -92.0 kJ/mol,將此溫度下的1 mol N2和3 mol H2放在一密閉容器中,在催化劑存在時進行反應,測得反應放出的熱量為(忽略能量損失)
2NH3( g ) △H = -92.0 kJ/mol,將此溫度下的1 mol N2和3 mol H2放在一密閉容器中,在催化劑存在時進行反應,測得反應放出的熱量為(忽略能量損失)
A. 一定大于92.0 kJB. 一定等于92.0 kJ
C. 一定小于92.0 kJD. 不能確定
查看答案和解析>>
科目: 來源: 題型:
【題目】硅及其化合物是重要的材料,應用范圍很廣。請回答下列問題:
(1)制備硅半導體材料必須先得到高純硅,三氯甲硅烷(SiHCl3)還原法是當前制備高純硅的主要方法,生產過程示意圖如下:
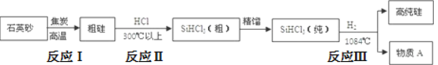
①用石英砂和焦炭高溫加熱時有碳化硅生成,該反應的化學方程式為______________。
②寫出由純SiHCl3制備高純硅的化學反應方程式:________________。
③SiHCl3遇水劇烈反應生成H2SiO3、HCl和另一種物質,寫出并配平該化學反應方程式:________________。
(2)水泥屬于硅酸鹽工業產品,是重要的建筑材料。水泥熟料的主要成分為CaO、SiO2,并含有一定量的鐵、鋁和鎂等金屬的氧化物。實驗室測定水泥樣品中鈣含量的過程如圖所示:
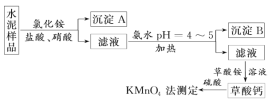
回答下列問題:
①在分解水泥樣品過程中,以鹽酸為溶劑,氯化銨為助溶劑,還需加入幾滴硝酸。加入硝酸的目的是_______________,還可使用_________代替硝酸。
②沉淀A的主要成分是__________,其不溶于強酸但可與一種弱酸反應,該反應的化學方程式為________。
③加氨水過程中加熱的目的是_______。沉淀B的主要成分為________、_______(寫化學式)。
查看答案和解析>>
科目: 來源: 題型:
【題目】唑啉草酯H是用于麥田的具有新穎結構的苯基吡唑啉除草劑。一種合成路線如下:
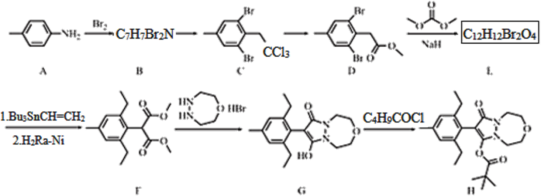
回答下列問題:
(1)A的化學名稱為__________
(2)B的結構簡式為__________
(3)G→H的反應類型為__,下列關于G、H的說法正確的是______(填選項字母)。
A.G不含手性碳原子,H含有一個手性碳原子
B.二者均能使酸性KMnO4溶液褪色
C.二者均含有3種含氧官能團
D.二者各1mol時,最多消耗H2的物質的量不相等
(4)寫出D→E的化學反應方程式:__________.
(5)同時滿足下列條件的F的同分異構體Ⅰ的結構有________種(不考慮立體異構),寫出兩種核磁共振氫譜顯示有3種不同化學環境的氫,且峰面積之比為9:1:1的Ⅰ的結構簡式:_________________
①苯環上連有2個相同的叔丁基[-C(CH3)3]②苯環上只有2個H③1molⅠ能與2molNaHCO3反應產生無色氣體
(6)已知:CH2=CH-R1+HBr→R1-CHBr-CH3,CH2=CH-R1+HBr![]() R1-CH2-CH2Br結合題給信息,寫出以2-甲基-1-丙烯和
R1-CH2-CH2Br結合題給信息,寫出以2-甲基-1-丙烯和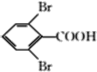 為原料(其他試劑任選)制備化合物
為原料(其他試劑任選)制備化合物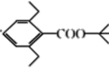 的合成路線:____________。
的合成路線:____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某同學設計實驗探究工業制乙烯的原理和乙烯的主要化學性質,實驗裝置如圖所示(已知烴類都不與堿反應)。請回答下列問題:

(1)工業制乙烯的實驗原理是烷烴(液態)在催化劑和加熱條件下發生反應生成不飽和烴。例如,石油分餾產物之一的十六烷烴發生反應:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,則甲的分子式為________,乙的結構簡式為____________________________________。
4乙,則甲的分子式為________,乙的結構簡式為____________________________________。
(2)B裝置中的實驗現象可能是________,寫出反應的化學方程式:__________,其反應類型是________。
(3)C裝置中可觀察到的現象是____________,反應類型是________。
(4)查閱資料知,乙烯與酸性高錳酸鉀溶液反應產生二氧化碳。根據本實驗中裝置_____(填字母)中的實驗現象可判斷該資料是否真實。為了探究溴與乙烯反應是加成反應而不是取代反應,可以測定裝置B中溶液在反應前后的酸堿性,簡述其理由: __________________。
(5)通過上述實驗探究,檢驗甲烷和乙烯的方法是________(選填字母,下同);除去甲烷中乙烯的方法是________。
A.氣體通入水中 B.氣體通過盛溴水的洗氣瓶
C.氣體通過盛酸性高錳酸鉀溶液的洗氣瓶 D.氣體通過氫氧化鈉溶液
(6)分別燃燒乙烯和甲烷,甲烷火焰明亮而乙烯產生少量黑煙,原因是_________________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com