
科目: 來源: 題型:
【題目】利用制磷肥的副產物氟硅酸鈉(Na2SiF6)生產冰晶石(Na3AlF6)的工藝流程如下:

(1)分解過程發生的反應為Na2SiF6+4NH3·H2O===2NaF+4NH4F+X↓+2H2O。工業上把濾渣X叫白炭黑,其化學式為__。
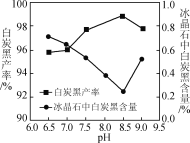
(2)分解時白炭黑產率和冰晶石純度與pH的關系如圖,分解時需要控制溶液的pH=______,能提高其分解速率的措施有____(填字母)。
A. 快速攪拌 B. 加熱混合液至100 ℃ C. 減小氨水濃度
(3)流程中可循環利用的物質為_____;冰晶石在電解冶煉鋁中的作用是_____。
(4)水浴加熱過程中生成冰晶石的化學方程式為____。
查看答案和解析>>
科目: 來源: 題型:
【題目】新型電池在飛速發展的信息技術中發揮著越來越重要的作用。Li2FeSiO4是極具發展潛力的新型鋰離子電池電極材料,在蘋果的幾款最新型的產品中已經有了一定程度的應用。其中一種制備Li2FeSiO4的方法為:固相法:2Li2SiO3+FeSO4![]() Li2FeSiO4+Li2SO4+SiO2
Li2FeSiO4+Li2SO4+SiO2
某學習小組按如下實驗流程制備Li2FeSiO4并測定所得產品中Li2FeSiO4的含量。
實驗(一)制備流程:
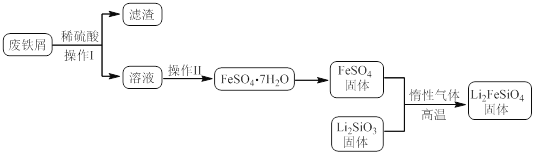
實驗(二) Li2FeSiO4含量測定:
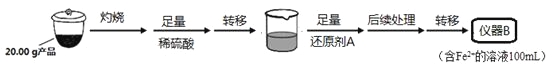
從儀器B中取20.00 mL溶液至錐形瓶中,另取0.2000 mol·Lˉ1的酸性KMnO4標準溶液裝入儀器C中,用氧化還原滴定法測定Fe2+含量。相關反應為:MnO4- +5Fe2++8H+=Mn2++5Fe3++4H2O,雜質不與酸性KMnO4標準溶液反應。經4次滴定,每次消耗KMnO4溶液的體積如下:
實驗序號 | 1 | 2 | 3 | 4 |
消耗KMnO4溶液體積 | 20.00 mL | 19.98mL | 21.38mL | 20.02mL |
(1)實驗(二)中的儀器名稱:儀器B ,儀器C 。
(2)制備Li2FeSiO4時必須在惰性氣體氛圍中進行,其原因是 。
(3)操作Ⅱ的步驟 ,在操作Ⅰ時,所需用到的玻璃儀器中,除了普通漏斗、燒杯外,還需 。
(4)還原劑A可用SO2,寫出該反應的離子方程式 ,此時后續處理的主要目的是 。
(5)滴定終點時現象為 ;根據滴定結果,可確定產品中Li2FeSiO4的質量分數為 ;若滴定前滴定管尖嘴處有氣泡,滴定后消失,會使測得的Li2FeSiO4含量 。(填“偏高”、“偏低”或“不變”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】研究CO2的利用對促進低碳社會的構建具有重要意義。
⑴ 將CO2與焦炭作用生成CO,CO可用于煉鐵等。
已知:Fe2O3(s) + 3C(石墨) = 2Fe(s) + 3CO(g) ΔH 1 = +489.0 kJ·mol-1
C(石墨) + CO2(g) =2CO(g) ΔH 2 = +172.5 kJ·mol-1
則CO還原Fe2O3(s)的熱化學方程式為___________________________________________。
⑵ 二氧化碳合成甲醇是碳減排的新方向,將CO2轉化為甲醇的熱化學方程式為:CO2(g) +3H2(g)![]() CH3OH(g) +H2O(g) ΔH
CH3OH(g) +H2O(g) ΔH
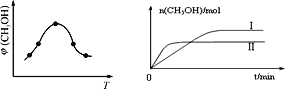
① 取一定體積CO2和H2的混合氣體(物質的量之比為1∶3),加入恒容密閉容器中,發生上述反應。反應過程中測得甲醇的體積分數φ(CH3OH)與反應溫度T的關系如圖所示,則該反應ΔH_______0(填“>”、“<”或“=”)。
② 在兩種不同條件下發生反應,測得CH3OH的物質的量隨時間變化如圖所示,曲線I、Ⅱ對應的平衡常數大小關系為:KⅠ______KⅡ(填“>” 或“<”)。
⑶ 以CO2為原料還可以合成多種物質。①工業上尿素[CO(NH2)2]由CO2和NH3在一定條件下合成,其反應方程式為_____________________________________。當氨碳比n(NH3 )/n(CO2 )=3,達平衡時CO2的轉化率為60%,則NH3的平衡轉化率為______。
查看答案和解析>>
科目: 來源: 題型:
【題目】某化學興趣小組利用NaI溶液中通入少量Cl2得到含碘廢液,再利用含碘廢液獲取NaI固體,實驗流程如下:

已知反應②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列問題:
(1)過濾實驗所需要的玻璃儀器有普通漏斗、燒杯、_____________。
(2)反應③中CuI被氧化,還原產物只有NO2,該反應的化學方程式為_________________。當有95.5 g CuI參與反應,則需要標況下______________L的O2才能將生成的NO2在水中完全轉化為硝酸。
(3)化合物B中含兩種元素,鐵原子與另一種元素原子的物質的量之比為3∶8,則化合物B的化學式為_____________。
(4)反應⑤中生成黑色固體和無色氣體,黑色固體的俗稱為磁性氧化鐵,則反應⑤的化學方程式為______。
(5)將足量的Cl2通入含12 g NaI的溶液中,一段時間后把溶液蒸干得到固體的質量為_________g。
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)化學反應2A(g)+B(?)![]() 2C(g)達到化學平衡時:
2C(g)達到化學平衡時:
①升高溫度時,C的量減少,則反應物的能量總和____________生成物的能量總和(填“>”、“<”或“=”)。
②如果增大壓強,平衡向正反應方向移動,則B是____________態物質。
③若增加B的物質的量,平衡不移動,說明B是____________態物質。
(2)如圖,在恒壓密閉容器中加入2 mol A和2 mol B,起始時容器體積為V L,發生如下反應并達到化學平衡狀態:2 A(g)+B(g)![]() x C(g)。平衡時,A、B、C的物質的量之比為1∶3∶4,C的物質的量為 y mol。
x C(g)。平衡時,A、B、C的物質的量之比為1∶3∶4,C的物質的量為 y mol。
 根據題中數據計算,x =_________、y =_________;
根據題中數據計算,x =_________、y =_________;
查看答案和解析>>
科目: 來源: 題型:
【題目】已知:2Fe2++Cl2=2Cl﹣+2Fe3+,2Br﹣+Cl2=Br2+2Cl﹣,2Fe2++Br2=2Br﹣+2Fe3+。在bL FeBr2溶液中通入amol Cl2時,使溶液中50% 的Br﹣氧化為Br2,則原FeBr2的物質的量濃度為
A. a/bmolL﹣1 B. 2a/bmolL﹣1 C. 3a/bmolL﹣1 D. 5a/bmolL﹣1
查看答案和解析>>
科目: 來源: 題型:
【題目】化合物I是合成抗心律失常藥普羅帕酮的前驅體,其合成路線如下:

已知:CH3COCH3+CH3CHO![]() CH3COCH=CHCH3+H2O
CH3COCH=CHCH3+H2O
回答下列問題:
(1)A的名稱_______。B的分子式為__________。
(2)A生成B的反應類型是_________;C生成D的反應類型是_________。
(3)F的結構簡式為________;H的結構簡式為________。
(4)化合物E中含有的兩種官能團名稱分別是________、_________;寫出一種同時符合下列條件的E的同分異構體的結構簡式:_____________。
①能發生銀鏡反應和水解反應
②核磁共振氫譜上顯示4組峰
(5)參照上述合成路線,以2-丙醇和苯甲醛為原料(無機試劑任選),設計制備![]() 的合成路線:________
的合成路線:________![]()
![]() (補出前面兩步)。
(補出前面兩步)。
查看答案和解析>>
科目: 來源: 題型:
【題目】2020年2月15日,由國家科研攻關組的主要成員單位的專家組共同研判磷酸氯喹在細胞水平上能
有效抑制新型冠狀病毒(2019-nCoV)的感染。
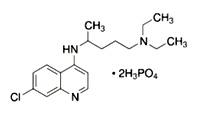
(1)已知磷酸氯喹的結構如圖所示,則所含C、N、O三種元素第一電離能由大到小的順序為_______________。P原子核外價層電子排布式為________,其核外電子有____個空間運動狀態。
(2)磷酸氯喹中N原子的雜化方式為_________,NH3是一種極易溶于水的氣體,其沸點比AsH3的沸點高,其原因是_______________________。
(3)H3PO4中PO43- 的空間構型為________________。
(4)磷化鎵是一種由ⅢA族元素鎵(Ga)與VA族元素磷(P)人工合成的Ⅲ—V族化合物半導體材料。晶胞結構可看作金剛石晶胞內部的碳原子被P原子代替,頂點和面心的碳原子被Ga原子代替。
①磷化鎵晶體中含有的化學鍵類型為__________(填選項字母)
A.離子鍵 B.配位鍵 C.σ鍵 D.π鍵 E.極性鍵 F.非極性鍵
②以晶胞參數為單位長度建立的坐標系可以表示晶胞中各原子的位置,稱作原子分數坐標。若沿y軸投影的晶胞中所有原子的分布圖如圖,則原子2的分數坐標為______________。
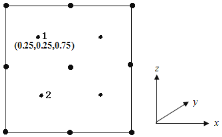
③若磷化鎵的晶體密度為ρ g·cm-3,阿伏加德羅常數的值為NA,則晶胞中Ga和P原子的最近距離為___________pm。
查看答案和解析>>
科目: 來源: 題型:
【題目】氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用。
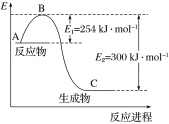
(1)上圖是N2(g)和H2(g)反應生成1 mol NH3(g)過程中能量的變化示意圖,請寫出N2和H2反應的熱化學方程式:______________。
(2)若已知下列數據:
化學鍵 | H—H | N≡N |
鍵能/kJ·mol-1 | 435 | 943 |
試根據表中及圖中數據計算N—H的鍵能:________ kJ·mol-1。
(3)用NH3催化還原NOx還可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ·mol-1①
N2(g)+O2(g)===2NO(g) ΔH2=-b kJ·mol-1②
若1 mol NH3還原NO至N2,則該反應過程中的反應熱ΔH3=________ kJ·mol-1(用含a、b的式子表示)。
(4)捕碳技術(主要指捕獲CO2)在降低溫室氣體排放中具有重要的作用。目前NH3和(NH4)2CO3已經被用作工業捕碳劑,它們與CO2可發生如下可逆反應:
反應Ⅰ:2NH3(l)+H2O(l)+CO2(g) ![]() (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反應Ⅱ:NH3(l)+H2O(l)+CO2(g) ![]() NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反應Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) ![]() 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
則ΔH3與ΔH1、ΔH2之間的關系是ΔH3=________。
查看答案和解析>>
科目: 來源: 題型:
【題目】丙烯是重要的工業品,可用于制取鹵代烴、丙醇及塑料等。回答下列問題:
(1)丙烯與HCl加成生成CH3CHClCH3或CH3CH2CH2Cl的能量與反應歷程如圖:
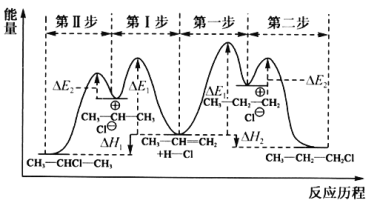
①從能量角度看,較穩定的產物是________(填“CH3CHClCH3”或“CH3CH2CH2Cl”)。
②制取CH3CHClCH3時,反應速率較慢的步驟是________(填“Ⅰ”或“Ⅱ”)。
(2)丙烷直接脫氫制丙烯的相關熱化學反應如下:
主反應:C3H8(g)→C3H6(g)+H2 ΔH1=+124.27kJ·mol-1
副反應:C3H8(g)→CH4(g)+C2H4(g) ΔH2=+81.30kJ·mol-1
C3H8(g)+H2(g)→CH4(g)+C2H6(g) ΔH3=-55.64kJ·mol-1
C2H4(g)+H2(g)→C2H6(g) ΔH4
①ΔH4=_____________kJ·mol-1
②分別在0.1Mpa和0.01Mpa時,丙烷和丙烯的平衡物質的量分數如圖所示:
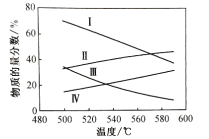
表示0.1Mpa時丙烷物質的量分數的是________(填羅馬數字,下同);表示0.01Mpa時丙烯物質量的分數的是________。
(3)用二氧化碳氧化丙烷制丙烯主要反應如下:
Ⅰ.C3H8(g)![]() C3H6(g)+ H2 ΔH1>0平衡常數K1
C3H6(g)+ H2 ΔH1>0平衡常數K1
Ⅱ.CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH2>0平衡常數K2
CO(g)+H2O(g) ΔH2>0平衡常數K2
Ⅲ.耦合反應C3H8(g)+CO2(g)![]() C3H6(g)+CO(g)+H2O(g)
C3H6(g)+CO(g)+H2O(g)
當C3H8的物質的量一定時,按不同投料比Z[Z=![]() ]向密閉容器中充入C3H8和CO2,發生反應Ⅲ,C3H8平衡轉化率隨溫度變化如圖所示:
]向密閉容器中充入C3H8和CO2,發生反應Ⅲ,C3H8平衡轉化率隨溫度變化如圖所示:
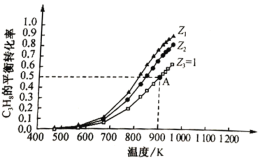
①反應Ⅲ的平衡常數K=________(用K1、K2表示)。
②Z1________(填“>”“<”“=”)Z2。原因是________
③若A點氣體總壓強為0.2Mpa,則丙烯的平衡分壓為________MPa;900K時反應Ⅲ的平衡常數Kp=________MPa(Kp為用平衡分壓表示的平衡常數)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com