
科目: 來源: 題型:
【題目】用Pt極電解含有Ag+、Cu2+和X3+各0.1 mol的溶液,陰極析出固體物質的質量m (g)與回路中通過電子的物質的量n (mol)關系如圖所示。則下列氧化性強弱的判斷正確的是

A. Ag+>X3+>Cu2+>H+>X2+
B. Ag+>Cu2+>X3+>H+>X2+
C. Cu2+>X3十>Ag十>X2+>H+
D. Cu2+>Ag+>X3+>H+>X2+
查看答案和解析>>
科目: 來源: 題型:
【題目】高純MnCO3在電子工業中有重要的應用,工業上利用軟錳礦(主要成分是MnO2,還含有Fe2O3、CaCO3、CuO等雜質)制取碳酸錳的流程如圖所示:

已知:還原焙燒主反應為2MnO2+C![]() 2MnO+CO2↑。
2MnO+CO2↑。
可能用到的數據如下:

根據要求回答下列問題:
(1)在實驗室進行步驟A,混合物應放在__________中加熱。
(2)步驟E中調節pH的范圍為____________,其目的是______________________________。
(3)步驟G,溫度控制在35℃以下的原因是____________________________________,若Mn2+恰好沉淀完全(當離子濃度≦10-5mol/L認為該離子沉淀完全)時測得溶液中![]() 的濃度為2.2×10-6mol/L,則Ksp(MnCO3)=____________。
的濃度為2.2×10-6mol/L,則Ksp(MnCO3)=____________。
(4)步驟D中氧化劑與還原劑的物質的量之比為__________;步驟C中的濾渣為__________。
(5)生成的MnCO3沉淀需經充分洗滌,檢驗洗滌是否干凈的方法是_____________________。
(6)現用滴定法測定產品中錳元素的含量。實驗步驟:稱取3.300 g試樣,向其中加入稍過量的磷酸和硝酸,加熱使產品中MnCO3完全轉化為[Mn(PO4)2]3-(其中![]() 完全轉化為
完全轉化為![]() );加入稍過量的硫酸銨,發生反應NO2-+
);加入稍過量的硫酸銨,發生反應NO2-+![]() =N2↑+2H2O以除去
=N2↑+2H2O以除去![]() ;加入稀硫酸酸化,再加入60.00 mL 0.500 mol·L-1硫酸亞鐵銨溶液,發生的反應為[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2
;加入稀硫酸酸化,再加入60.00 mL 0.500 mol·L-1硫酸亞鐵銨溶液,發生的反應為[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2![]() ;用5.00 mL 0.500 mol·L-1酸性K2Cr2O7溶液恰好除去過量的Fe2+。
;用5.00 mL 0.500 mol·L-1酸性K2Cr2O7溶液恰好除去過量的Fe2+。
①酸性K2Cr2O7溶液與Fe2+反應的離子方程式為_____________________________________。
②試樣中錳元素的質量分數為____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】二氧化硫是重要的化工原料,用途非常廣泛。
實驗一:SO2可以抑制細菌滋生,具有防腐功效。某實驗小組欲用下圖所示裝置測定某品牌葡萄酒中(葡萄酒中含有乙醇、有機酸等)的SO2含量。
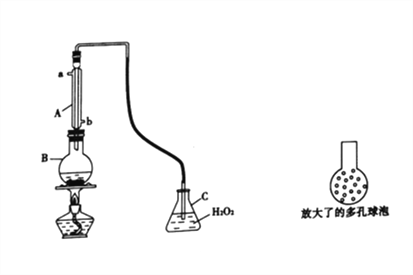
(1)儀器A的名稱是________;使用該裝置主要目的是____________________。
(2)B中加入 300.00 mL葡萄酒和適量鹽酸,加熱使SO2全部逸出并與C中H2O2完全反應,C中化學方程式為_________________________________________。
(3)將輸入C裝置中的導管頂端改成具有多孔的球泡(如圖15所示)。可提高實驗的準確度,理由是_______________________________________。
(4)除去C中的H2O 然后用0.099mol·L-1NaOH標準溶液滴定。
①用堿式滴定管量取0.09mol·L-1NaOH標準溶液前的一步操作是___________________________;
②用該方法測定葡萄酒中SO2的含量偏高,主要原因是__________________________________,利用現有的裝置,提出改進的措施是_______________________________________________。
(5)利用C中的溶液,有很多實驗方案測定葡萄酒中SO2的含量。現有0.1mol·L-1BaCl2溶液,實驗器材不限,簡述實驗步驟:________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】利用某分子篩作催化劑,NH3可脫除廢氣中的NO和NO2,生成兩種無毒物質,其反應歷程如下圖所示,下列說法正確的是( )
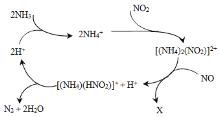
A.X是N2
B.汽車尾氣中含有的氮氧化合物是由于汽油燃燒產生的
C.NH4+中含有非極性共價鍵
D.上述歷程的總反應為:2NH3+NO +NO2 2N2+3H2O
2N2+3H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】用如圖所示裝置探究Cl2和NO2在NaOH溶液中的反應,若通入適當比例的Cl2和NO2,即發生反應Cl2+2NO2+4NaOH=2NaNO3+2NaCl+2H2O。
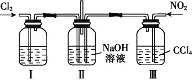
下列敘述正確的是
A. 實驗室中用二氧化錳與3 mol·L-1的鹽酸共熱制備氯氣
B. 裝置Ⅰ中盛放的試劑是濃硫酸,作用是干燥氯氣
C. 裝置Ⅲ的作用是便于控制通入NO2的量
D. 若制備的NO2中含有NO,應將混合氣體通入水中以除去NO
查看答案和解析>>
科目: 來源: 題型:
【題目】艾司洛爾(I )是預防和治療手術期心動過速的一種藥物,某合成路線如下:
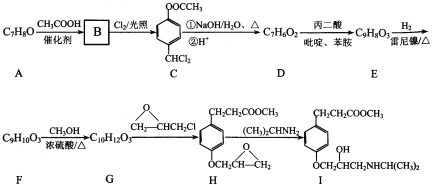
回答下列問題:
(1)A的結構簡式為_____________________,D 的化學名稱為__________________。
(2)G→H的反應類型為_______________,H中所含官能團的名稱為______________。
(3)C→D中步驟①的化學反應方程式為_________________。
(4)已知:1 mol D 和1 mol 丙二酸在吡啶、苯胺中反應生成 1 mol E、1 mol H2O和1 molCO2,且E 能與溴水發生加成反應,則 E 的結構簡式為 ____________。
(5)X是F的同分異構體,寫出滿足下列條件的 X 的結構簡式________。①與碳酸氫鈉溶液反應生成二氧化碳②與FeC13溶液發生顯色反應③核磁共振氫譜有四組峰且峰面積之比為 6 : 2 : 1 : 1
(6)參照上述合成路線,設計以![]() 和
和![]() 為主要原料制備
為主要原料制備![]() 的合成路線______。
的合成路線______。
查看答案和解析>>
科目: 來源: 題型:
【題目】在標準狀況下,在三個干燥的燒瓶內分別裝有純凈的NH3,含一半空氣的HCl氣體, NO2 和O2的混合氣體[V(NO2)∶V(O2) = 4∶1 ],然后分別作噴泉實驗,三個燒瓶內所得溶液的物質的量濃度之比為
A. 2∶1∶2 B. 5∶5∶4 C. 1∶1∶1 D. 無法確定
查看答案和解析>>
科目: 來源: 題型:
【題目】下列反應中,不屬于四種基本反應類型,但屬于氧化還原反應的是( )
A.2Na+2H2O═2NaOH+H2↑B.CaCO3+2HCl═CaCl2+H2O+CO2↑
C.2KClO3![]() 2KCl+3O2↑D.CH4+2O2
2KCl+3O2↑D.CH4+2O2![]() CO2+2H2O
CO2+2H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】NO2 是大氣的主要污染物之一,某研究小組設計如圖所示的裝置對NO2 進行回收利用,裝置中a、b均為多孔石墨電極。下列說法正確的是

A. a 為電池的負極,發生還原反應
B. 電子流向:a 電極→用電器→b 電極→溶液→a 電極
C. 一段時間后,b 極附近HNO3濃度增大
D. 電池總反應為4NO2 +O2 +2H2O= 4HNO3
查看答案和解析>>
科目: 來源: 題型:
【題目】以煤為原料可合成一系列燃料。
(1)已知:①2H2(g)+O2(g)= 2H2O(g)△H=-483.6kJ/mol
②CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ/mol
請寫出甲醇燃燒生成H2O(g)的熱化學方程式_________;
(2)向1L密閉容器中加入2mol CO、4mol H2,在適當的催化劑作用下,發生反應:2CO(g)+4H2(g)![]() CH3OCH3(l)+H2O(l)△H=+71kJ/mol
CH3OCH3(l)+H2O(l)△H=+71kJ/mol
①該反應能否_________自發進行(填“能”、“不能”或“無法判斷”)
②下列敘述能說明此反應達到平衡狀態的是_________.
a.混合氣體的平均相對分子質量保持不變
b.CO和H2的轉化率相等
c.CO和H2的體積分數保持不變
d.混合氣體的密度保持不變
e.1mol CO生成的同時有1mol O-H鍵斷裂
(3)CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H<0在一定條件下,某反應過程中部分數據如下表:
CH3OH(g)+H2O(g)△H<0在一定條件下,某反應過程中部分數據如下表:
反應條件 | 反應時間 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) |
恒溫 恒容 (T1℃、 2L) | 0min | 2 | 6 | 0 | 0 |
10min | 4.5 | ||||
20min | 1 | ||||
30min | 1 |
①0~10min內,用H2O(g)表示的化學反應速率v(H20)=_________mol/(L·min)
②達到平衡時,該反應的平衡常數K=_________(用分數表示),平衡時H2的轉化率是_________。
③在其它條件不變的情況下,若30min時改變溫度為T
(4)用甲醚(CH3OCH3)作為燃料電池的原料,請寫出在堿性介質中電池負極反應式_________.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com