
科目: 來源: 題型:
【題目】某同學在實驗室中進行如下實驗:
編號 | Ⅰ | Ⅱ | Ⅲ |
實驗 |
|
|
|
現象 | 沒有明顯變化,溶液仍為無色 | 有沉淀生成,溶液為藍綠色 | 有無色氣泡產生 |
以下結論不正確的是( )
A.Ⅰ中無明顯變化,說明兩溶液不反應
B.Ⅱ中的白色沉淀為BaSO4
C.Ⅲ中發生的反應是離子反應
D.Ⅲ中發生反應的離子方程式為2H++Zn=Zn2++H2↑
查看答案和解析>>
科目: 來源: 題型:
【題目】下列說法錯誤的是( )
A.基態Cr原子有6個未成對電子
B.PH3和NH3分子中均含有孤電子對,且PH3提供孤電子對的能力強于NH3
C.BeO的晶格能大于MgO,可推測BeCO3的分解溫度低于MgCO3
D.向1mol配合物![]() 中加入足量AgNO3溶液,可以得到3molAgCl沉淀
中加入足量AgNO3溶液,可以得到3molAgCl沉淀
查看答案和解析>>
科目: 來源: 題型:
【題目】某硝酸廠處理尾氣中NO的方法是在催化劑存在下,用H2將NO還原為N2,其熱化學方程式為NO(g)+H2(g)=![]() N2(g)+H2O(g) ΔH=mkJ·mol-1,其能量變化過程如圖:
N2(g)+H2O(g) ΔH=mkJ·mol-1,其能量變化過程如圖:
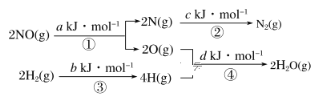
下列說法正確的是( )
A.過程①、②、③、④都是放熱過程B.m=+![]() (a+b-c-d)kJ·mol-1
(a+b-c-d)kJ·mol-1
C.m=-![]() (c+a-d-b)kJ·mol-1D.m=+
(c+a-d-b)kJ·mol-1D.m=+![]() (c+d-a-b) kJ·mol-1
(c+d-a-b) kJ·mol-1
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖是某同學設計的放熱反應的觀察裝置,

其實驗操作步驟如下:
①按圖所示將實驗裝置連接好;
②在U形管內加入少量紅墨水(或品紅溶液),打開T形管活塞,使U形管內兩邊的液面處于同一水平面,再關閉T形管活塞;
③在盛有1.0g氧化鈣的小試管里滴入2 mL左右的蒸餾水,觀察現象。
試回答:
(1)實驗前必須進行的一步實驗操作是_______________。
(2)實驗中觀察到的現象是______________________________________________________________。
(3)實驗中發生的化學反應方程式:____________________________。
(4)說明CaO、H2O的能量與Ca(OH)2的能量之間的關系:_______________________________________。
(5)若該實驗中CaO換成NaCl,實驗還能否觀察到相同現象?____(填“能”或“否”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】隨著現代工業的快速發展,SO2煙氣的排放量急劇增加。將SO2還原為硫磺是目前煙氣脫硫研究的熱點。根據SO2的反應狀態,將SO2還原法分為氣相還原法和液相還原法。
Ⅰ.氣相還原法—固體還原劑直接還原法
固體還原劑直接還原法是指在一定溫度下(200℃~300℃)將SO2煙氣通過固體還原劑,使SO2中的氧原子轉移到固體還原劑上,從而實現SO2的還原,其流程如下:
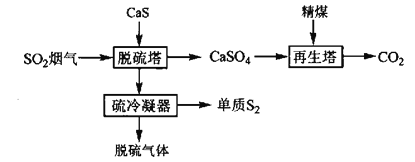
(1)再生塔中生成的物質______(填化學式)可在流程中循環使用。
(2)脫硫塔中發生反應的化學方程式為________。脫硫過程中,當產生48g單質S2時,轉移電子的物質的量為______mol。
Ⅱ.液相還原法—液相催化歧化制硫法
V.M Petrusevski等人用![]() 作為催化劑,在常溫下,將NaHSO3進行液相催化回收硫磺的工藝如下:
作為催化劑,在常溫下,將NaHSO3進行液相催化回收硫磺的工藝如下:
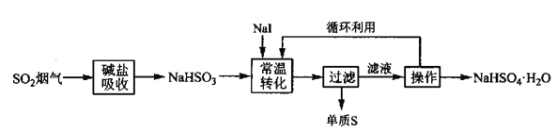
(3)下列儀器中,“操作”時不需要用到的是______(填標號)。
a.![]() b.
b.![]() c.
c.![]() d.
d.![]()
(4)![]() 催化NaHSO3的反應過程為①_________(用離子方程式表示);②
催化NaHSO3的反應過程為①_________(用離子方程式表示);②![]() 。
。
(5)液相催化歧化制硫法具有反應條件溫和、運行費用低等優點,然而其缺點是硫磺的回收率不會高于______%(保留1位小數)。
(6)若采用Na2S溶液作為堿鹽吸收液,隨著吸收液pH的變化,會生成二次污染物______(填化學式)。
查看答案和解析>>
科目: 來源: 題型:
【題目】某化學興趣小組為了探究鋁電極在電池中的作用,設計并進行了以下一系列實驗,實驗結果記錄如下表:
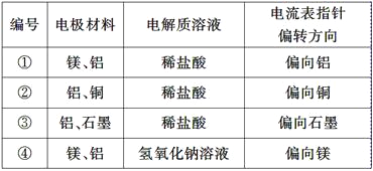
試根據表中的實驗現象完成下列問題:
(1)實驗①、②中鋁所作的電極(指正極或負極)________(填“相同”或“不相同”)。
(2)實驗③中鋁為________極,電極反應式為_________________________________________;石墨為________極,電極反應式為______________;電池總反應式為____________________。
(3)實驗④中鋁作負極還是正極?____________,理由是_________________________,鋁電極的電極反應式為__________________________________________________________。
(4)根據實驗結果總結出影響鋁在原電池中作正極或負極的因素為______________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】恒溫下,將a mol N2與b mol H2的混合氣體通入一定容積的密閉容器中,發生如下反應:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(1)若反應進行到某時刻t時,n(N2)=13mol,n(NH3)=6mol,
計算a=_______。
(2)反應達到平衡時,混合氣體的體積為716.8L(標準狀況下),其中NH3的百分含量(體積分數)為25%。計算:平衡時NH3的物質的量為_____________。
(3)原混合氣體與平衡混合氣體的總物質的量之比
n(始): n(平)=____________。
(4)原混合氣體中a : b=_______________。
(5)達到平衡時,N2和H2的轉化率![]() (N2):
(N2):![]() (H2)=______________。
(H2)=______________。
(6)平衡混合氣體中n(N2): n(H2): n(NH3)=______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】納米Fe3O4在磁流體、催化劑、醫學等領域具有廣闊的應用前景。氧化共沉淀制備納米Fe3O4的方法如下:
I.Fe2+的氧化:將FeSO4溶液用NaOH溶液調節pH至a,再加入H2O2溶液,立即得到 FeO( OH)紅棕色懸濁液。
(1)①若用NaOH溶液調節pH過高會產生灰白色沉淀,該反應的離子方程式是 _____________。
②上述反應完成后,測得a值與FeO(OH)產率及其生成后溶液pH的關系,結果如下:
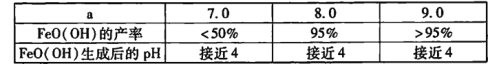
用離子方程式解釋FeO( OH)生成后溶液pH下降的原因:____。
(2)經檢驗:當a=7時,產物中存在大量Fe2O3。對Fe2 O3的產生提出兩種假設:
i.反應過程中溶液酸性增強,導致FeO( OH)向Fe2 O3的轉化;
ii.溶液中存在少量Fe2+,導致FeO( OH)向Fe2O3的轉化。
①經分析,假設i不成立的實驗依據是____。
②其他條件相同時,向FeO( OH)濁液中加入不同濃度Fe2+,30 min后測定物質的組成,結果如下:
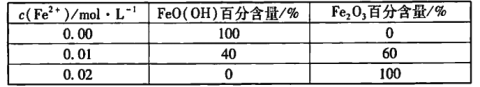
以上結果表明:____。
③ a=7和a =9時,FeO( OH)產率差異很大的原因是____。
Ⅱ.Fe2+和Fe3+共沉淀:向FeO( OH)紅棕色懸濁液中同時加入FeSO4溶液和NaOH濃溶液進行共沉淀,再將此混合液加熱回流、冷卻、過濾、洗滌、干燥,得到納米Fe3O4。
(3)共沉淀時的反應條件對產物純度和產率的影響極大。
①共沉淀pH過高時,會導致FeSO4溶液被快速氧化;共沉淀pH過低時,得到的納米Fe3O4中會混有的物質是____。
②已知N=n[FeO(OH)]/n(Fe2+),其他條件一定時,測得納米Fe3O4的產率隨N的變化曲線如下圖所示:

經理論分析,N=2共沉淀時納米Fe3O4產率應最高,事實并非如此的可能原因是_________。
查看答案和解析>>
科目: 來源: 題型:
【題目】將一定量的二氧化硫和含0.7 mol氧氣的空氣(忽略CO2)放入一定體積的密閉容器中,550℃時,在催化劑作用下發生反應2SO2+O2![]() 2SO3。反應達到平衡后,將容器中的混合氣體通過過量氫氧化鈉溶液,氣體體積減小了21.28 L;再將剩余氣體通過一種堿性溶液吸收氧氣,氣體的體積又減少了5.6 L(以上氣體體積均為標準狀況下的體積)。(計算結果保留一位小數)請回答下列問題:
2SO3。反應達到平衡后,將容器中的混合氣體通過過量氫氧化鈉溶液,氣體體積減小了21.28 L;再將剩余氣體通過一種堿性溶液吸收氧氣,氣體的體積又減少了5.6 L(以上氣體體積均為標準狀況下的體積)。(計算結果保留一位小數)請回答下列問題:
(1)判斷該反應達到平衡狀態的標志是(填字母)__________________。
a.二氧化硫和三氧化硫濃度相等
b.三氧化硫百分含量保持不變
c.容器中氣體的壓強不變
d.三氧化硫的生成速率與二氧化硫的消耗速率相等
e.容器中混合氣體的密度保持不變
(2)求該反應達到平衡時,消耗二氧化硫的物質的量占原二氧化硫的物質的量的百分比____。
(3)若將平衡混合氣體的5%通入過量的氯化鋇溶液中,生成沉淀的質量是多少?______
查看答案和解析>>
科目: 來源: 題型:
【題目】碳、硫的含量影響鋼鐵性能.碳、硫含量的一種測定方法是將鋼樣中碳、硫轉化為氣體,再用測碳、測硫裝置進行測定.
(1)采用如圖裝置A,在高溫下將x克鋼樣中碳、硫轉化為CO2、SO2.
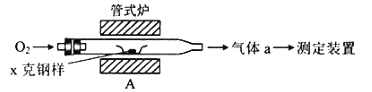
①氣體a的成分是_____.
②若鋼樣中硫以FeS形式存在,A中反應:3FeS+5O2![]() 1_____+3_____.
1_____+3_____.
(2)將氣體a通入測硫酸裝置中(如圖),采用滴定法測定硫的含量.
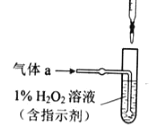
①H2O2氧化SO2的化學方程式:_____
②用NaOH溶液滴定生成的H2SO4,消耗z mL NaOH溶液.若消耗1mL NaOH溶液相當于硫的質量為y克,則該鋼樣中硫的質量分數:_____.
(3)將氣體a通入測碳裝置中(如圖),采用重量法測定碳的含量.
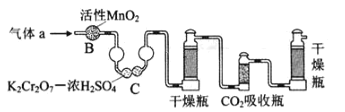
①氣體a通過B和C的目的是_____
②計算鋼樣中碳的質量分數,應測量的數據是_____.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com