
科目: 來源: 題型:
【題目】2019年3月21日是第二十七屆“世界水日”,保護水資源,合理利用廢水節(jié)省水資源,加強廢水的回收利用已被越來越多的人所關注。已知:某無色廢水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的幾種,為分析其成分,分別取廢水樣品100![]() ,進行了三組實驗,其操作和有關圖像如下圖所示,請回答下列問題:
,進行了三組實驗,其操作和有關圖像如下圖所示,請回答下列問題:

(1)根據(jù)上述3組實驗可以分析廢水中一定不存在的陰離子是_______,一定存在的陽離子是_____。
(2)分析圖像,在原溶液中c(NH4+)與c(Al3+)的比值為_______
(3) 若通過實驗確定原廢水中c(Na+)=0.14mol/L,試判斷原廢水中NO3-是否存在?_____(填“存在”“不存在”或“不確定”)。若存在,c(NO3-)=______mol/L。(若不存在或不確定則此空不填)。
查看答案和解析>>
科目: 來源: 題型:
【題目】在化學分析中,常常需要用KMnO4標準溶液,由于KMnO4晶體在室溫下不太穩(wěn)定,因而很難直接配制準確物質的量濃度的KMnO4溶液。用Na2C2O4固體測定KMnO4溶液濃度的實驗步驟如下:(反應原理為:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O)
步驟一:先粗配濃度約為0.15mol/L的KMnO4溶液500mL。
步驟二:準確稱取Na2C2O4固體mg放入錐形瓶中,用蒸餾水溶解并加稀硫酸酸化,加熱至70~80℃,用步驟一所配KMnO4溶液進行滴定。記錄相關數(shù)據(jù)。
步驟三:重復步驟二兩到三次。計算得KMnO4溶液的物質的量濃度。
試回答下列問題:
(1)盛放KMnO4溶液的滴定管為___(填“酸式”或“堿式”)滴定管。
(2)該滴定實驗滴定終點的現(xiàn)象是___。
(3)步驟二中滴定操作如圖所示,正確的操作是___(填編號)。
A. B.
B. C.
C.
(4)若m的數(shù)值為1.340g,滴定的KMnO4溶液平均用量為25.00mL,則KMnO4溶液的濃度為___mol/L。
(5)若滴定完畢后讀數(shù)時俯視,則實驗誤差會__(填“偏高”、“偏低”或“無影響”)。
查看答案和解析>>
科目: 來源: 題型:
【題目】某同學通過以下裝置測定M樣品(只含Fe、Al、Cu)中各成分的質量分數(shù)。取兩份質量均為m g的M樣品,按實驗1(如圖1)和實驗2(如圖2)進行實驗,該同學順利完成了實驗并測得氣體體積分別為V1 mL和V2 mL(已折算到標準狀況下)。
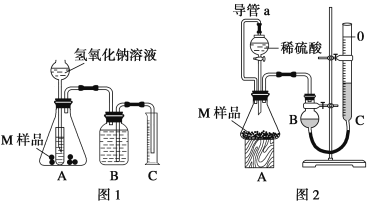
(1)寫出實驗1中可能發(fā)生反應的離子方程式:____________。
(2)該實驗需要0.50 mol·L-1的NaOH溶液480 mL,請回答下列問題:
①配制時應用托盤天平稱量______g NaOH,應選擇________ ml容量瓶。
②配制NaOH溶液時,NaOH固體中含有Na2O雜質會導致所配溶液濃度________。(填“偏大”、“偏小”或“無影響”)。
(3)該實驗中所用稀硫酸是用98%的濃硫酸(ρ=1.84g/cm3)配制的,則該濃硫酸的物質的量濃度是_______。
(4)對于實驗2,讀數(shù)時冷卻至室溫除視線平視外,還應進行的操作是: ___________。
(5)實驗2中導管a的作用_________。
(6)M樣品中銅的質量的數(shù)學表達式為(用V1和V2 表示):_______。
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖為相互串聯(lián)的甲乙兩個電解池,請回答:
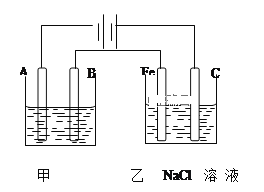
(1)甲池若為用電解原理精煉銅的裝置,A極是__極,材料是___,B極電極反應方程式為___。
(2)乙池中若滴入少量酚酞試液,開始一段時間后,___極(填“Fe”或“C”)附近變紅色。
(3)若乙槽陽極放出氣體在標準狀況下的體積為2.24L,
①甲槽陰極增重___g。
②若乙槽電解后得到堿液的物質的量濃度為2moL/L,則乙槽剩余液體體積為__mL。
查看答案和解析>>
科目: 來源: 題型:
【題目】金屬銅、鐵、鋁等在人類文明史上先后被廣泛使用。回答下列問題:
(1)銅、銀、金三種金屬在元素周期表同族且依次相鄰,因此價電子層結構相似。銀原子價層電子排布式為________;金元素在周期表的位置是________。
(2)觀察如下循環(huán)圖可以獲知FeO的晶格能為________ kJ·mol-1。

(3)氯化鋁熔點194℃,會升華,熔融態(tài)不易導電。實驗測得氣態(tài)氯化鋁分子組成式為Al2Cl6,其結構式為________;氣態(tài)氯化鋁中存在________(填選項標號)
A.離子鍵 B.配位鍵 C.氫鍵 D.范德華力 E.金屬鍵 F.非極性共價鍵
(4)石墨微觀結構如下圖。其中碳原子雜化類型為________。金剛石晶體中碳碳鍵鍵長為0.155nm。金剛石的熔點略低于石墨,而遠高于C60的原因是________。
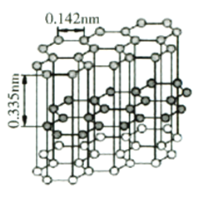
(5)設阿伏加德羅常數(shù)值為NA,則石墨的密度為________![]() (列出計算表達式)
(列出計算表達式)
查看答案和解析>>
科目: 來源: 題型:
【題目】依據(jù)電化學知識,解決下列問題:
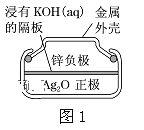
(1)圖1為鋅銀電池,負極是Zn,正極是Ag2O,電解質是KOH。寫出該電池負極電極反應式:___,電池工作時,正極區(qū)周圍溶液的pH___(填“增大”、“減小”、“不變”)。
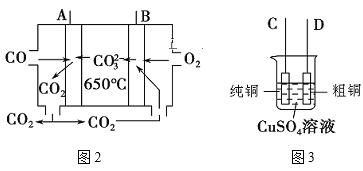
(2)圖2是一種新型燃料電池,以CO為燃料,一定比例的Li2CO3和Na2CO3的熔融混合物為電解質,圖3是粗銅精煉的裝置圖,現(xiàn)用該燃料電池為電源進行粗銅的精煉實驗。
①寫出A極的電極反應式:___。
②要用燃料電池為電源進行粗銅的精煉實驗,則B極應該與__極(填“C”或“D”)相連。
③當消耗標準狀況下2.24LO2時,C電極的質量變化為___。
查看答案和解析>>
科目: 來源: 題型:
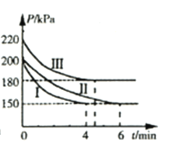
【題目】工業(yè)上用CO2和NH3合成尿素 [CO(NH2)2]。某研發(fā)小組為合成尿素進行如下實驗:向5L恒容密閉容器中通入0.2molNH3和0.1molCO2,分別進行Ⅰ、Ⅱ、Ⅲ三組實驗。在不同條件下發(fā)生反應:![]() ,反應體系總壓強隨時間的變化曲線如圖所示。
,反應體系總壓強隨時間的變化曲線如圖所示。
(1)已知:
①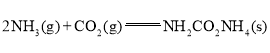
![]()
②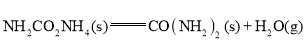
![]()
用CO2和NH3合成尿素的熱化學方程式為________。
(2)Ⅰ、Ⅱ、Ⅲ三組實驗中,反應溫度最高的是________。(填“Ⅰ”、“Ⅱ”或“Ⅲ”)
(3)Ⅰ、Ⅲ兩組實驗中,NH3轉化率較高的是________。(填“Ⅰ”或“Ⅲ”)
(4)若要增加實驗Ⅱ的反應速率并提高NH3轉化率,改變下列條件可以實現(xiàn)的是________(填標號)
A.增加CO2的物質的量 B.加入惰性氣體使壓強增大
C.升高反應的溫度 D.改用2L的容器進行實驗
(5)Ⅰ、Ⅱ兩組實驗中,反應達到平衡的時間不同,可能的原因是________。
(6)第Ⅱ組實驗開始6min內NH3的平均反應速率為________![]() ,平衡常數(shù)
,平衡常數(shù)![]() ________。
________。
查看答案和解析>>
科目: 來源: 題型:
【題目】按要求回答以下問題:
(1)寫出![]() 溶液與稀硫酸反應的離子方程式___________,等物質的量的
溶液與稀硫酸反應的離子方程式___________,等物質的量的![]() 與
與![]() 固體分別與足量的硫酸反應,消耗硫酸的物質的量之比為________。
固體分別與足量的硫酸反應,消耗硫酸的物質的量之比為________。
(2)在![]() 稀
稀![]() 反應中,________是氧化劑;________是還原劑;氧化劑與還原劑的物質的量之比為__________
反應中,________是氧化劑;________是還原劑;氧化劑與還原劑的物質的量之比為__________
(3)向酸性高錳酸鉀溶液中滴加硫酸亞鐵,紫色逐漸褪去,寫出該反應的離子方程式: _______。
(4)將![]() 的鈉、鎂、鋁分別投入
的鈉、鎂、鋁分別投入![]() 的硫酸溶液中,三者產生氫氣的體積比是________。
的硫酸溶液中,三者產生氫氣的體積比是________。
(5)等質量的Fe分別與足量的![]() 、S、
、S、![]() 反應轉移電子數(shù)之比為_______;
反應轉移電子數(shù)之比為_______;
查看答案和解析>>
科目: 來源: 題型:
【題目】常溫下,向20mL0.10molL-1醋酸溶液中滴加0.10molL-1NaOH溶液,滴加過程中測得pH與NaOH溶液體積(V)的關系如圖所示。下列說法正確的是( )
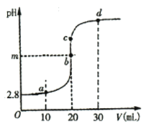
A.m=7
B.由水電離出的c(H+):a>b>c>d
C.由圖可知,醋酸Ka的數(shù)量級為10-6
D.b與d之間的任意一點c都有:![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】X、Y、Z、W為原子序數(shù)依次增大的短周期主族元素,Y與W的最高化合價之和為8,X與Z同主族,且Z的核電荷數(shù)是X的2倍。下列說法正確的是( )
A.簡單氣態(tài)氫化物的穩(wěn)定性:X>ZB.簡單離子半徑:![]()
C.由X、Y組成的化合物中不含共價鍵D.最高價氧化物對應水化物的酸性:Z>W
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com