
科目: 來源: 題型:
【題目】將一定體積的CO2通入NaOH溶液中,向所得的溶液A中逐滴加入1 mol·L-1的稀鹽酸,所加鹽酸的體積與產生CO2的體積關系如圖所示:
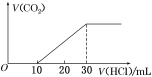
溶液A中的溶質是( )。
A.Na2CO3和NaHCO3B.NaOH和Na2CO3C.Na2CO3D.NaHCO3
查看答案和解析>>
科目: 來源: 題型:
【題目】科學工作者結合實驗與計算機模擬結果,研究了在Pt/SiO2催化劑表面上CO2與H2的反應歷程,前三步歷程如圖所示,其中吸附在Pt/SiO2催化劑表面上的物種用“· ”標注,Ts表示過渡態。
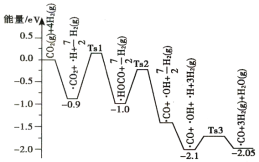
下列有關敘述正確的是
A.前三步總反應的△H<0
B.·HOCO轉化為·CO和·OH為吸熱過程
C.催化劑通過參與化學反應,能降低反應的活化能,提高反應物的轉化率
D.歷程中活化能(能壘)最小的反應方程式為![]()
查看答案和解析>>
科目: 來源: 題型:
【題目】25℃時,H3AsO4水溶液中含砷的各物種的分布分數(平衡時某物種的濃度占各物種濃度之和的分數)與pH的關系分別如圖所示。
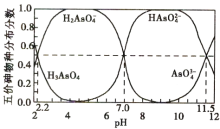
下列敘述錯誤的是
A.將NaOH溶液逐滴加入到H3AsO4溶液中,當溶液pH在5~6時發生反應的離子方程式為![]()
B.Na2HAsO4溶液中離子濃度關系c(Na+)>c(HAsO![]() )>c(OH-)>c(H2AsO
)>c(OH-)>c(H2AsO![]() )>c(AsO
)>c(AsO![]() )
)
C.向H3AsO4溶液滴加NaOH溶液至中性時c(Na+)=2c(HAsO![]() )+3c(AsO
)+3c(AsO![]() )
)
D.AsO43-第一步水解的平衡常數的數量級為10-3
查看答案和解析>>
科目: 來源: 題型:
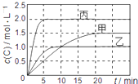
【題目】向甲、乙、丙三個密閉容器中充入一定量的A和B,發生反應:xA(g)+B(g)![]() 2C(g)。各容器的反應溫度、反應物起始量,反應過程中C的濃度隨時間變化關系分別用下表和如圖表示:下列說法正確的是( )
2C(g)。各容器的反應溫度、反應物起始量,反應過程中C的濃度隨時間變化關系分別用下表和如圖表示:下列說法正確的是( )
容器 | 甲 | 乙 | 丙 |
容積 | 0.5L | 0.5L | 1.0L |
溫度 | T1 | T2 | T2 |
反應物起始量 | 0.5molA 1.5molB | 0.5molA 1.5molB | 2.0molA 6.0molB |
A.由圖可知:T1<T2,且該反應為吸熱反應
B.T2時該反應的平衡常數K=0.8
C.物質A的化學計量數x=2
D.保持甲容器體積不變,向其中通入He氣體,達到新平衡后,C的百分含量減小
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖所示為氣相直接水合法C2H4(g)+H2O(g)![]() C2H5OH(g)中乙烯的平衡轉化率與溫度、壓強的關系[其中n(H2O)∶n(C2H4)=1∶1]。
C2H5OH(g)中乙烯的平衡轉化率與溫度、壓強的關系[其中n(H2O)∶n(C2H4)=1∶1]。
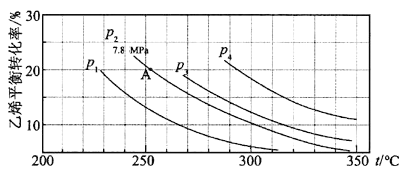
計算乙烯水合制乙醇反應在圖中A點的平衡常數Kp為 (用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
A.0.082B.0.072C.0.072MPa-1D.0.082 MPa-1
查看答案和解析>>
科目: 來源: 題型:
【題目】關于Na2CO3與NaHCO3的性質判斷正確的是( )
A.常溫下溶解度:Na2CO3<NaHCO3
B.熱穩定性:Na2CO3<NaHCO3
C.與同濃度同體積的鹽酸反應的速率:Na2CO3>NaHCO3
D.與澄清石灰水反應,均有白色沉淀生成
查看答案和解析>>
科目: 來源: 題型:
【題目】一定條件下,通過下列反應可以制備特種陶瓷的原料MgO, MgSO3(s) + CO(g)![]() MgO(s) + CO2(g) +SO2(g) △H>0。該反應在恒容的密閉容器中達到平衡后,若僅改變圖中橫坐標x的值,重新達到平衡后,縱坐標y隨x變化趨勢合理的是
MgO(s) + CO2(g) +SO2(g) △H>0。該反應在恒容的密閉容器中達到平衡后,若僅改變圖中橫坐標x的值,重新達到平衡后,縱坐標y隨x變化趨勢合理的是

選項 | x | y |
A | 溫度 | 容器內混合氣體的密度 |
B | CO的物質的量 | CO2與CO的物質的量之比 |
C | SO2的濃度 | 平衡常數K |
D | MgSO4的質量(忽略體積) | CO的轉化率 |
查看答案和解析>>
科目: 來源: 題型:
【題目】在海水綜合利用中,下列敘述不正確的是( )
A.海水經過蒸發結晶得到粗鹽
B.海水中提取鎂單質的方法是海水![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
C.海水提鎂的工藝中用貝殼為原料生產石灰乳
D.海水中提取溴單質可以用氯氣將海水中的Br-氧化
查看答案和解析>>
科目: 來源: 題型:
【題目】重鉻酸鉀是工業合成的常用氧化劑和催化劑,如圖所示的微生物電池,能利用K2Cr2O7實現對含苯酚(或醛類)廢水的有效處理,該電池工作一段時間后,中間室內的NaC1溶液濃度減小,則下列敘述正確的是

A.a電極為負極,電子從a電極經過中間室到達b電極
B.M為陽離子交換膜,電解過程中中間室內的n(NaC1)減小
C.處理含苯甲醛廢水時a電極反應式為:C6H5CHO-32e-+13H2O=7CO2+32H+
D.當b電極消耗等物質的量的K2Cr2O7時,a電極消耗的C6H5OH或C6H5CHO的物質的量之比為8:7
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com