
科目: 來源: 題型:
【題目】鋼鐵是用途最廣泛的金屬材料。
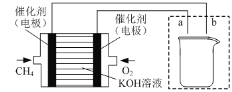
(1)將鐵粉和活性炭的混合物用NaCl溶液濕潤后,置于如圖所示裝置中,進行鐵的電化學腐蝕實驗。寫出正極反應式:______。

(2)純鐵作電極插入濃的NaOH溶液電解可制得Na2FeO4,裝置如圖所示。陽極的電極反應式為______;若消耗11.2g鐵,則通過離子交換膜的Na+物質的量為______。

(3)如圖所示裝置為利用甲烷燃料電池實現在鐵質材料上鍍鋅的一部分,燃料電池的負極反應式為______;在如圖所示虛線框內補充完整在鐵質材料上鍍鋅的裝置圖(注明電極材料和電解質溶液的成分)。_____
查看答案和解析>>
科目: 來源: 題型:
【題目】根據下列圖示所得出的結論正確的是( )

A. 圖甲表示1 mL pH=2某一元酸溶液加水稀釋時,pH隨溶液總體積的變化曲線,說明該酸是強酸
B. 圖乙表示恒容密閉容器中其他條件相同時改變溫度,反應CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)中n(CH3OH)隨時間的變化曲線,說明反應平衡常數KⅠ>KⅡ
CH3OH(g)+H2O(g)中n(CH3OH)隨時間的變化曲線,說明反應平衡常數KⅠ>KⅡ
C. 圖丙表示不同溫度下水溶液中-lg c(H+)、-lg c(OH-)變化曲線,說明T1>T2
D. 圖丁表示1 mol H2和0.5 mol O2反應生成1 mol H2O過程中的能量變化曲線,說明H2的燃燒熱是241.8 kJ·mol-1
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖是電解水制高純氫的示意圖,通過控制開關連接K1或K2,可交替得到H2和O2。下列說法正確的是
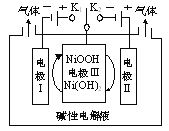
A.制H2時,連接K2
B.連接K1時,電極Ⅰ附近堿性減弱
C.制O2時,電極Ⅲ的反應為:NiOOH+e+H2O=Ni(OH)2+OH-
D.通過控制開關連接K1和K2,可使電極Ⅲ循環使用
查看答案和解析>>
科目: 來源: 題型:
【題目】多相催化反應是在催化劑表面通過吸附、解吸過程進行的。我國學者發現T℃時(各物質均為氣態),甲醇與水在銅基催化劑上的反應機理和能量圖如圖:
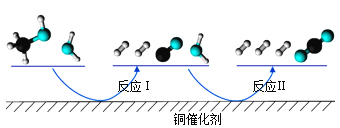

下列說法正確的是( )
A.反應Ⅱ的熱化學方程式為:CO(g)+H2O(g)=H2(g)+CO2(g) △H=+akJ/mol(a>0)
B.1molCH3OH(g)和1molH2O(g)的總能量大于1molCO2(g)和3molH2(g)的總能量
C.選擇優良的催化劑降低反應Ⅰ和Ⅱ的活化能,有利于減少過程中的能耗
D.CO(g)在反應中生成又消耗,CO(g)可認為是催化劑
查看答案和解析>>
科目: 來源: 題型:
【題目】下列圖示與對應的敘述相符的是
A.如圖表示反應2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0在有無催化劑時的能量變化
2SO3(g) ΔH<0在有無催化劑時的能量變化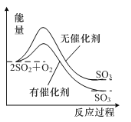
B.如圖表示電解精煉銅時純銅和粗銅的質量隨時間的變化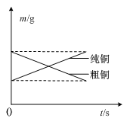
C.如圖表示鉛蓄電池放電時負極質量隨轉移電子物質的量的變化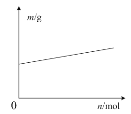
D.如圖表示反應2NO2(g)![]() N2O4(g)和2NO2(g)
N2O4(g)和2NO2(g)![]() N2O4(l)的能量變化
N2O4(l)的能量變化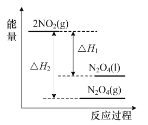
查看答案和解析>>
科目: 來源: 題型:
【題目】一種天然化合物X的結構簡式如圖所示。下列有關該化合物的說法中正確的是

A.化合物X分子中所有原子可能在同一平面上
B.化合物X能使酸性高錳酸鉀溶液褪色
C.化合物X存在順反異構和手性異構
D.X能與NaHCO3溶液反應生成CO2
查看答案和解析>>
科目: 來源: 題型:
【題目】某微生物脫鹽池的裝置如圖所示,下列說法正確的是
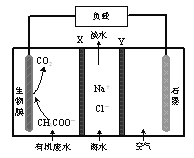
A.電子由石墨電極流出
B.生物膜電極反應式為:CH3COO-+2H2O+8e-=2CO2↑+7H+
C.X、Y依次為陰離子、陽離子選擇性交換膜
D.該裝置可以將電能轉化為化學能
查看答案和解析>>
科目: 來源: 題型:
【題目】某實驗小組對中學課本中可生成氫氣的反應進行了研究,總結出三個可以生成H2的反應:①Zn+鹽酸 ②Na+水 請回答下列問題:

(1)寫出①、②反應的離子方程式
①__________________________________________;
②________________________________________________________
(2)在點燃H2之前必須先進行_______________________________________。
(3)實驗小組在點燃用上述裝置制得的H2時,①實驗獲得成功,②卻失敗了。他們分析認為失敗的原因是Na與H2O的反應速率太快,Na的用量太少。于是他們準備增加鈉的用量,可老師說太危險,你認為產生危險的原因___________________________________________________________________
(4)實驗小組查閱鈉、苯、水的密度分別為0.97g/mL、0.88g/mL、1.00g/mL,并據此對實驗進行了改進。在改進后的實驗中H2的生成速率會_______________。改進后的實驗現象為_________________________________________________________________________。
(5)2.3 g鈉投入20 mL水中完全反應放出的氣體在標準狀況下的體積是____________,所得溶液的物質的量濃度是______________________。(不計溶液體積的變化)
查看答案和解析>>
科目: 來源: 題型:
【題目】作為高中生,學會利用我們課堂上學到的知識來解決生活中的一些問題,是我們學習的重要目的之一.成外某化學實驗興趣小組,一行四人,利用實驗室老師提供的基本儀器和藥品,自行購置了雞蛋,食醋等生活用品,進行了如下探究.
I.甲同學老家在閬中,對兒時在家鄉品嘗到的閬中老陳醋的滋味記憶猶新,跟隨父母來到成都后,總是覺得超市買到的醋不如兒時的味道,查閱相關資料后,得知如圖1信息:
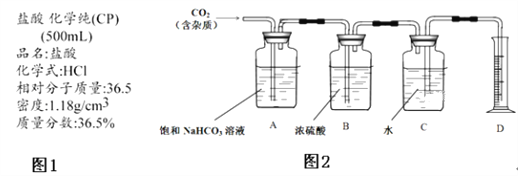
①醋分兩種,釀造醋和配制醋.正宗的老陳醋必須經長久時間釀造才得此美味,市場上多充斥著工業醋酸加水勾兌的配制醋.
②釀造醋國家標準為醋酸含量必須大于3.50g/100mL,而配制醋國家標準僅為1.50g~3.50g/100mL.
③在老師的幫助下,測定了超市購買的食醋中,醋酸的物質的量濃度為0.75mol/L.
(1)請幫助甲同學計算從超市購買的食醋中醋酸含量為_____g/100mL,屬于_____醋(填“釀造”或“配制”).(提示:醋酸摩爾質量為60g/mol)
(2)請寫出醋酸與雞蛋殼(主要成分為CaCO3)反應的離子方程式_____。
II.如圖1是成外化學實驗室濃鹽酸試劑標簽上的部分內容.乙同學現用該濃鹽酸配制100mL 1molL﹣1的稀鹽酸.可供選用的儀器有:①膠頭滴管;②燒瓶;③燒杯;④藥匙;⑤量筒;⑥托盤天平;⑦玻璃棒.請回答下列問題:
(1)配制稀鹽酸時,還缺少的儀器有_____;
(2)經計算,配制100mL1molL﹣1的稀鹽酸需要用量筒量取上述濃鹽酸的體積為_____mL(保留小數點后一位);
(3)對所配制的稀鹽酸進行測定,發現其濃度小于1molL﹣1,引起誤差的原因可能是_____。
A.定容時俯視容量瓶刻度線
B.容量瓶在使用前未干燥,里面有少量蒸餾水
C.轉移溶液后,未洗滌燒杯和玻璃棒
D.定容搖勻后發現液面低于容量瓶的刻度線,再加水至刻度線
III.丙同學對課堂上學到的膠體的相關知識產生了濃厚興趣.
(1)他利用買來的雞蛋的蛋清配制成溶液,用激光筆照射溶液,發現一條光束穿過雞蛋清溶液,此現象稱為_____。
(2)他將乙同學配制好的鹽酸溶液加入到雞蛋清溶液中,發現出現絮狀沉淀,此現象稱為_____。
IV.丁同學試圖測定CO2的相對分子質量.
①利用丙同學用完后剩下的雞蛋殼和乙同學配制好的稀鹽酸溶液制備CO2;
②查詢相關書籍后,設計了如圖2所示裝置:
(1)其他同學認為B裝置在此處沒必要,請簡述原因_____。
(2)A裝置中的飽和NaHCO3溶液可以吸收_____。
(3)實驗前測得C裝置(含水)重量為50.00g,實驗完畢后C裝置(含水)重量為40.02g,D中量筒讀數為10.0mL,已知H2密度為0.09g/L(以上數據均已折合為標況下數值),請根據以上數據,計算CO2的相對分子質量為_____(保留小數點后一位).
查看答案和解析>>
科目: 來源: 題型:
【題目】下列指定反應的離子方程式正確的是
A.向NaOH溶液中通入過量CO2:OH-+CO2=HCO![]()
B.向Na2SiO3溶液中滴加稀鹽酸:Na2SiO3+2H+=H2SiO3↓+2Na+
C.電解MgCl2溶液:2H2O+2Cl-![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D.SO2水溶液吸收Br2蒸汽:SO2+H2O+Br2=SO![]() +2H++2Br-
+2H++2Br-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com