
科目: 來源: 題型:
【題目】某工業含銅廢料含有 Cu、CuO、CuS、CuSO4 等成分,利用該含銅廢料可生產硝酸銅晶體[Cu(NO3)2·3H2O],生產的工藝流程如圖所示,請回答下列問題:

(1)“焙燒”過程中生成的廢氣中有害氣體的成分是______________。
(2)“酸化”過程為加快反應速率,可采用的措施有___________________________(寫出一條即可)。
(3)若試劑 a 可以是____________,試劑b的作用是______________________________________。
(4)“反應”一步中使用 20% HNO3 和 10% H2O2,整個過程無紅棕色氣體產生,則發生反應的離子方程式為______________________________________;若該步驟只使用 20% HNO3,隨著反應的進行,溫度升高,出現大量紅棕色氣體,則還原劑與氧化劑的物質的量之比為_______________。
(5)“系列操作”中應包含____________、______________、過濾、洗滌、干燥。
查看答案和解析>>
科目: 來源: 題型:
【題目】氫化鋁鋰(LiAlH4)以其優良的還原性能在醫藥、香料、農藥、染料等行業中廣泛應用。純氫化鋁鋰是一種白色晶狀固體,熔點 125℃,加熱至 130℃時分解,溶于醚、四氫呋喃,在 120℃以下和干燥的空氣中相對穩定,但遇水即爆炸性反應。目前世界上有四種工業生產 LiAlH4的方法,其中施萊興格(Schlesinger)法和高壓合成法最為常見。
Ⅰ. 施萊興格(Schlesinger)法
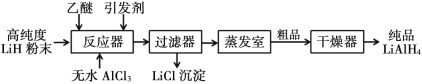
Ⅱ.高壓合成法
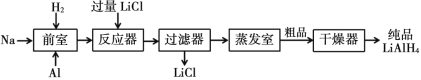
請根據題中信息回答以下問題:
(1)Schlesinger 中的反應器需要附加電磁攪拌器,目的是________。
(2)Schlesinger 的反應器中發生的化學反應方程式是________。
(3)采用 Schlesinger 時需要使用大量高純度氬氣,氬氣的作用是________。
(4)為了降低成本,在 Schlesinger 工藝中有一種原料可以循環使用,這種原料是________。
(5)已知乙醚沸點為 35℃,某工廠準備在蒸發室采用減壓蒸發分離出產品,你認為有無必要,請簡述理由________。
(6)兩種工藝均使用過濾器,中學實驗室中過濾裝置需要的玻璃儀器有________。
(7)使用氫化鋁鋰要注意安全, 少量未反應完的需要分解處理。其中一種處理方法是向其中緩慢加入適量的稀鹽酸,待無氣體放出后視為處理完全。請寫出此過程的化學反應方程式______________________________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】在相同容積的4個密閉器中進行同一種可逆反應,2A(g)+B(g)![]() 3C(g)+2D(g),起始時4個容器所盛A、B的量如表所示各容器所盛物質的量:
3C(g)+2D(g),起始時4個容器所盛A、B的量如表所示各容器所盛物質的量:
容器 | 甲 | 乙 | 丙 | 丁 |
A | 2mol | 1mol | 2mol | 1mol |
B | 1mol | 1mol | 2mol | 2mol |
在相同溫度下,建立平衡時,4個容器中A或B的轉化率的大小關系是
A.A的轉化率為:甲<丙<乙<丁B.A的轉化率為:甲<乙<丙<丁
C.B的轉化率為:甲>丙>乙>丁D.B的轉化率為:丁>乙>丙>甲
查看答案和解析>>
科目: 來源: 題型:
【題目】Na2SO3是一種白色粉末,工業上可用作還原劑、防腐劑等。某化學小組探究不同pH的Na2SO3溶液與同濃度AgNO3溶液反應的產物,進行如下實驗。
I.(1)配制500mL一定濃度的Na2SO3溶液
①溶解:準確稱取一定質量的Na2SO3晶體,用煮沸的蒸餾水溶解。蒸餾水需煮沸的原因是___。
②移液:將上述溶解后的Na2SO3溶液在燒杯中冷卻后轉入儀器A中,則儀器A為_,同時洗滌___(填儀器名稱)2~3次,將洗滌液一并轉入儀器A中;
③定容:加水至刻度線1~2cm處,改用膠頭滴管滴加蒸餾水至液面與刻度線相切,蓋好瓶塞,反復上下顛倒,搖勻。
Ⅱ.探究不同pH的Na2SO3溶液與pH=4的AgNO3溶液反應的產物
查閱資料:i.Ag2SO3為白色固體,不溶于水,溶于過量Na2SO3溶液
ii.Ag2O,棕黑色固體,不溶于水,可與濃氨水反應
(2)將pH=8的Na2SO3溶液滴人pH=4的AgNO3溶液中,至產生白色沉淀。
假設一:該白色沉淀為Ag2SO3
假設二:該白色沉淀為Ag2SO4
假設三:該白色沉淀為Ag2SO3和Ag2SO4的混合物
①寫出假設一的離子方程式__;
②提出假設二的可能依據是___;
③驗證假設三是否成立的實驗操作是__。
(3)將pH=4的AgNO3溶液逐滴滴人足量的pH=11的Na2SO3溶液中,開始產生白色沉淀A,然后變成棕黑色物質。為了研究白色固體A的成分,取棕黑色固體進行如下實驗:

①已知反應(b)的化學方程式為Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O,則反應(a)的化學方程式為___;
②生成白色沉淀A的反應為非氧化還原反應,則A的主要成分是__(寫化學式)。
(4)由上述實驗可知,鹽溶液間的反應存在多樣性。經驗證,(2)中實驗假設一成立,則(3)中實驗的產物不同于(2)實驗的條件是__。
查看答案和解析>>
科目: 來源: 題型:
【題目】有一無色透明溶液,可能含Al3+、Fe3+、Cu2+、Mg2+、K+、OH-、CO32-、Cl-離子中的若干種。現做如下實驗:
(1)取少量該溶液,滴入用硝酸酸化的AgNO3溶液,有白色沉淀生成。
(2)另取部分溶液,加入氫氧化鈉,有白色沉淀產生,加入氫氧化鈉的量與生成白色沉淀的量可用右圖表示。
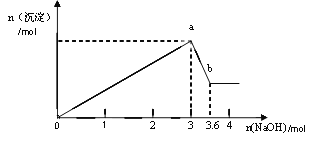
試推斷:
(1)該溶液中以上離子一定存在的有___________,一定不存在的有____________。
(2)上述溶液中至少有_____________、(填化學式)等物質混合而成,其物質的量的比為_________。
(3)寫出圖中a![]() b變化過程的離子方程式_________________。
b變化過程的離子方程式_________________。
(4)為進一步確定溶液中其他的陽離子,應該補充的實驗是_____________
查看答案和解析>>
科目: 來源: 題型:
【題目】工業上采用的一種污水處理方法如下:保持污水的pH在5.0~6.0之間,通過電解生成Fe(OH)3。Fe(OH)3具有吸附性,可吸附污物而沉積下來,有凈化水的作用。陰極產生的氣泡把污水中懸浮物帶到水面形成浮渣層,刮去(或撇掉)浮渣層,即起到了浮選凈化的作用。某科研小組用該原理處理污水,設計裝置如圖所示。下列說法正確的是
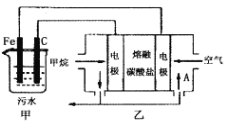
A.為了增加污水的導電能力,應向污水中加入適量的H2SO4溶液
B.甲裝置中Fe電極的反應為Fe-3e-=Fe3+
C.當乙裝置中有1.6gCH4參加反應,則C電極理論上生成氣體體積為4.48L
D.為了使該燃料電池長時間穩定運行,電池的電解質組成應保持穩定,電池工作時,循環的物質A為CO2
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室里需要純凈的氯化鈉溶液,但手邊只有混有Na2SO4、NH3HCO3 等雜質 的NaCl。某學生設計了如下圖方案提取純凈物的NaCl溶液(已知:NH4HCO3![]() NH3↑+H2O+CO2↑)
NH3↑+H2O+CO2↑)
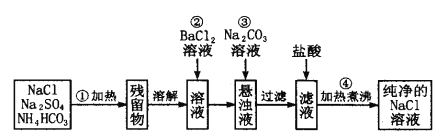
如果此方案正確,那么:
(1)操作①可選擇_______ 或__________(儀器)。
(2)操作②為什么不用加硝酸鋇溶液?其理由是___________。
(3)進行操作②后,如何判斷SO42-已除盡的方法是__________ 。
(4)操作③的目的是________,寫出此操作涉及的離子方程式:___________
(5)操作④的目的是_________。
查看答案和解析>>
科目: 來源: 題型:
【題目】據《科技日報》報道,我國科學家研制成功一系列石墨烯限域的3d過渡金屬中心(Mn、Fe、Co、Ni、Cu)催化劑,在室溫條件下以H2O2為氧化劑直接將CH4氧化成C的含氧化合物。請回答下列問題:
(1)在Fe、Co、Ni、Cu中,某基態原子核外電子排布遵循“洪特規則特例”(指能量相同的原子軌道在全滿、半滿、全空狀態時,體系的能量最低),該原子的外圍電子排布式為__。
(2)在第四周期所有元素中,基態原子未成對電子數最多的元素是__(填元素符號)。
(3)金屬晶體熱導率隨溫度升高會降低,其原因是__。
(4)銅的焰色反應呈___。在現代化學中,常用于區分晶體與非晶體的方法為___。
(5)Mn和Co的熔點較高的是___,原因___。
(6)鈷晶胞和白銅(銅鎳合金)晶胞分別如圖1、2所示。

①鈷晶胞堆積方式的名稱為__;
②已知白銅晶胞的密度為dg·cm-3,NA代表阿伏加德羅常數的值。圖2晶胞中兩個面心上銅原子最短核間距為__pm(列出計算式)。
查看答案和解析>>
科目: 來源: 題型:
【題目】在恒容條件下,反應:2SO2 (g) + O2 (g) ![]() 2SO3(g) ΔH =-QkJ·mol-1。在上述條件下分別充入的氣體和反應放出的熱量 ( Q>0 )如下表所列:
2SO3(g) ΔH =-QkJ·mol-1。在上述條件下分別充入的氣體和反應放出的熱量 ( Q>0 )如下表所列:
容器 | SO2 (mol) | O2(mol) | N2(mol) | Q(kJ·mol-1) |
甲 | 2 | 1 | 0 | Q1 |
乙 | 1 | 0.5 | 0 | Q2 |
丙 | 1 | 0.5 | 1 | Q3 |
根據以上數據,下列敘述正確的是( )
A. 在上述條件下反應生成lmol SO3固體放熱Q/2 kJ B. 2Q3 <2Q2=Q1<Q
C. Ql =2Q2= 2Q3 = Q D. 2Q2 = 2Q3 < Q1 < Q
查看答案和解析>>
科目: 來源: 題型:
【題目】二氧化硫是危害最為嚴重的大氣污染物之一,它主要來自化石燃料的燃燒,研究CO催化還原SO2的適宜條件,在燃煤電廠的煙氣脫硫中具有重要價值。
Ⅰ.從熱力學角度研究反應
(1) C(s)+O2(g)![]() CO2(g) ΔH1=-393.5 kJ·mol-1
CO2(g) ΔH1=-393.5 kJ·mol-1
CO2(g)+C(s)![]() 2CO(g) ΔH2=+172.5 kJ·mol-1
2CO(g) ΔH2=+172.5 kJ·mol-1
S(s)+O2(g)![]() SO2(g) ΔH3=-296.0 kJ·mol-1
SO2(g) ΔH3=-296.0 kJ·mol-1
寫出CO 還原SO2的熱化學方程式:_________________。
(2)關于CO還原SO2的反應,下列說法正確的是______。
A.在恒溫恒容條件下,若反應體系壓強不變,則反應已達到平衡狀態
B.平衡狀態時,2v正(CO)=v逆(SO2)
C.其他條件不變,增大SO2的濃度,CO的平衡轉化率增大
D.在恒溫恒壓的容器中,向達到平衡狀態的體系中充入N2,SO2的平衡轉化率不變
Ⅱ.NOx的排放主要來自于汽車尾氣,包含NO2和NO,有人提出用活性炭對NOx進行吸附,發生反應如下:
反應a:C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH=-34.0kJ/mol
N2(g)+CO2(g) ΔH=-34.0kJ/mol
反應b:2C(s)+2NO2(g)![]() N2(g)+2CO2(g) ΔH=-64.2kJ/mol
N2(g)+2CO2(g) ΔH=-64.2kJ/mol
(3)對于反應a,在T1℃時,借助傳感器測得反應在不同時間點上各物質的濃度如下:
時間(min) 濃度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①0~10min內,NO的平均反應速率v(NO)=___________,當升高反應溫度,該反應的平衡常數K___________(選填“增大”、“減小”或“不變”)。
②30min后,只改變某一條件,反應重新達到平衡;根據上表中的數據判斷改變的條件可能是___________(填字母)。
A.加入一定量的活性炭 B.通入一定量的NO
C.適當縮小容器的體積 D.加入合適的催化劑
(4)①某實驗室模擬反應b,在密閉容器中加入足量的C和一定量的NO2氣體,維持溫度為T2℃,如圖為不同壓強下反應b經過相同時間NO2的轉化率隨著壓強變化的示意圖。請從動力學角度分析,1050kPa前,反應b中NO2轉化率隨著壓強增大而增大的原因_____________;在1100kPa時,NO2的體積分數為___________。
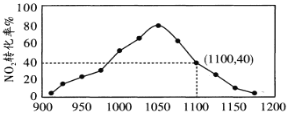
②用某物質的平衡分壓代替其物質的量濃度也可以表示化學平衡常數(記作Kp);在T2℃、1.1×106Pa時,該反應的化學平衡常數Kp=___________(計算表達式表示);已知:氣體分壓(P分)=氣體總壓(P總)×體積分數。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com