
科目: 來源: 題型:
【題目】下列說法不正確的是
A.在硫酸工業的吸收塔中,采用濃硫酸吸收三氧化硫
B.Na2O2吸收CO2產生O2,可用作呼吸面具供氧劑
C.SO2與過量氨水反應得到![]()
D.無水CoCl2吸水會變為藍色,可用于判斷變色硅膠是否吸水
查看答案和解析>>
科目: 來源: 題型:
【題目】溴化鈣是一種重要的化工原料,常見有![]() 和
和![]() 等結晶形式。某興趣小組以廢鐵屑為原料制備
等結晶形式。某興趣小組以廢鐵屑為原料制備![]() 的主要流程:
的主要流程:
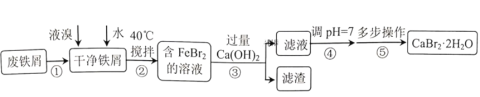
相關信息如下:
①![]() 吸濕性強。
吸濕性強。
②34℃時結晶得到![]() ,
,![]() 加熱至210℃得到
加熱至210℃得到![]() 。
。
請回答:
(1)步驟①的目的是去除廢鐵屑表面的油污,方法是________。
(2)實驗室模擬海水提取溴的過程中,用苯萃取溶液中的溴,選出其正確操作并按順序列出字母:涂凡士林→檢漏→()→()→()→()→()→清洗干凈。________
a.打開玻璃塞放氣
b.打開旋塞放氣
c.將溶液和苯轉移至分液漏斗中,塞上玻璃塞
d.雙手托住分液漏斗,右手壓住玻璃塞,左手握住旋塞,上下顛倒振蕩
e.右手壓住玻璃塞,左手握住旋塞,將分液漏斗倒轉振蕩
f.置于鐵架臺鐵圈上靜置,打開玻璃塞,將旋塞擰開,放出下層液體
g.從下口放出溴的苯溶液
h.從上口倒出溴的苯溶液
(3)步驟④調pH=7,適宜加入的試劑是________,通過調節分液漏斗的活塞可以控制添加液體的速率。當溶液pH接近7時,滴加試劑的分液漏斗的活塞應如圖中的________(填序號)所示。

(4)下列有關說法正確的是________。
A.步驟②反應控制在40℃左右,原因是防止反應過于劇烈并減少液溴揮發
B.步驟③濾渣成分只有![]() 、
、![]() 和
和![]()
C.為使![]() 快速結晶,可用冰水浴進行冷卻
快速結晶,可用冰水浴進行冷卻
D.步驟⑤包括蒸發濃縮、冷卻結晶、過濾、洗滌、干燥等多步操作
(5)制得的![]() 可以通過如下步驟測定其純度:①稱取樣品質量;②溶解;③滴入足量Na2CO3溶液,充分反應后過濾,洗滌,干燥;④稱量。
可以通過如下步驟測定其純度:①稱取樣品質量;②溶解;③滴入足量Na2CO3溶液,充分反應后過濾,洗滌,干燥;④稱量。
若實驗操作規范而測定結果偏低,其可能的原因是________。
查看答案和解析>>
科目: 來源: 題型:
【題目】四種短周期元素的微粒信息如表:
元素代號 | Q | R | X | Z |
微粒信息 | 離子: | 單質分子:R2 | 離子:X3+ | 一種原子: |
已知Q、R、X都在第三周期,R2常溫常壓下為黃綠色氣體。
完成下列填空:
(1)Q在周期表的位置是:___。化合物Q2Z的電子式為___。
(2)Q、R、X的原子半徑由大到小的順序為___(用元素符號表示);Q、R、X、Z中金屬性最強的是___(用元素符號表示)。
(3)Q與X兩者的最高價氧化物對應的水化物之間發生反應的方程式為____。
查看答案和解析>>
科目: 來源: 題型:
【題目】氰[(CN)2]的化學性質與鹵素(X2)很相似,化學上稱之為擬鹵素,其氧化性介于Br2和I2之間,下列有關反應方程式不正確的是
A. (CN)2和NaOH溶液反應:(CN)2+2OH-=CN-+CNO-+H2O
B. MnO2和HCN反應:MnO2+4HCN(濃)![]() Mn(CN)2+(CN)2↑+2H2O
Mn(CN)2+(CN)2↑+2H2O
C. 在NaBr和KCN混合溶液中通入少量Cl2:Cl2+2CN-=2Cl-+(CN)2
D. 向KCN溶液中加入碘水:I2+2KCN=2KI+(CN)2
查看答案和解析>>
科目: 來源: 題型:
【題目】現使用酸堿中和滴定法測定市售鹽酸的總酸量(g/100mL)。
Ⅰ.實驗步驟:
(1)用酸式滴定管取待測鹽酸溶液20.00mL于錐形瓶中,向其中滴加2滴___作指示劑。
(2)讀取盛裝0.1000mol/LNaOH溶液的堿式滴定管的初始讀數。如果液面位置如圖所示,則此時的讀數為____mL。
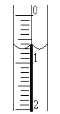
(3)滴定。當___時,停止滴定,并記錄NaOH溶液的終讀數。重復滴定3次。
Ⅱ.實驗記錄
滴定次數 實驗數據(mL) | 1 | 2 | 3 | 4 |
V(樣品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.數據處理與討論:
(4)甲同學在處理數據時計算得:
平均消耗的NaOH溶液的體積V=(15.95+15.00+15.05+14.95)/4mL = 15.24mL。
指出他的計算的不合理之處:___。按正確數據處理,可得c(待測鹽酸)=___mol/L。
查看答案和解析>>
科目: 來源: 題型:
【題目】測定硫酸銅晶體(CuSO4xH2O)中x值的實驗過程如下:

完成下列填空:
(1)必須要進行恒重操作的原因是___。
(2)下面是某同學的一次實驗記錄,請完成下表。
稱量數據1 | 稱量數據2 | 稱量數據3 | 結晶水的X值 | 實驗誤差 |
11.685g | 13.691g | 12.960g | ____ | ____ |
(3)本次實驗測得X值偏__(高、低),可能這次實驗中產生誤差的原因可能是___。
A.硫酸銅晶體中含有不揮發性雜質 B.實驗前晶體表面有濕存水
C.加熱時有晶體飛濺出去 D.加熱失水后露置在空氣中冷卻
查看答案和解析>>
科目: 來源: 題型:
【題目】乙烯、乙炔屬于不飽和鏈烴,易起加成、聚合、氧化反應。
完成下列填空:
(1)乙烯分子中的官能團是____。
(2)能與乙烯發生加成反應的物質是___(填寫編號)。
a.溴水 b.氧氣 c.氯化氫 d.酸性高錳酸鉀溶液
(3)乙烯和氫氣的加成產物為____。(寫結構簡式)
(4)寫出乙烯發生加聚反應的化學方程式___。
(5)實驗室制取乙炔的化學方程式為____。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列有關說法正確的是
A. 1L水中溶解了40.0 g NaOH,該溶液的物質的量濃度為1 mol/L
B. 從1L2mol/L的NaCl液中取出0.5L,取出的該溶液的濃度為1mol/L
C. 中和100 mL 1mol/L的H2SO4溶液,需NaOH8.0g
D. 配制500mL0.5mol/L的CuSO4溶液,需40.0g膽礬
查看答案和解析>>
科目: 來源: 題型:
【題目】過二硫酸鈉(Na2S2O8)也叫高硫酸鈉,可用于廢氣處理及有害物質氧化降解.用(NH4)2S2O8溶液和一定濃度的NaOH溶液混合可制得Na2S2O8晶體,同時還會放出氨氣。某化學興趣小組利用該原理在實驗室制備Na2S2O8晶體(裝置如圖所示).

已知:反應過程中發生的副反應為2NH3+3Na2S2O8+6NaOH![]() 6Na2SO4+6H2O+N2
6Na2SO4+6H2O+N2
(1)圖中裝有NaOH溶液的儀器的名稱為___,反應過程中持續通入氮氣的目的是___。
(2) (NH4)2S2O8可由電解硫酸銨和硫酸的混合溶液制得,寫出電解時陽極的電極反應式:___。
(3)Na2S2O8溶于水中,會發生一定程度的水解,最終僅生成H2SO4、Na2SO4和另一種常溫下為液態且具有強氧化性的物質,寫出該反應的化學方程式:___。
(4)Na2S2O8具有強氧化性,該興趣小組設計實驗探究不同環境下Na2S2O8氧化性的強弱。將MnSO4H2O(1.69g)與過量Na2S2O8(10g)溶于水中形成的混合溶液煮沸3min,觀察并記錄加入試劑時和加熱過程中的現象(如表格所示)。
環境 | 調節溶液氧化環境時的現象 | 加熱煮沸3min期間產生的現象 |
中性 | 加入VmL蒸餾水,無明顯現象 | 30s時開始有大量氣泡冒出,3min后溶液變深棕色,溶液中有懸浮小顆粒 |
堿性 | 加入VmL某濃度的NaOH溶液,瞬間變為棕色(MnO2) | 10s后溶液逐漸變為深紫色(MnO4-),沒有明顯冒氣泡現象 |
酸性 | 加入VmL稀H2SO4無明顯現象 | 煮沸3min后,有氣泡冒出 |
①在___(填“中性”“酸性”或“堿性”)條件下,Na2S2O8的氧化能力最強。
②中性氧化時,會產生大量氣泡,其原因為___。
③若用0.1molL-1的H2O2溶液滴定堿性氧化反應后的溶液(先將溶液調至酸性再滴定),滴定終點時的現象為___;達到滴定終點時,消耗H2O2溶液的體積為V1rnL。則堿性氧化后的溶液中NaMnO4的質量為___ g(用含V1的代數式表示,5H2O2~2![]() )。
)。
查看答案和解析>>
科目: 來源: 題型:
【題目】X、Y、Z三種短周期元素在周期表中的位置如下圖所示。若X的最高正價與負價的代數和為2,則下列說法正確是
![]()
A. 原子序數由大到小為 Z >Y>X
B. 氫化物最穩定的元素為Z
C. 最高價氧化物的水化物酸性最強的元素為Z
D. 原子半徑由大到小為 Y>Z>X
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com