
科目: 來源: 題型:
【題目】按要求填空:某班同學用如下實驗探究Fe2+、Fe3+的性質。回答下列問題:
(1)甲組同學取2mLFeCl2溶液,加入幾滴氯水,再加入1滴KSCN溶液,溶液變紅,說明Cl2可將Fe2+氧化。FeCl2溶液與氯水反應的離子方程式為___。
(2)乙組同學認為甲組的實驗不夠嚴謹,該組同學在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入幾滴氯水和1滴KSCN溶液,溶液變紅,煤油的作用是___。
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖中,A是氯氣的發生裝置,B、C是凈化氣體的裝置,B裝置中裝有飽和食鹽水,D中裝鐵絲網;反應后E的底部有棕色固體聚集;F是堿液用于吸收多余氣體的裝置。
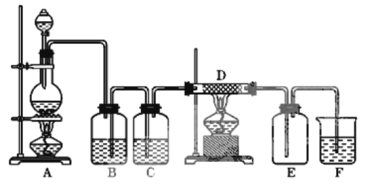
(1)上述裝置中有一處錯誤,請指出是___處(用字母表示)。
(2)B裝置的作用是___,C裝置中需要加入___。
(3)寫出A中發生反應的化學方程式___。
(4)如果A中產生氯氣2.24L(標準狀況),則被氧化的HCl的物質的量為___。
查看答案和解析>>
科目: 來源: 題型:
【題目】某溶液中可能含有H+、Mg2+、NH4+、Al3+、Fe3+、CO32—、SO42—、Cl—中的幾種。若加入鋅粒,產生無色無味的氣體;若加入NaOH溶液,產生白色沉淀,且產生的沉淀量與加入NaOH的物質的量之間的關系如圖所示。則下列說法不正確的是
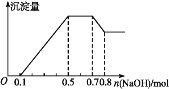
A. 溶液中的陽離子有H+、Mg2+、NH4+、Al3+
B. 溶液中n(Al3+)=0.1 mol
C. 溶液中一定不含CO32—,可能含有SO42—和Cl—
D. n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
查看答案和解析>>
科目: 來源: 題型:
【題目】(NH4)3[Fe(SCN)6]、[Fe(TCNE)(NCCH3)2][FeCl4] 、K4[Fe(CN)6]·3H2O等鐵的配合物用途非常廣泛。回答下列問題:
(1)基態Fe原子價層電子的電子排布圖(軌道表達式)為______。
(2)Fe與Ca位于同一周期且最外層電子構型相同,鐵的熔點和沸點均比鈣的高,其原因是____。
(3)配合物(NH4)3[Fe(SCN)6]中的H、S、N的電負性從大到小的順序是_____ 。
(4)[Fe(TCNE)(NCCH3)2][FeCl4]中,配體為CH3CN和TCNE( )。
)。
①CH3CN中碳原子的雜化方式是 ____ 和_____ 。
②TCNE中第一電離能較大的是 ___(填元素符號),分子中所有原子____(填“在”或“不在”)同一平面,分子中σ 鍵與π鍵的數目之比是 ___。
(5)K4[Fe(CN)6]·3H2O是食鹽的抗結劑,強熱分解有Fe3C生成, Fe3C 的晶胞結構如圖所示:

Fe3C的密度為 ___(列出計算式)g·cm-3。
查看答案和解析>>
科目: 來源: 題型:
【題目】Cl2通入足量的氫氧化鈉溶液,溫度不同時充分反應后產物溶液中除大量OH-外,還有Cl-、ClO-、ClO3-,已知:Cl2+OH-→Cl-+ClO-+H2O(冷堿)、Cl2+OH-→Cl-+ClO3-+H2O(熱堿),并知ClO-、ClO3-離子的物質的量比為2:1,試問原混合氣體中Cl2與反應后溶液中的Cl-物質的量之比為( )
A.2:5B.3:1C.1:1D.5:7
查看答案和解析>>
科目: 來源: 題型:
【題目】葡萄可用于釀酒。
(1)檢驗葡萄汁含葡萄糖的方法是:向其中加堿調至堿性,再加入新制備的Cu(OH)2,加熱,其現象是_______________________________________。
(2)葡萄在釀酒過程中,葡萄糖轉化為酒精的過程如下,補充完成下列化學方程式。
C6H12O6(葡萄糖)![]() 2________+2C2H5OH
2________+2C2H5OH
(3)葡萄酒密封儲存過程中生成了有香味的酯,酯也可以通過化學實驗來制備。實驗室用下圖所示裝置制備乙酸乙酯:

①試管a中生成乙酸乙酯的化學方程式是________________________________。
②試管b中盛放的試劑是飽和_________________溶液。
⑧實驗開始時,試管b中的導管不伸入液面下的原因是___________________。
④若分離出試管b中生成的乙酸乙酯,需要用到的儀器是____(填序號)。
a. 漏斗 b. 分液漏斗 c. 長頸漏斗
查看答案和解析>>
科目: 來源: 題型:
【題目】按要求填空:
(1)有機物命名:
![]() ________________________________;
________________________________;
![]() ___________________________________;
___________________________________;
(2)依據名稱寫出物質:
3,4-二甲基-4-乙基庚烷 ______________;3,4,4-三甲基-1-戊炔 ______________。
(3)已知有機物降冰片二烯的分子結構可表示為: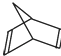
①降冰片二烯的分子式為 ______________;②降冰片二烯屬于 __________;
a.環烴 b.不飽和烴 c.烷烴 d.烯烴
查看答案和解析>>
科目: 來源: 題型:
【題目】工業上用某礦渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取銅的操作流程如圖(金屬單質E可由濾液C制取):
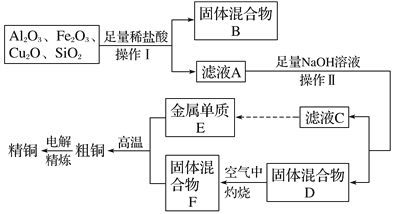
已知:Cu2O+2H+=Cu+Cu2++H2O。
(1)固體混合物B的成分是__。
(2)濾液A中鐵元素的存在形式為__(填離子符號),生成該離子與Fe元素有關的離子反應方程式為___,___。
(3)在濾液C中通入過量CO2氣體,除了CO2+OH-=HCO3-主要離子方程式有:__。
查看答案和解析>>
科目: 來源: 題型:
【題目】氮化硅高溫陶瓷材料是現代重要的結構陶瓷,因其有硬度大、熔點高、化學性質穩定等特點而受到廣泛關注。工業上普遍用下列流程進行生產:
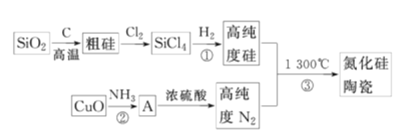
(1)SiO2和C反應除了得到粗硅外,還有可能得到一種硬度也很大的物質SiC,是生成粗硅還是生成該物質主要是由___決定的。
(2)反應①的條件是隔絕空氣和____。
(3)寫出制粗硅的反應的化學方程式____。
(4)寫出硅與氫氧化鈉溶液的離子方程式____。
(5)現在是用四氯化硅、氮氣、氫氣在稀有氣體保護下加強熱,得到純度較高的氮化硅,其反應方程式為___。
查看答案和解析>>
科目: 來源: 題型:
【題目】將一塊鎂鋁合金(不含其它物質)投入到50ml的稀鹽酸溶液中,充分反應后,固體無剩余,向所得溶液中逐滴滴入cmol/LNaOH溶液時,得到沉淀的質量與所滴加NaOH溶液的體積有如圖關系:
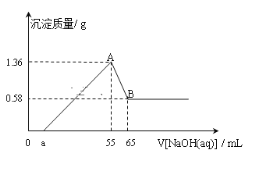
(1)圖中B點表示沉淀的化學式為___;AB段發生反應的離子方程式為___。
(2)合金中金屬鋁的物質的量為___mol;
(3)稀鹽酸溶液的濃度為___mol/L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com