
科目: 來源: 題型:
【題目】抗癌藥托瑞米芬的前體J的合成路線如下。
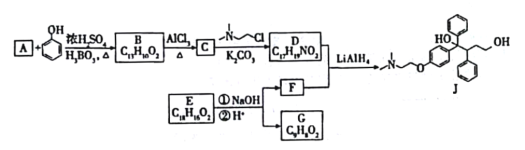
已知:
i.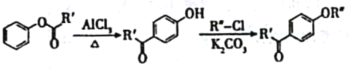
ii.有機物結構可用鍵線式表示,如(CH3)2NCH2CH3的鍵線式為![]()
(1)有機物A能與Na2CO3溶液反應產生CO2,其鈉鹽可用于食品防腐,其名稱為_______________.
(2)C中含有的官能團為______________________________(填名稱)。
(3)C→D的化學反應方程式為_________________________,反應類型為______________________。
(4)E是一種天然香料,經堿性水解、酸化,得F和G。G經還原可轉化為F。G的結構簡式為________________________________。
(5)K是G的同分異構體,符合下列條件的K的結構簡式是_____________________。(任意寫一種)
①包含2個六元環
②K可水解,與NaOH溶液供熱時,1molK消耗1molNaOH
(6)推測D和F反應得到J的過程中,反應物LiAIH4的作用是_________________。
(7)由J合成托瑞米芬的古城:
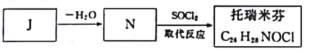
托瑞米芬具有反應結構,其結構簡式為_______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】有600 mL某種混合物溶液,只可能含有以下離子中的若干種:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,現將此溶液分成三等份,進行如下實驗:
(1)向第一份中加入AgNO3溶液,有沉淀產生;
(2)向第二份中加足量NaOH溶液并加熱后,收集到氣體0.04 mol;
(3)向第三份中加足量BaCl2溶液后,得干燥的沉淀6.27g,經足量鹽酸洗滌、干燥后,沉淀質量為2.33g。 根據上述實驗現象,以下推測正確的是
A. K+不一定存在 B. Ba2+、Mg2+不一定都存在
C. Cl-不一定存在 D. 混合溶液中CO32-的濃度為0.2 mol/L
查看答案和解析>>
科目: 來源: 題型:
【題目】在恒容密閉容器中,由CO合成甲醇:CO(g)+2H2(g)![]() CH3OH(g),在其他條件不變的情況下,研究溫度對反應的影響,實驗結果如圖所示,下列說法正確的是
CH3OH(g),在其他條件不變的情況下,研究溫度對反應的影響,實驗結果如圖所示,下列說法正確的是

A.CO合成甲醇的反應為吸熱反應B.平衡常數![]()
C.該反應在![]() 時的平衡常數比
時的平衡常數比![]() 時的小D.處于A點的反應體系從
時的小D.處于A點的反應體系從![]() 變到
變到![]() ,達到平衡時
,達到平衡時![]() 增大
增大
查看答案和解析>>
科目: 來源: 題型:
【題目】在恒溫密閉容器中發生反應:CaCO3(s)![]() CaO(s)+CO2(g) H>0,反應達到平衡后,tl時縮小容器體積, x隨時間(t)變化的關系如下圖所示。x不可能是( )
CaO(s)+CO2(g) H>0,反應達到平衡后,tl時縮小容器體積, x隨時間(t)變化的關系如下圖所示。x不可能是( )
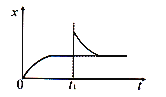
A. υ逆(逆反應速率)B. ρ(容器內氣體密度)
C. m(容器內CaO質量)D. p(容器壓強)
查看答案和解析>>
科目: 來源: 題型:
【題目】已知298.15K時,可逆反應:Pb2+(aq)+Sn(s)![]() Pb(s)+Sn2+(aq)的平衡常數K=2.2,若溶液中Pb2+和Sn2+的濃度均為0.010mol·L-1,則反應進行的方向是
Pb(s)+Sn2+(aq)的平衡常數K=2.2,若溶液中Pb2+和Sn2+的濃度均為0.010mol·L-1,則反應進行的方向是
A. 向右進行 B. 向左進行 C. 處于平衡狀態 D. 無法判斷
查看答案和解析>>
科目: 來源: 題型:
【題目】高鐵酸鉀是一種高效多功能的新型非氯綠色消毒劑,主要用于飲水處理。實驗小組制備高鐵酸鉀(K2FeO4)并探究其性質。
資料:K2FeO4為紫色固體,微溶于KOH溶液;具有強氧化性,在酸性或中性溶液中快速產生O2,在堿性溶液中較穩定。
(1)制備K2FeO4(夾持裝置略)
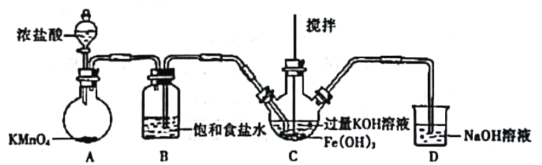
①如圖所示,A為氯氣發生裝置。裝置A、B、C、D中存在錯誤的是______________(填序號)。
②C中得到紫色固體和溶液。C中通入氯氣發生反應,生成高鐵酸鉀(K2FeO4)的化學方程式為_______,此外Cl2還可能與過量的KOH反應。
(2)探究K2FeO4的性質
①取C中紫色溶液,加入稀硫酸,產生黃綠色氣體,得溶液a,經檢驗氣體中含有Cl2。為證明是否K2FeO4,氧化了Cl-而產生Cl2,設計以下方案:
方案I | 取少量溶液a,滴加KSCN溶液至過量,溶液呈紅色。 |
方案II | 用KOH溶液充分洗滌C中所得固體,再用KOH溶液將K2FeO4溶出,得到紫色溶液b。取少量b,滴加鹽酸,有Cl2產生。 |
i.由方案I中溶液變紅可知溶液a中含有__________離子,但該離子的存在不能判斷一定是K2FeO4,氧化了Cl2,因為K2FeO4,在酸性溶液中不穩定,請寫出K2FeO4在酸性溶液中發生反應的離子方程式___________________________________。
ii.方案Ⅱ可證明K2FeO4,氧化了Cl-.用KOH溶液洗滌的目的是_______________。
②根據K2FeO4的制備實驗得出:氧化性Cl2_____FeO42- (填“>”或“<”),而方案Ⅱ實驗表明,Cl2和FeO42-的氧化性強弱關系恰好相反,原因是_______________。
(3)若在制備裝置C中加入Fe(OH)3的質量為14.0g,充分反應后經過濾、洗滌、干燥得K2FeO4固體19.3g,則K2FeO4的產率為______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】非線性光學晶體在信息、激光技術、醫療、國防等領域具有重要應用價值。我國科學家利用Ca2CO3, XO2(X= Si、Ge)和H3BO3首次合成了組成為CsXB3O7的非線性光學晶體。回答下列問題:
(1)基態硼原子的價電子排布圖是____________,與硼處于同周期的非金屬主族元素的第一電離能由大到小的順序為________________。
(2)B的簡單氫化物BH3,不能游離存在,常傾向于形成較穩定的B2H6或與其他分子結合。
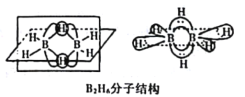
①B2H6分子結構如圖,則B原子的雜化方式為____________________。
②氨硼烷(NH3BH3)被認為是最具潛力的新型儲氫材料之一,分子中存在配位鍵,提供孤電子對的成鍵原子是______________,寫出一種與氨硼烷互為等電子體的分子_________(填分子式)。
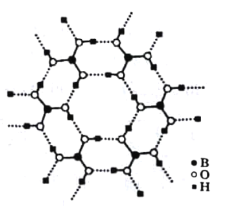
(3)如圖為H3BO3晶體的片層結構,其中B的雜化方式為_______;硼酸在熱水中比在冷水中溶解度顯著增大的主要原因是____________。
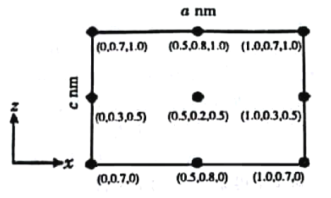
(4)以晶胞參數為單位長度建立的坐標系可以表示晶胞中各原子的位置,稱為原子分數坐標。CsSiB3O7屬于正交晶系(長方體形),晶胞參數為anm、bnm和cnm.如圖為沿y軸投影的晶胞中所有Cs原子的分布圖和原子分數坐標。據此推斷該晶胞中Cs原子的數目為_________;CsSiB3O7的摩爾質量為Mg·mol-1,設NA為阿伏加德羅常數的值,則CsSiB3O7晶體的密度為_____g·cm-3(用含字母的代數式表示)。
查看答案和解析>>
科目: 來源: 題型:
【題目】實驗室中某些氣體的制取、收集及尾氣處理裝置如圖所示(省略夾持和凈化裝置)。僅用此裝置和表中提供的物質完成相關實驗,最合理的選項是

選項 | a中的物質 | b中的物質 | c中收集的氣體 | d中的物質 |
A | 濃氨水 | CaO | NH3 | H2O |
B | 濃硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 濃鹽酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目: 來源: 題型:
【題目】在一定溫度下,CO和水蒸氣分別為1 mol、3 mol,在密閉容器中發生反應CO+H2O(g)![]() CO2+H2,達平衡后測得CO2為0.75 mol,再通入6 mol水蒸氣,達到新的平衡后,CO2和H2的物質的量之和可能為
CO2+H2,達平衡后測得CO2為0.75 mol,再通入6 mol水蒸氣,達到新的平衡后,CO2和H2的物質的量之和可能為
A. 1.2 mol B. 1.8 mol C. 2.5 mol D. 1.5mol
查看答案和解析>>
科目: 來源: 題型:
【題目】赤銅礦的主要成分是Cu2O,輝銅礦的主要成分是Cu2S,將赤銅礦與輝銅礦混合加熱發生以下反應:
Cu2S+2Cu2O=6Cu+SO2↑,關于該反應的說法中正確的是
A.該反應的氧化劑與還原劑物質的量之比為2:1
B.Cu2S 在反應中只做還原劑
C.Cu 是氧化產物,SO2是還原產物
D.每生成38.4gCu,反應中轉移0.6mol電子
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com