
科目: 來源: 題型:
【題目】隨原子序數遞增,八種短周期元素(用字母x等表示)原子半徑的相對大小、最高正價或最低負價的變化如下圖所示。

根據判斷出的元素回答問題:
(1)f在周期表中的位置是____________。
(2)比較d、e常見離子的半徑大小(用化學式表示,下同):________>________;比較g、h的最高價氧化物對應水化物的酸性強弱:____________>____________。
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式:________________________。
(4)寫出e的單質在空氣中燃燒所得產物的電子式:______________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】下列反應的離子方程式書寫正確的是
A.向硫酸銅溶液中加入鐵片:3Cu2++2Fe=2Fe3++3Cu
B.石灰石與醋酸反應:CaCO3+2CH3COOH=2CH3COO-+Ca2++CO2↑+H2O
C.碳酸氫銨與足量熱的NaOH溶液反應:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
D.向Ba(OH)2溶液中加入少量NaHSO3溶液:2HSO3-+Ba2++2OH-= BaSO3↓+SO32-+H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】新型納米材料MFe2Ox(3<x<4)中M表示+2價的金屬元素,在反應中化合價不發生變化。常溫下,MFe2Ox能使工業廢氣中的SO2轉化為S,流程如下,則下列判斷正確的是( )
![]()
A.MFe2Ox是氧化劑
B.SO2是該反應的催化劑
C.x<y
D.MFe2Oy是還原產物
查看答案和解析>>
科目: 來源: 題型:
【題目】常用調味劑花椒油是一種從花椒籽中提取的揮發性香精油,可溶于乙醇、乙醚等有機溶劑。利用如圖所示裝置處理花椒籽粉,經分離提純得到花椒油。
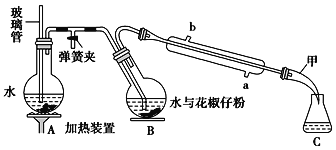
實驗步驟:
(一)在A裝置中的圓底燒瓶中裝入![]() 容積的水,加幾粒沸石。同時,在B中的圓底燒瓶中加入20g花椒籽粉和50mL水。
容積的水,加幾粒沸石。同時,在B中的圓底燒瓶中加入20g花椒籽粉和50mL水。
(二)加熱A裝置中的圓底燒瓶,當有大量蒸氣產生時關閉彈簧夾,進行蒸餾。
(三)向餾出液中加入食鹽至飽和,再用15mL乙醚萃取2次,將兩次萃取的醚層合并,加入少量無水Na2SO4;將液體傾倒入蒸餾燒瓶中,蒸餾得花椒油。
(1)裝置A中玻璃管的作用是___,裝置B中圓底燒瓶傾斜的目的是___。
(2)步驟(二)中,當觀察到儀器甲中有無色油狀液體餾出時,可停止蒸餾。蒸餾結束時,下列操作的順序為___(填標號)。
①停止加熱 ②打開彈簧夾 ③關閉冷凝水
(3)在餾出液中加入食鹽的作用是___;加入無水Na2SO4的作用是___。
(4)實驗結束后,用稀NaOH溶液清洗冷凝管,反應的化學方程式為___。
(殘留物以 表示)
表示)
(5)為測定花椒油中油脂的含量,取20.00mL花椒油溶于乙醇中,加80.00mL0.5mol/LNaOH的乙醇溶液,攪拌,充分反應,加水配成200mL溶液。取25.00mL加入酚酞,用0.1moI/L鹽酸進行滴定,滴定終點消耗鹽酸20.00mL。則該花椒油中含有油脂___g/L。
(以 計,式量:884)。
計,式量:884)。
查看答案和解析>>
科目: 來源: 題型:
【題目】下圖是幾種常見有機物之間的轉化關系圖。A為常見醫用消毒藥品,C具有濃郁香味。
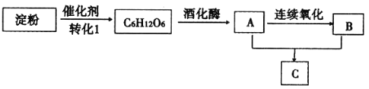
根據以上信息及各物質的轉化關系,完成下列各題:
(1)A的結構簡式為_____,寫出工業上用乙烯生產A的化學方程式_________。
(2)B的官能團名稱為______。
(3)A+B→C的化學方程式為______,反應類型為反應_______。
(4)下列說法正確的是_____
a.上圖物質中只有C6H12O6屬于糖類
b.轉化1可在人體內完成
c.物質C屬于油脂
d.物質A和B均為電解質
查看答案和解析>>
科目: 來源: 題型:
【題目】有機物M(C6H4S4)是隱形飛機上吸波材料的主要成分。某化學興趣小組為探究其組成和分子結構,進行如下實驗:
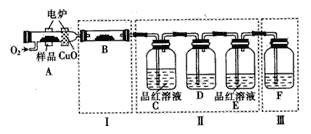
(1)將少量樣品放入燃燒管A中,通入足量O2,用電爐加熱使其充分燃燒,并將燃燒產物依次通入余下裝置(夾持儀器的裝置已略去)。
①寫出A中樣品燃燒的化學方程式______。
②裝置B的目的是驗證有機物中含氫元素,則B中盛裝的試劑可為______。
③D中盛放的試劑是______(填序號)。
a.NaOH溶液b.品紅溶液c.KMnO4溶液d.飽和石灰水
④裝置A中燃燒管放入CuO的作用是______。
⑤指出裝置F的錯誤______。
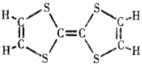
(2)M的結構簡式如圖所示,4.08g M可使_____mol氫氣發生反應,同樣質量的M完全燃燒需要消耗氧氣_____mL(標準狀況)。
查看答案和解析>>
科目: 來源: 題型:
【題目】現有某鐵碳合金,某化學興趣小組為了測定鐵碳合金中鐵的質量分數,并探究濃硫酸的還原產物,設計了如圖所示的實驗裝置和實驗方案(夾持儀器已省略),請你參與此項活動并回答相應問題:
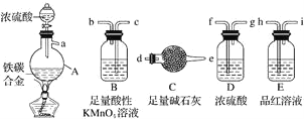
(1)該裝置的連接順序a___(填接口字母),連接好裝置后,首先應進行的操作是____。
(2)mg鐵碳合金中加入濃H2SO4,點燃酒精燈一段時間后,用滴管吸取A中的溶液滴入到適量水中作為試樣,試樣中所含金屬離子的成分有以下三種可能:A:只含有Fe3+;B:只含有Fe2+;C:____,若為A,則A中反應的化學方程式為___,驗證C種可能的實驗方法___。
(3)待A中不再逸出氣體時,停止加熱,拆下C并稱重,C增重bg。鐵碳合金中鐵的質量分數____(寫表達式)。
(4)某同學認為利用此裝置測得鐵的質量分數偏大,請你寫出可能的原因:_____。
(5)隨著反應的進行,A中還可能發生某些離子反應。寫出相應的離子方程式____。
查看答案和解析>>
科目: 來源: 題型:
【題目】某實驗小組探究H2O2分解的速率及影響因素,在相同溫度下按照下表所示的方案完成實驗。

(1)上述實驗方案中,探究的變量因素只有催化劑的實驗組合是_____和_____。
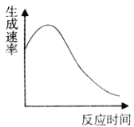
(2)實驗④過程中氧氣的生成速率和時間的趨勢關系如圖所示,判斷該反應是反應(填“放熱”或“吸熱”)______。
(3)實驗⑤:在試管中加入10mL 0.4mol/L H2O2溶液,加入固體催化劑,在一定溫度下測得不同時刻生成O2的體積(以折算為標準狀況)如下表所示(假設反應過程溶液的體積保持不變):
![]()
①反應6min,H2O2分解了_______%。
②0至6min,以H2O2的濃度變化表示的反應速率為υ(H2O2)=________molL-1min-1。
查看答案和解析>>
科目: 來源: 題型:
【題目】某同學按下圖裝置進行實驗探究,請回答下列問題:

(1)電能轉化為化學能的裝置為_______池(填“A”或“B”)。
(2)A裝置鋅為_______極,實驗過程中氫離子濃度較大的是區域______(填“Zn電極”或“Cu電極”)。
(3)B裝置石墨2為_______極,電極反應式為_______;當石墨1放出2240mL氣體(標準狀況下)時,電路中轉移電子的數目為_________,若A裝置也轉移相同數量的電子,鋅的質量減少了_______g。
查看答案和解析>>
科目: 來源: 題型:
【題目】酯化反應是酸與醇發生反應生成酯和水的反應。下列反應屬于酯化反應的是( )
A. CH3COOH+NaOH→CH3COONa+H2O
B. CH2==CHCOOCH3+H2![]() CH3CH2COOCH3
CH3CH2COOCH3
C. CH3COOCH2CH3+H2O![]() CH3COOH+CH3CH2OH
CH3COOH+CH3CH2OH
D. 2CH3COOH+HOCH2CH2OH![]() CH3COOCH2CH2OOCCH3+2H2O
CH3COOCH2CH2OOCCH3+2H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com