
科目: 來源: 題型:
【題目】基本知識填空
(1)在一定條件下,當一個可逆反應的_____與____相等時,反應物的濃度與生成物的濃度不再改變,即達到化學平衡狀態。
(2)化學平衡狀態的特征:_____、____、_____、_____、_____。
(3)對于可逆化學反應mA+nBpC+qD在一定溫度下達到化學平衡時,其平衡常數表達式為:______。
(4)強電解質包括的范圍:____、____、____。弱電解質包括的范圍:____、_____、____、_____。
查看答案和解析>>
科目: 來源: 題型:
【題目】NA表示阿伏伽德羅常數,下列判斷正確的是( )
A.NA個O2和28g N2所占的體積都約為22.4 L
B.標準狀況下,22.4 L H2O含有NA個水分子
C.71g Cl2與足量NaOH溶液反應,轉移的電子數為2NA
D.1.8g的NH4+ 離子中含有的電子數NA
查看答案和解析>>
科目: 來源: 題型:
【題目】自然界的氮循環如下圖所示,下列說法不正確的是( )

A.①中N2與O2反應生成NO
B.②中合成氨屬于人工固氮
C.③中氮元素只被氧化
D.氧元素參與了氮循環
查看答案和解析>>
科目: 來源: 題型:
【題目】鐵元素是重要的金屬元素,鐵及其化合物在日常生產生活中應用廣泛,研究鐵及其化合物的應用意義重大。
(1)所含鐵元素具有氧化性也有還原性的物質是_________。
a.鐵單質 b.氯化亞鐵 c.鐵紅 d.Fe3O4
(2)高鐵酸鉀(K2FeO4)是一種新型、高效、多功能綠色水處理劑,濕法制備高鐵酸鉀(K2FeO4)的反應體系中有六種微粒:Fe(OH)3、C1O-、OH-、FeO42-、Cl-、H2O。寫出并配平濕法制高鐵酸鉀的離子反應方程式:____ Fe(OH)3+___ ClO-+_______=____FeO42-+____Cl-+______
(3)電子工業上用氯化鐵腐蝕銅箔,制造印刷電路板,并從使用過的腐蝕廢液(含有FeCl2、CuCl2、FeCl3)中回收銅,并獲得氯化鐵晶體,其工藝流程如下:回答下列問題:
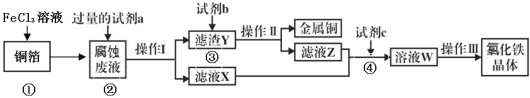
①反應①的化學方程式:_______________;
②從反應①和②可以判斷出Fe2+、Cu2+、Fe3+的氧化性從強到弱順序為:____________;
③操作I用到的玻璃儀器有燒杯、玻璃棒和___________;
④濾液X、Z中都有同一種溶質,它們轉化為溶液W的離子方程式為:___________________。
查看答案和解析>>
科目: 來源: 題型:
【題目】(1)請寫出NaHCO3在水中的電離方程式:______________;NaOH溶液與NaHCO3溶液反應的離子方程式:________________。
(2)某無色透明溶液中可能大量存在NH4+、Na+、Ba2+、Fe3+、CO32-、SO42-、Cl-中的幾種離子。從其中取兩份各100mL溶液,進行如下實驗:
①根據溶液顏色可以判斷溶液中不存在的離子是_____________;
②取其中的一份溶液進行實驗,加入過量氫氧化鈉濃溶液并加熱,共生成448mL氣體(標準狀況下),有關的離子方程式為______________;
③取另一份溶液加入過量Ba(NO3)2溶液,生成3.94g白色沉淀,過濾,向沉淀中再加入足量稀鹽酸,沉淀全部溶解;根據以上實驗結果確定:原溶液中肯定存在的離子有___________;請你設計實驗方案證明該溶液中是否含有Cl-?_____________ 。
(3)某氮肥廠的氨氮廢水中氮元素多以NH4+和NH3·H2O的形式存在。該廠的技術團隊設計該廢水處理方案流程如下:
![]()
①過程Ⅱ:在微生物的作用下實現NH4+→NO2-→NO3-轉化,稱為硝化過程。在堿性條件下,NH4+被氧氣(O2)氧化成NO3-的總反應的離子方程式為________________。
②過程Ⅲ:在一定條件下向廢水中加入甲醇(CH3OH),實現HNO3→NO2-→N2轉化,稱為反硝化過程。反硝化過程中甲醇(C元素為-2價)轉化為CO2,若有6molHNO3完全轉化成N2,消耗的甲醇的物質的量為_____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某小組同學通過“FeSO4被HNO3氧化”的實驗,驗證Fe2+的還原性。
實驗一:驗證Fe2+的還原性
實驗操作 | 預測現象 | 實驗現象 |
向盛有2mLFeSO4溶液的試管中,滴入幾滴濃硝酸,振蕩 | 試管中產生紅棕色氣體,溶液變為黃色 | 試管中產生紅棕色氣體, 溶液變為深棕色 |
(1)紅棕色氣體是______________ (填化學式);
(2)實驗現象與預期不符,繼續進行實驗。取深棕色溶液于試管中,滴加KSCN溶液,溶液變為血紅色,該現象說明____________。
實驗二:探究溶液變為深棕色的原因
〔資料與猜想〕查閱資料后猜想,可能是生成的NO2或者NO與溶液中的Fe2+或Fe3+反應,而使溶液變為深棕色。
〔實驗與探究〕用下圖所示裝置進行實驗,步驟及現象如下:(裝置的氣密性已檢驗,尾氣處理已略去)
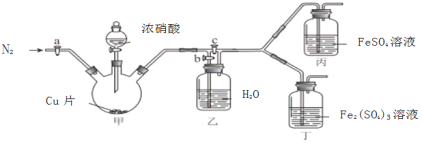
ⅰ關閉c,打開a和b,通入N2,一段時間后關閉a;
ⅱ向甲中加入適量濃HNO3,一段時間后丙中溶液變為深棕色,丁中溶液無明顯變化;
ⅲ關閉b,打開c,更換丙、丁中的溶液(試劑不變);
ⅳ繼續向甲中加入濃HNO3,一段時間后觀察到了與ⅱ相同的實驗現象。
根據以上實驗步驟和實驗現象回答下列問題:
(3)通入N2的目的是______________;
(4)銅與濃硝酸反應的化學方程式是_______________;
(5)裝置乙的作用是_________________;
(6)實驗結論是____________。
查看答案和解析>>
科目: 來源: 題型:
【題目】連二亞硫酸鈉(Na2S2O4),有極強的還原性,受熱、遇水都會發生分解反應放出大量的熱,甚至引起燃燒,不溶于乙醇,可溶于氫氧化鈉水溶液并穩定存在。
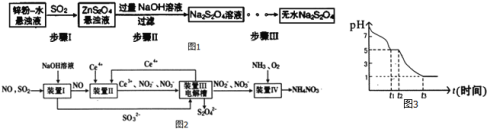
(1)鋅粉法是制備Na2S2O4的一種常見方法,其原理如圖1所示:
①須將鋅粉和水制成懸濁液的原因是 ______ ;若用Na2SO3固體和某酸反應制備SO2氣體,你認為下列最適宜選用的酸是 ______
A.濃鹽酸 B.質量分數為70%的H2SO4
C.稀硝酸 D.質量分數為10%的稀硫酸
②步驟III過程較為復雜,其中涉及過濾、洗滌、干燥等操作,請寫出洗滌過程的操作方法: ______ 。
(2)吸收大氣污染物SO2和NO,獲得Na2S2O4和NH4NO3產品的流程圖如圖2(Ce為鈰元素):
①裝置Ⅱ中,酸性條件下,NO被Ce4+氧化的產物主要是NO3-、NO2-,寫出生成NO3-的離子方程式 ______
②裝置III中電解槽陰極發生的電極反應為 ______ 。
③已知進入裝置IV的溶液中,NO2-的濃度為a gL-1,要使1m3該溶液中的NO2-完全轉化為NH4NO3,需至少向裝置IV中通入標準狀況下的O2 ______ L。(用含a代數式表示,計算結果保留整數)
(3)課題小組測定0.050molL-1Na2S2O4溶液在空氣中pH變化如圖3,0-t1段主要生成HSO3-,則0-t1發生離子反應方程式為 ______ ,t1時刻溶液中離子濃度由大到小的順序是 ______ ,t3時溶液中主要陰離子符號是 ______ 。
查看答案和解析>>
科目: 來源: 題型:
【題目】氟化鉻可用作毛織品防蛀劑、鹵化催化劑、大理石硬化及著色劑。以鉻云母礦石(含4.5%Cr2O3,還含Fe2O3、FeO、MgO、SiO2)為原料制備氟化鉻的工藝流程如下。
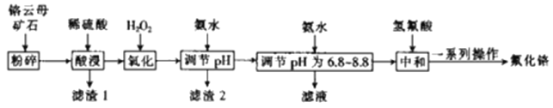
下表列出了相關金屬離子生成氫氧化物沉淀的pH:
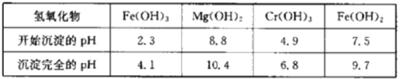
請回答下列問題:
(1)Fe2O3、MgO、FeO、SiO2中屬于堿性氧化物的有___種。
(2)將鉻云母礦石粉碎的目的是___。
(3)濾渣1主要成分的用途是___。(寫一種)
(4)Cr2O3與稀硫酸反應的化學方程式為___。
(5)第一次滴加氨水調節pH范圍為___。
(6)第二次滴加氨水調節pH為6.8~8.8的目的是___,Cr(OH)3與Al(OH)3一樣具有兩性,若第二次滴加的氨水改為NaOH溶液,生成的Cr(OH)3會部分溶解,寫出Cr(OH)3溶解的離子方程式:___。
查看答案和解析>>
科目: 來源: 題型:
【題目】如圖為碳元素的價類二維圖,結合圖中的物質部分轉化關系,完成下列問題:
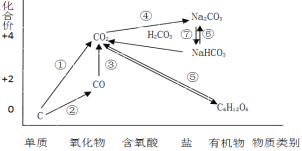
(1)下列說法正確的是 __________
a.要實現反應①一定要與氧化劑作用
b.要實現反應②一定要與還原劑作用
c.在一定條件下木炭與濃硝酸能實現 反應①轉化
d.反應⑤屬于非氧化還原反應
(2)下列有關碳及其化合物類別及性質說法不正確的是__________
a.CO不屬于酸性氧化物,具有還原性
b.CO2屬于酸性氧化物,可以與堿反應生成碳酸鹽
c.NaHCO3屬于弱酸的酸式鹽,既能與硫酸反應又能與NaOH反應
d.金剛石和石墨互為同素異形體,其物理性質和化學性質均相同
(3)高爐煉鐵的過程是將鐵礦石(Fe2O3)還原成金屬鐵的過程,實現了反應③的轉化,請寫出其反應的化學方程式,并用“雙線橋”表示電子的得失情況______________________________ 。
(4)化學活動課上,兩組同學分別用如圖所示甲、乙兩裝置探究“Na2CO3、NaHCO3與稀鹽酸的反應”。按下表中的試劑用量,在相同條件下,將兩個氣球中的固體粉末同時倒入試管中(裝置的氣密性已檢查)。請回答:
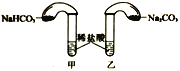
①兩組反應開始時,裝置___________(填“甲”或“乙”)中的氣球體積先變大,該裝置中反應的離子方程式是______________________。
②當試管中不再有氣體生成時,兩組實驗出現不同現象。
試劑用量 | 實驗現象 | 分析原因 | |
第A組 | 0.84gNaHCO3 1.06gNa2CO3 6ml 4mol·L-1鹽酸 | 甲中氣球與乙中氣球的 體積相等 | 甲、乙鹽酸均過量 n(NaHCO3)= n(Na2CO3) V(CO2)甲=V(CO2)乙 |
第B組 | 1.2gNaHCO3 1.2gNa2CO3 6ml 2mol·L-1鹽酸 | 甲中氣球比乙中氣球的體積大 片刻后,乙中氣球又縮小,甲中氣球的體積基本不變 |
|
按上表第A組原因分析方法,分析第B組實驗甲中氣球為比乙中氣球體積大的原因__________。用離子方程式表示第B組乙中氣球又縮小的原因:______________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某化學興趣小組為了制取并探究氨氣的性質,按下圖裝置進行實驗,制取氨氣的原理:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O,下列說法不正確的是( )
CaCl2+2NH3↑+2H2O,下列說法不正確的是( )
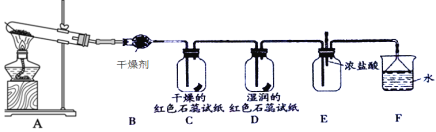
A.裝置B中的干燥劑可以是P2O5B.裝置C中的試紙不變色,D中試紙變藍色
C.在裝置E中滴入幾滴濃鹽酸會出現白煙D.裝置F中的漏斗能起防倒吸作用
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com