
科目: 來源: 題型:
【題目】已知可逆反應:M(g)+N(g)![]() P(g)+Q(g) ΔH>0,請回答下列問題:
P(g)+Q(g) ΔH>0,請回答下列問題:
(1)在某溫度下,反應物的起始濃度分別為:c(M)=1 mol·L-1,c(N)=2.4 mol·L-1;5 min后反應達到平衡,M的轉化率為60%,此時N的轉化率為________;用M表示的反應速率為________;該溫度下反應的平衡常數K=________。
(2)若反應溫度升高,M的轉化率________(填“增大”“減小”或“不變”)。
(3)若反應溫度不變,反應物的起始濃度分別為:c(M)=4 mol·L-1,c(N)=a mol·L-1;達到平衡后,c(P)=c(N)=2 mol·L-1,a=________。
(4)若反應溫度不變,反應物的起始濃度為c(M)=c(N)=b mol·L-1,達到平衡后,M的轉化率為________。
查看答案和解析>>
科目: 來源: 題型:
【題目】某實驗小組用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液進行中和熱的測定,其實驗裝置如圖所示.
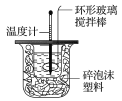
(1)寫出該反應的熱化學方程式(中和熱為57.3 kJ·mol-1):___________________________________。
(2)取50 mL NaOH溶液和30 mL硫酸溶液進行實驗,實驗數據如下表。請填寫下表中的空白:
溫度 實驗次數 | 起始溫度t1/℃ | 終止溫度t2/℃ | 溫度差平均值(t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | _____ |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(3)近似認為0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比熱容c=4.18 J·g-1·℃-1。則中和熱ΔH=________________________(取小數點后一位)。
(4)上述實驗數值結果與57.3 kJ·mol-1有偏差,產生偏差的原因可能是____________(填字母)。
a 實驗裝置保溫、隔熱效果差
b 量取NaOH溶液的體積時仰視讀數
c 分多次把NaOH溶液倒入盛有硫酸的小燒杯中
d 用溫度計測定NaOH溶液起始溫度后直接測定H2SO4溶液的溫度
查看答案和解析>>
科目: 來源: 題型:
【題目】一定條件下,在體積為3L的密閉容器中化學反應CO(g)+2H2(g)![]() CH3OH(g)達到平衡狀態。
CH3OH(g)達到平衡狀態。
(1)該反應的平衡常數表達式K=__;根據圖,升高溫度,K值將__(填“增大”、“減小”或“不變”)。
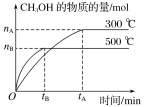
(2)500℃時,從反應開始到化學平衡狀態,以H2的濃度變化表示的化學反應速率是__(用nB、tB表示)。
(3)判斷該可逆反應達到化學平衡狀態的標志是__(填字母,下同)。
a.υ生成(CH3OH)=υ消耗(CO) b.混合氣體的密度不再改變
c.混合氣體的平均相對分子質量不再改變 d.CO、H2、CH3OH的濃度均不再變化
(4)300℃時,將容器的容積壓縮到原來的![]() ,在其他條件不變的情況下,對平衡體系產生的影響是____。
,在其他條件不變的情況下,對平衡體系產生的影響是____。
a.c(H2)減小 b.正反應速率加快,逆反應速率減慢
c.CH3OH的物質的量增加 d.重新平衡時![]() 減小
減小
查看答案和解析>>
科目: 來源: 題型:
【題目】下列表示對應化學反應的離子方程式正確的是( )
A.MnO2與濃鹽酸反應制Cl2:MnO2+4HCl![]() Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O
B.明礬溶于水產生Al(OH)3膠體:Al3++3H2O =Al(OH)3↓+3H+
C.Na2O2溶于水產生O2:Na2O2+H2O =2Na++2OH-+O2↑
D.Ca(HCO3)2溶液與少量NaOH溶液反應:HCO3-+Ca2++OH-= CaCO3↓+H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】一定溫度下,在容積固定的V L密閉容器中加入n mol A.2n mol B,發生反應:A(g)+2B(g) ![]() 2C(g) ΔH<0,反應達平衡后測得平衡常數為K,此時A的轉化率為x。
2C(g) ΔH<0,反應達平衡后測得平衡常數為K,此時A的轉化率為x。
(1)一段時間后上述反應達到平衡。則下列說法中正確的是________(填字母)。
A.物質A.B的轉化率之比為1∶2
B.起始時刻和達到平衡后容器中的壓強之比為3n∶(3n-nx)
C.當2v正(A)=v逆(B)時,反應一定達到平衡狀態
D.充入惰性氣體(如Ar),平衡向正反應方向移動
(2)K和x的關系滿足K=________。在保證A濃度不變的情況下,擴大容器的體積,平衡______(填字母)。
A.向正反應方向移動 B.向逆反應方向移動 C.不移動
(3)該反應的逆反應速率與時間的關系如圖所示。

①由圖可知,反應在t1.t3.t7時都達到了平衡,而t2.t8時都改變了一種條件,試判斷改變的條件:t2時_______________________;t8時_________________________。
②t2時平衡向___________________(填“正反應”或“逆反應”)方向移動。
③若t4時降壓,t5時達到平衡,t6時增大反應物的濃度,請在圖中畫出t4~t6時逆反應速率與時間的關系曲線__________。
查看答案和解析>>
科目: 來源: 題型:
【題目】在溫度、容積相同的3個密閉容器中,按不同方式投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如下(已知N2(g)+3H2(g)===2NH3(g) △H=-92.4kJ·mol-1)
容器 | 甲 | 乙 | 丙 |
反應物投入量 | 1 mol N2、3 mol H2 | 2 mol NH3 | 4 mol NH3 |
NH3的濃度(mol·L-1) | c1 | c2 | c3 |
反應的能量變化 | 放出a kJ | 吸收b kJ | 吸收 c kJ |
體系壓強(Pa) | p1 | p2 | p3 |
反應物轉化率 |
|
|
|
下列說法正確的是( )
A. 2c1>c3B. a+b=92.4C. 2p2<p3D. ![]() 1+
1+![]() 3>1
3>1
查看答案和解析>>
科目: 來源: 題型:
【題目】在某密閉容器中,可逆反應:A(g) + B(g)![]() xC(g)符合圖中(Ⅰ)所示關系:
xC(g)符合圖中(Ⅰ)所示關系:![]() (C)表示C氣體在混合氣體中的體積分數。由此判斷,對圖像 (Ⅱ) 說法不正確的是:
(C)表示C氣體在混合氣體中的體積分數。由此判斷,對圖像 (Ⅱ) 說法不正確的是:

A.p3>p4,Y軸表示A的轉化率
B.p3>p4,Y軸表示B的質量分數
C.p3>p4,Y軸表示B的轉化率
D.p3>p4,Y軸表示混合氣體的平均相對分子質量
查看答案和解析>>
科目: 來源: 題型:
【題目】純堿是一種重要的化工原料,對于“氨堿法”和“聯合制堿法”的分析中,錯誤的是( )
A.主反應的原理相同B.二氧化碳來源不同
C.都有氨的循環利用D.都具有一定局限性
查看答案和解析>>
科目: 來源: 題型:
【題目】甲、乙、丙、丁四種物質中,甲、乙、丙均含有相同的某種元素,它們之間具有如下轉化關系:![]() 。下列有關物質的推斷不正確的是
。下列有關物質的推斷不正確的是
A. 若甲為Cl2,則丁可能是鐵B. 若甲為NH3,則丁可能是氧氣
C. 若甲為AlCl3溶液,則丁可能是氨水D. 若甲為NaOH,則丁可能是SO2
查看答案和解析>>
科目: 來源: 題型:
【題目】通過排飽和食鹽水,用大試管收集體積比為1∶1的甲烷和氯氣混合氣(如圖),強光照射下發生反應。下列說法錯誤的是( )
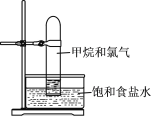
A.試管中氣體顏色變淺
B.試管內液面慢慢上升
C.水槽中的液體溶有氯化氫
D.試管內壁的油滴是純凈物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com