
科目: 來源: 題型:
【題目】銅板上鐵鉚釘長期暴露在潮濕的空氣中,形成一層酸性水膜后鐵鉚釘會被腐蝕,示意圖如下。下列說法不正確的是
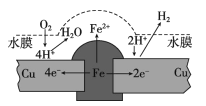
A. 腐蝕過程中銅極上始終只發生: 2H++2e-= H2↑
B. 若水膜中溶有食鹽將加快鐵鉚釘的腐蝕
C. 若在金屬表面涂一層油脂能防止鐵鉚釘被腐蝕
D. 若將該銅板與直流負極相連,則鐵銅均難被腐蝕
查看答案和解析>>
科目: 來源: 題型:
【題目】用惰性電極電解飽和食鹽水(含少量Ca2+、Mg2+)并進行相關實驗(裝置如圖),電解一段時間后,各部分裝置及對應的現象為:(1)中黑色固體變紅;(2)電極a附近溶液出現渾濁;(3)中溶液出現渾濁;(4)中溶液紅色褪去。下列對實驗現象解釋不正確的是
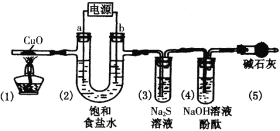
A.(1)中:CuO+H2![]() Cu+H2O
Cu+H2O
B.(2)中a電極:2H2O+2e-=H2↑+2OH-,Mg2++2OH-=Mg(OH)2↓
C.(3)中:Cl2+S2-=S↓+2Cl-
D.(4)中:Cl2具有強氧化性
查看答案和解析>>
科目: 來源: 題型:
【題目】釩基固溶體合金是一類重要的貯氫材料。某課外小組采用廉價原料NH4VO3、TiO2和Fe2O3,制出含VO2+、 TiO2+和Fe3+的金屬鹽溶液,然后選擇氨水作沉淀劑進行共沉淀反應,對共沉淀物[含 VO(OH)2, Ti(OH)4、Fe(OH)3]進行煅燒還原制備合金樣品。制備共沉淀物的裝置如下圖:
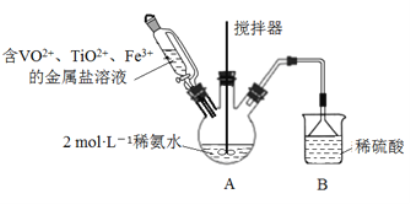
(1)用濃氨水配制500mL2mol·L-l的稀氨水,需用到的玻璃儀器有燒杯、膠頭滴管和_____________。
(2)裝置B的作用是__________________________。
(3)制備VO2+時,用草酸將VCV還原得VO2+。若把草酸改為鹽酸,也能得到VO2+,但會產生一種有毒氣體,該反應的離子方程式為__________________________。
(4)反應過程補控制溫度為60℃,三頸燒瓶的加熱方式是__________________________。
(5)往三頸燒瓶中滴加含金屬離子的混合液,得懸濁液,取出充分沉降。
①檢測上層清液是否含Fe3+的實驗方案是__________________________。
②若過濾速度較慢,可采用__________________________(填操作名稱)
③用無水乙醇洗滌:與水相比,使用無水乙醉洗滌的優點是:__________________________;簡述洗涂的具體操作:_______________________________________。
④低溫干燥,得共沉淀物。
(6)將(5)所得共沉淀物鍛燒并還原后得釩基固溶體合金。為測定產品中鐵的質量分數,取50.60g 產品溶于足量稀硫酸(其中V、Ti不溶),過濾,將濾液配成250.00mL,取25.00mL溶液,用 0.1000mol·L-1酸性KMnO4溶液滴定,進行平行實驗后,平均消耗KMnO4溶液的體積為20.00mL。則產品中鐵(M=56)的質量分數為______________________(保留2位有效數字)。
查看答案和解析>>
科目: 來源: 題型:
【題目】分別在三個容積均為2.0L的恒容密閉容器中發生反應:A(g)+B(g)D(g)。其中容器甲中反應進行至5min時達到平衡狀態,相關實驗數據如表所示:
容器 | 溫度/℃ | 起始物質的量/mol | 平衡物質的量/mol | 化學平衡常數 | ||
n(A) | n(B) | n(D) | n(D) | |||
甲 | 500 | 4.0 | 4.0 | 0 | 3.2 | K1 |
乙 | 500 | 4.0 | a | 0 | 2.0 | K2 |
丙 | 600 | 2.0 | 2.0 | 2.0 | 2.8 | K3 |
下列說法不正確的是
A.0~5min內,甲容器中A的平均反應速率v(A)=0.64mol·L-1·min-1
B.a=2.2
C.若容器甲中起始投料為2.0molA、2.0molB,反應達到平衡時,A的轉化率小于80%
D.K1=K2>K3
查看答案和解析>>
科目: 來源: 題型:
【題目】為研究鐵鹽與亞硫酸鹽之間的反應,某研究小組利用孔穴板進行了實驗探究:

小組記最的實驗現象如下表所示:
開始時 | 5min 后 | 3天后 | |
實驗I | 溶液立即變為紅褐色,比II、III中略淺 | 與開始混合時一致 | 溶液呈黃色,底部出現紅褐色沉淀 |
實驗II | 溶液立即變為紅褐色 | 紅褐色明顯變淺 | 溶液呈黃綠色 |
實驗III | 溶液立即變為紅褐色 | 紅褐色變淺,比II中深 | 溶液呈黃色 |
(1)測得實驗所用0.4mol/LFeCl3溶液及Fe(NO3)3溶液pH均約為1.0。兩溶液均呈酸性的原因是_______________(用離子方程式表示)。
(2)開始混合時,實驗I中紅褐色比II、III中略淺的原因是____________________________。
(3)為了探究5min后實驗II、III中溶液紅褐色變淺的原因,小組同學設計了實驗IV;分別取少量 5min后實驗I、II、III中溶液,加入2滴鐵氰化鉀溶液,發現實驗II、III中出現藍色沉淀,實驗I中無明顯變化。試用方程式解釋溶液中出現Fe2+的原因______________________________。
(4)針對5min后實驗III中溶液顏色比實驗II中深,小組同學認為可能存在三種因素:
①Cl-可以加快Fe3+與SO32-的氧化還原反應:
②NO3-可以______________________________;
③NO3-在酸性環境下代替Fe3+氧化了SO32-,同時消耗H+,使Fe3+水解出的Fe(OH)3較多。
通過實驗V和實驗VI進行因素探究:
實驗操作(己知Na+對實驗無影響) | 5min后的現象 | |
實驗V | 在2mLpH=1.0的0.4mol/L Fe(NO3)3溶液中溶解 固體,再加入2滴0.4mol/L Na2SO3溶液 | 溶液的紅褐色介于II、III之間 |
實驗VI | 在2mLpH=1.0的稀硝酸中溶解約0.19gNaNO3固體,再加 入2滴0.4mol/LNa2SO3溶液。向其中滴入少量BaCl2溶液 | _______________________。 |
實驗結論:因素①和因素②均成立,因素③不明顯。請將上述方案填寫完整。
(5)通過上述時間,以下結果或推論合理的是_______________(填字母)。
a.Fe3+與SO32-同時發生水解反應和氧化還原反應,且水解反應的速率快,等待足夠長時間后,將以氧化還原反應為主
b.濃度為1.2mol/L的稀硝酸在5min內不能將Fe2+氧化
c.向pH大于1的稀硝酸中加入少量Ba(NO3)2,使其完全溶解,可用來檢驗實驗1的上層淸液中是否存在SO42-
查看答案和解析>>
科目: 來源: 題型:
【題目】中科院科學家設計出一套利用SO2和太陽能綜合制氫方案,其基本工作原理如圖所示。下列說法錯誤的是
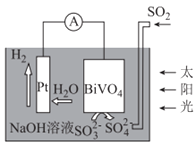
A.該電化學裝置中,Pt電極作正極
B.Pt電極的電勢高于BiVO4電極的電勢
C.電子流向:Pt電極→導線→BiVO4電極→電解質溶液→Pt電極
D.BiVO4電極上的反應式為SO32--2e-+2OH-=SO42-+H2O
查看答案和解析>>
科目: 來源: 題型:
【題目】現向下列裝置中緩慢通入氣體X,分別進行關閉和打開活塞K的操作,則品紅溶液和澄清石灰水中現象相同的一組是
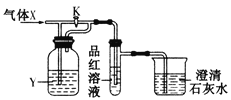
選項 | A | B | C | D |
X | NO2 | SO2 | Cl2 | CO2 |
Y(過量) | 濃H2SO4 | NaHCO3飽和溶液 | Na2SO3溶液 | NaHSO3飽和溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 來源: 題型:
【題目】利用如圖裝置可以進行實驗并能達到實驗目的的是( )

選項 | 實驗目的 | X中試劑 | Y中試劑 |
A | 用KMnO4和濃鹽酸制取并收集純凈干燥的Cl2 | 飽和食鹽水 | 濃硫酸 |
B | 用Cu與濃硝酸制取并收集純凈干燥的NO2 | 水 | 濃硫酸 |
C | 用生石灰與濃氨水制取并收集純凈干燥的NH3 | 水 | 濃硫酸 |
D | 用銅片和濃硫酸制取并收集純凈干燥的SO2 | 飽和NaHSO3溶液 | 濃硫酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 來源: 題型:
【題目】研究碳、氮、硫等元素化合物的性質或轉化對建設生態文明、美麗中國具有重要意義。
(1)海水中無機碳的存在形式及分布如下圖所示:用離子方程式表示海水呈弱堿性的原因_________。己知春季海水pH=8.1,預測夏季海水堿性將會_________(填寫“增強”或“減弱”),理由是________(寫出1條即可)
無機碳 | HCO3- | 90% |
CO32- | 9% | |
CO2 | 1% | |
H2CO3 | ||
其中H2CO3僅為CO2的0.2% | ||
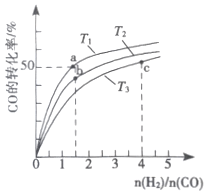
(2)工業上以CO和H2為原料合成甲醇的反應:CO(g)+2H2(g) ![]() CH3OH(g) △H<0,在容積為1L 的恒容容器中,分別在T1、T2、T3三種溫度下合成甲醇。如圖是上述三種溫度下不同H2和CO的 起始組成比(起始時CO的物質的量均為lmol)與CO平衡轉化率的關系。下列說法正確的是_________(a、b點橫坐標相同,a在曲線T1上,b在曲線T2上)
CH3OH(g) △H<0,在容積為1L 的恒容容器中,分別在T1、T2、T3三種溫度下合成甲醇。如圖是上述三種溫度下不同H2和CO的 起始組成比(起始時CO的物質的量均為lmol)與CO平衡轉化率的關系。下列說法正確的是_________(a、b點橫坐標相同,a在曲線T1上,b在曲線T2上)
A.a、b、c三點H2轉化率:c>a>b
B.上述三種溫度之間關系為T1>T2>T3
C.a點(1.5,50)狀態下再通入0.5 mol CO和0.5 mol CH3OH,平衡不移動
D.c點狀態下再通入1 molCO和4molH2,新平衡中H2的體積分數增大
(3)NO加速臭氧層被破壞,其反應過程如圖所示:
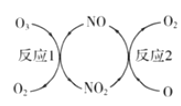
①NO的作用是__________________。
②己知:O3(g)+O(g)=2O2(g) △H =-143kJ·mol-1
反應 1: O3(g)+NO(g) ![]() NO2(g)+O2(g) △H1=-200.2kJ·mol-1
NO2(g)+O2(g) △H1=-200.2kJ·mol-1
反應2:熱化學方程式為______________________。
(4)近年來,地下水中的氮污染己成為一個世界性的環境問題。在金屬Pt、Cu和銥(Ir)的催化作用 下,密閉容器中的H2可髙效轉化酸性溶液中的硝態氮(NO3-)從而降低水體中的氮含量,其工作原理如下圖所示
①Ir表面發生反應的方程式為__________________________。
②若導電基體上的Pt顆粒增多,造成的后果是__________________________。

(5)利用電化學原理,將NO2、O2和熔融KNO3制成燃料電池,模擬工業電解法來精煉銀,裝置如圖所示,甲池工作時,NO2轉變成綠色硝化劑Y,Y是N2O5,可循環使用,則石墨II附近發生的電極反應式為__________________________。
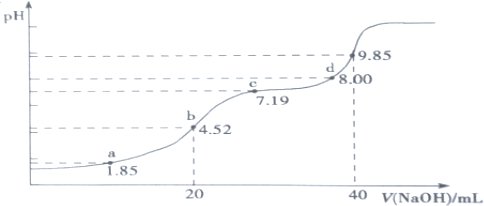
(6)大氣污染物SO 2可用NaOH吸收。已知pKa=-lgKa,25℃時,H2SO3 的 pKa1=1.85, pKa2=7.19。該溫度下用 0.1mol·L-1NaOH溶液滴定 20mL0.1mol·L-1H2SO3溶液的滴定曲線如下圖所示。b點所得溶液中各離子濃度由大到小的順序是__________________________;c點所得溶液中:c(Na+)__________3c(HSO3-)(填“>”、“<”或“=”)
查看答案和解析>>
科目: 來源: 題型:
【題目】硫化氫的轉化是資源利用和環境保護的重要研究課題。將H2S和空氣的混合氣體通入FeCl3、FeCl2、CuCl2的混合溶液中反應回收S,其物質轉化如圖所示。下列敘述正確的是
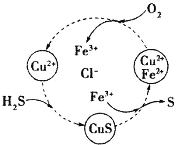
A.在轉化過程中化合價不變的元素只有Cu和Cl
B.由圖示的轉化可得出氧化性的強弱順序:O2>Cu2+>S
C.在轉化過程中能循環利用的物質只有FeCl2
D.反應中當有34gH2S轉化為硫單質時,保持溶液中Fe3+的量不變,需要消耗O2的質量為16g
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com