
科目: 來源:四川省成都市北湖校區2016-2017學年高一3月月考化學試卷 題型:填空題
填空題
(1)H、D、T三種原子,它們之間的關系是_________;在標準狀況下,它們的單質的密度之比為_____;1 mol各單質中,它們的質子數之比為________;在標準狀況下,1L各種單質中,它們的電子數之比為________。
(2)第116號元素(元素符號Lv)被中國科學技術名詞審定委員會命名為垃,該元素在元素周期表中的位置是_____,屬于______元素(填“金屬”或“非金屬”),若該元素存在最高價氧化物對應的水化物,則其化學式為_______。
(3)下列曲線分別表示元素的某種性質與核電荷數的關系(Z為核電荷數,Y為元素的有關性質)。請把與下面元素有關性質相符的曲線標號(A~G)填入相應的空格中:
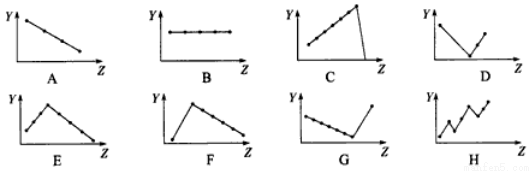
①IIA族元素的價電子數__________;②第三周期元素的最高正化合價____________;
③VIIA族元素氫化物的沸點____________。
(4)核內中子數為N的R2+,質量數為A,則ng它的相同價態氧化物中所含的電子的物質的量約為_____mol。
①若R為鈣元素,且N=19,則采用原子符號的表達方式,可將R2+表示為_______;
②若R為第五周期IIA元素,則其硫酸鹽______于水(填“溶”或“不溶”)。
查看答案和解析>>
科目: 來源:四川省成都市北湖校區2016-2017學年高一3月月考化學試卷 題型:填空題
元素周期表的形式多種多樣,下圖是扇形元素周期表的一部分(1~36號元素),對比中學常見元素周期表,思考扇形元素周期表的填充規律,并回答下列問題:

(1)L元素在常見周期表中所處的位置是________,其單質與A2E反應的化學方程式為____________。
(2)元素F、G、J、K、M對應簡單離子的離子半徑由大到小的順序是(用離子符號表示)___________。
(3)用電子式表示MO2的形成過程:_______________。
(4)B、F、G三種元素最高價氧化物對應的水化物堿性最強的是__________(填化學式)。比較元素C和J的非金屬性強弱:C______J(填“強于”或“弱于”)。
(5)向元素B和N形成的化合物的水溶液中,加入元素K的單質,所發生的反應的離子方程式為_____;反應后,向溶液中加入C、K形成的化合物,現象為___________。
(6)均由A、B、E、J四種元素組成的兩種化合物可相互反應,寫出反應的化學方程式______________。
查看答案和解析>>
科目: 來源:四川省成都市北湖校區2016-2017學年高一3月月考化學試卷 題型:填空題
現有A、B、C、D、E、F六種短周期元素,其中B,C、D、E四種元素在化學反應中均能形成簡單的陰、陽離子,且B、C、D離子具有相同的電子層結構。已知:
①A是形成物質種類最多的元素,F和A同主族;
②C的氫化物分子G是具有10電子的微粒,且可以發生下圖轉化:

③E和D是同主族元素;
④B和D可形成個數比為1:1和2:1的離子化合物X和Y。
請回答下列問題:
(1)B與D形成離子化合物Y具有漂白性,寫出Y的電子式______,該化合物和元素A的最高價氧化物O反應的化學方程式為:__________;一定量的Y與O反應后得到的固體物質,能恰好與含400 mL 2 mol/L的稀鹽酸反應,并收集到0.25 mol氣體,則該固體物質的組成為________(用物質的量表示)。
(2)G氣體的檢驗方法為_________;13.44 L氣體G(標準狀況下測定)按照上圖轉化方式可以獲得M物質的量分別為__________mol。
(3)某化學興趣小組欲采用右圖裝置證明A、C、F三種元素性質的遞變性,其中甲裝置中錐形瓶內所加試劑為石灰石:

①甲裝置中發生反應的離子方程式為________________;
②乙裝置中應添加的試劑為______________;
③丙裝置中可能發生的實驗現象為___________________________。
查看答案和解析>>
科目: 來源:四川省成都市北湖校區2016-2017學年高一3月月考化學試卷 題型:填空題
現有A、B、C、D、E、F、G七種元素,其中A、B、C、D、E、F為短周期元素且原子序數依次增大;A的最高正價與最低負價的代數和為零;B的最高價氧化物與C的氫化物在水中反應得到的生成物X既可與酸反應又可與堿反應;標準狀況下,D2氣體的密度約是1.43 g/L;E原子半徑在同周期中除稀有氣體外最大,F原子M層上的電子比K層多5個。金屬G的合金在生活中用量最大,用途最廣。
(1)畫出元素F形成的簡單離子結構示意圖_______;
(2)若X為正鹽,則其中所含的化學鍵類型有_______________;若X為酸式鹽,則它與足量E的最高價氧化物對應水化物的稀溶液反應的離子方程式為_________________;
(3)以下三種說法中,可以驗證B和F原子得電子能力強弱的是______________(填寫編號)
a.比較這兩種元素的常見單質的沸點
b.二者形成的化合物中,F元素的原子顯負價
c.比較這兩種元素的氣態氫化物的穩定性
(4)向A和F形成的化合物的水溶液中加入少量G單質,反應后,再向溶液申加入A與D形成的化合物,發現溶液顏色變黃,請用離子方程式解釋溶液變黃的原因____________。
(5)元素A和C的常見單質都是重要的化工原料,可發生反應:C2(g)+ 3A2 (g) 2CA3 (g),且己知反應物總能量高于生成物總能量。
2CA3 (g),且己知反應物總能量高于生成物總能量。
①用電子式表示C2的形成過程________________。
②己知常溫下拆開1 molA-A鍵、1 molA-C鍵、1mol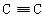 鍵分別需要吸收的能量為a kJ、b kJ、c kJ,則按上述反應生成1molCA3的過程中的能量變化為:_________(填“吸收”或“放出”) ______kJ。
鍵分別需要吸收的能量為a kJ、b kJ、c kJ,則按上述反應生成1molCA3的過程中的能量變化為:_________(填“吸收”或“放出”) ______kJ。
查看答案和解析>>
科目: 來源:四川省成都市北湖校區2016-2017學年高一3月月考化學試卷 題型:填空題
鋁是一種重要的金屬,在生產、生活中具有許多重要的用途,下圖是工業上從鋁土礦(主要成分是Al2O3,含有少量SiO2、Fe2O3等雜質)中生產鋁的工藝流程:

據此回答下列問題:
(1)電解制取鋁的化學反應中,反應物的鍵能之和_____生成物的鍵能之和(填“大于”、“小于”或“等于”)。
(2)鋁土礦中絕大部分成分都可以溶解在NaOH溶液中。請根據周期表對角線規則寫出鈹的氧化物與NaOH溶液反應的離子方程式:______________。
(3)濾渣A的主要成分____________。
(4)在工藝流程第三步中,通入過量二氧化碳所發生反應的化學方程式_______________。
(5)某同學在實驗室模擬工業生產鋁,稱取ag鋁土礦可制得bgAl(儇設每步反應進行完全),則鋁土礦中Al2O3的質量分數為____________。
查看答案和解析>>
科目: 來源:2016-2017學年河南省南陽市高一下學期第一次月考(3月)化學試卷(解析版) 題型:選擇題
下列說法中不正確的是( )
①質子數相同的微粒一定屬于同種元素
②同位素的性質幾乎完全相同
③質子數相同、電子數也相同的微粒,不可能是一種分子和一種離子
④電子數相同的微粒不一定是同一種元素
⑤一種元素只能有一種質量數
⑥某種元素的相對原子質量取整數就是其質量數
A. ①②④⑤ B. ③④⑤⑥ C. ②③⑤⑥ D. ①②⑤⑥
查看答案和解析>>
科目: 來源:2016-2017學年河南省南陽市高一下學期第一次月考(3月)化學試卷(解析版) 題型:選擇題
下列復合材料對應的性能正確的是( )
序號 | 復合材料 | 可能的性能 |
A | 金屬;C | 強度高,抗沖擊,絕緣性好,耐熱溫度低于300℃ |
B | 陶瓷;SiO2 | 耐1600℃以上高溫,強度高,密度小 |
C | 合成樹脂;SiO2、Al2O3、MgO | 耐酸堿,化學穩定性好,強度高,密度小,韌性好 |
D | 合成樹脂;C | 耐高溫,強度高,導電性好,導熱性好 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 來源:2016-2017學年河南省南陽市高一下學期第一次月考(3月)化學試卷(解析版) 題型:選擇題
鎂鋁合金溶于適量鹽酸后,再加入過量燒堿溶液, 溶液中可能大量存在的離子是( )
A. Na+、Mg2+、Al3+、Cl- B. Na+、[Al(OH)4]-、Cl- 、OH-
C. Na+、Mg2+、[Al(OH)4]-、Cl- D. Na+、Al3+、[Al(OH)4]-、Cl-
查看答案和解析>>
科目: 來源:2016-2017學年河南省南陽市高一下學期第一次月考(3月)化學試卷(解析版) 題型:選擇題
下圖是部分短周期元素化合價與原子序數的關系圖,下列說法正確的是( )

A. 原子半徑:Z>Y>X
B. 氣態氫化物的穩定性:W>R
C. W最高價氧化物對應的水化物是強堿
D. Y和Z兩者最高價氧化物對應的水化物能相互反應
查看答案和解析>>
科目: 來源:2016-2017學年河南省南陽市高一下學期第一次月考(3月)化學試卷(解析版) 題型:選擇題
已知mRn-陰離子的原子核內有x個中子,W g mRn-陰離子含有的電子的物質的量為( )
A. (m-x)n B. W(m-x-n)n C. 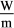 (m-x+n) D.
(m-x+n) D. 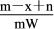
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com