
科目: 來源: 題型:解答題
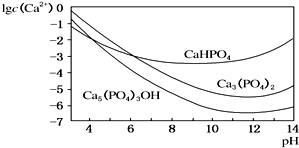 羥基磷灰石[Ca5(PO4)3OH]是一種重要的生物無機材料,其常用的制備方法有兩種:
羥基磷灰石[Ca5(PO4)3OH]是一種重要的生物無機材料,其常用的制備方法有兩種:查看答案和解析>>
科目: 來源: 題型:解答題
| 乙醇 | 溴乙烷 | 正丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸點/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:填空題
| 沸點/℃ | 水溶性 | |
| 甲醇 | 65 | 混溶 |
| 甲醛 | -21 | 混溶 |

查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:解答題
 合成氨技術的創立開辟了人工固氮的重要途徑,其研究來自正確的理論指導,合成氨反應N2+3H2?2NH3的平衡常數K值和溫度的關系如下:
合成氨技術的創立開辟了人工固氮的重要途徑,其研究來自正確的理論指導,合成氨反應N2+3H2?2NH3的平衡常數K值和溫度的關系如下:| 溫度/℃ | 360 | 440 | 520 |
| K值 | 0.036 | 0.010 | 0.0038 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| t/s | 0 | 500 | 1 000 | 1 500 |
| c(N2O5)/mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | 500 s內N2O5分解速率為2.96×10-3 mol/(L•s) | |
| B. | T1溫度下的平衡常數為K2=125,1 000 s時N2O5轉化率為50% | |
| C. | 其他條件不變時,T2溫度下反應到1 000 s時測得N2O5(g)濃度為2.98 mol/L,則T1<T2 | |
| D. | T1溫度下的平衡常數為K1,T3溫度下的平衡常數為K3,若K1>K3,則T1>T3 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| 容器編號 | 起始時各物質物質的量/mol | 達平衡時體系能量的變化 | ||
| X2 | Y2 | XY3 | ||
| ① | 1 | 3 | 0 | 放熱46.3 kJ |
| ② | 0.8 | 2.4 | 0.4 | Q(Q>0) |
| A. | 容器①、②中反應達平衡時XY3的平衡濃度相同 | |
| B. | 容器①、②中達到平衡時各物質的百分含量相同 | |
| C. | 達平衡時,兩個容器中XY3的物質的量濃度均為2 mol•L-1 | |
| D. | 若容器①體積為0.20 L,則達平衡時放出的熱量大于46.3 kJ |
查看答案和解析>>
科目: 來源: 題型:解答題
| 時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com