
科目: 來源: 題型:選擇題
| 時間/min | n(X)/mol | n(Y)/mol | n(Z)/mol |
| 0 | 0.20 | 0.60 | 0 |
| 10 | a1 | a2 | 0.25 |
| 13 | b1 | 0.45 | b2 |
| 15 | d1 | d2 | 0.30 |
| A. | 前10 min內的平均反應速率v(Y)=2.5×10-3 mol/(L•min) | |
| B. | 保持其它條件不變,升高溫度,反應達平衡時c(X)<5.0×10-3 mol/L | |
| C. | 若起始時只充入0.60 mol Z(g),反應達平衡時Z(g)的轉化率為50% | |
| D. | 若起始時充入0.60 mol X(g)、0.10 mol Y(g)和0.50 mol Z(g),達到平衡前v(正)>v(逆) |
查看答案和解析>>
科目: 來源: 題型:解答題
| 溫度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡總壓強(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡氣體總濃度(×10-3 mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| 選項 | 操作 | 現象 | 結論 |
| A | 將濃硫酸滴到蔗糖表面 | 固體變黑膨脹 | 濃硫酸有脫水性和強氧化性 |
| B | 常溫下將Al片放入濃硝酸中 | 無明顯變化 | Al濃硝酸不反應 |
| C | 將鹽酸滴入NaOH溶液 | 無現象 | 鹽酸與氫氧化鈉不反應 |
| D | 將水蒸氣通過灼熱鐵粉 | 粉末變紅 | 鐵水在高溫下發生反應 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 來源: 題型:填空題
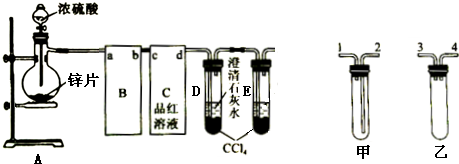
查看答案和解析>>
科目: 來源: 題型:解答題
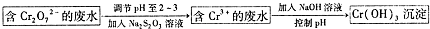
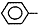 CH=CH2),聚苯乙烯的化學式為
CH=CH2),聚苯乙烯的化學式為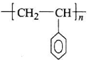 .
.查看答案和解析>>
科目: 來源: 題型:填空題
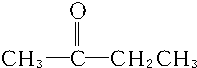 C:CH2═CH-CH2CH3或CH3CH═CH-CH3.
C:CH2═CH-CH2CH3或CH3CH═CH-CH3.查看答案和解析>>
科目: 來源: 題型:多選題
| A. | 第四周期IVA族 | B. | 第五周期IVA族 | C. | 第四周期VA族 | D. | 第五周期VA族 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | ①③⑥ | B. | ①③⑤ | C. | ②④⑤ | D. | ①②④⑥ |
查看答案和解析>>
科目: 來源: 題型:填空題
查看答案和解析>>
科目: 來源: 題型:解答題
| 時間t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
| 總壓強p/100kPa | 4.56 | 5.14 | 5.87 | 6.30 | 7.24 | 8.16 | 8.18 | 8.20 | 8.20 |
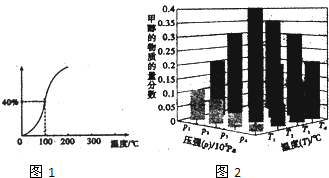
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com