
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:解答題
| 溫度/℃ | 1000 | 1150 | 1300 |
| 平衡常數 | 4.0 | 3.7 | 3.5 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| 甲 | 乙 | 丙 | 丁 | ||
| 密閉容器體積/L | 2 | 2 | 2 | 1 | |
| 起始物質的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
| n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
| SO2的平衡轉化率% | 80 | α1 | α2 | α3 | |
| A. | 甲中反應的平衡常數小于乙 | |
| B. | 該溫度下,該反應的平衡常數K為400 | |
| C. | SO2的平衡轉化率:α1>α2=α3 | |
| D. | 容器中SO3的物質的量濃度:丙=丁<甲 |
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:解答題
 催化還原CO2是解決溫室效應及能源問題的重要手段之一.研究表明,在Cu/ZnO催化劑存在下,CO2和H2可發生兩個平衡反應,分別生成CH3OH和CO.反應的熱化學方程式如下:
催化還原CO2是解決溫室效應及能源問題的重要手段之一.研究表明,在Cu/ZnO催化劑存在下,CO2和H2可發生兩個平衡反應,分別生成CH3OH和CO.反應的熱化學方程式如下:| T(K) | 催化劑 | CO2轉化率(%) | 甲醇選擇性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
查看答案和解析>>
科目: 來源: 題型:解答題
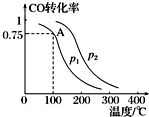 利用CO和H2可以合成甲醇,反應原理為CO(g)+2H2(g)═CH3OH(g).一定條件下,在容積為V L的密閉容器中充入a mol CO與2a mol H2合成甲醇,平衡轉化率與溫度、壓強的關系如圖所示.
利用CO和H2可以合成甲醇,反應原理為CO(g)+2H2(g)═CH3OH(g).一定條件下,在容積為V L的密閉容器中充入a mol CO與2a mol H2合成甲醇,平衡轉化率與溫度、壓強的關系如圖所示.查看答案和解析>>
科目: 來源: 題型:選擇題
 已知鹵化銀AgX的沉淀溶解平衡曲線如圖所示,橫坐標p(Ag+)=-lg(Ag+),縱坐標Y=-lg(X-),下列說法正確的是( )
已知鹵化銀AgX的沉淀溶解平衡曲線如圖所示,橫坐標p(Ag+)=-lg(Ag+),縱坐標Y=-lg(X-),下列說法正確的是( )| A. | 該溫度下AgCl的Ksp約為1×10-15 | |
| B. | a點可表示AgCl的過飽和溶液 | |
| C. | b點時c(Ag+)=c(I-) | |
| D. | 該溫度下,AgCl和AgBr飽和溶液中:c(Cl-)<c(Br-) |
查看答案和解析>>
科目: 來源: 題型:選擇題
| 化學式 | CH3COOH | H2CO3 | AgCl | Ag2CrO4 |
| Ka或Ksp | Ka=1.8×10-5 | Ka1=4.1×10-7 Ka2=5.6×10-11 | Ksp=1.8×10-10 | Ksp=2.0×10-12 |
| A. | 常溫下,相同濃度①CH3COONH4 ②NH4HCO3 ③(NH4)2CO3溶液中,c(NH4+)由大到小的順序是:①>②>③ | |
| B. | 向飽和氯水中滴加NaOH 溶液至溶液剛好為中性時,c(Na+)=2c(ClO-)+c(HClO) | |
| C. | AgCl 易溶于氨水難溶于水,所以AgCl 在氨水中的Ksp 大于水中的 Ksp | |
| D. | 向濃度均為1×10-3mol•L-1的KCl 和K2CrO4混合液中滴加1×10-3mol•L-1 的AgNO3溶液,CrO42-先形成沉淀 |
查看答案和解析>>
科目: 來源: 題型:解答題
 化工工業中常用乙苯脫氫的方法制備苯乙烯.
化工工業中常用乙苯脫氫的方法制備苯乙烯.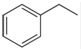 (g)→
(g)→ (g)+H2(g),△H=+117.6kJ/mol;
(g)+H2(g),△H=+117.6kJ/mol; (g)+CO(g)+H2O(g) △H=+158.8 kJ/mol
(g)+CO(g)+H2O(g) △H=+158.8 kJ/mol查看答案和解析>>
科目: 來源: 題型:多選題
| 容量 | 甲 | 乙 | 丙 | 丁 |
| A | 2mol | 1mol | 2mol | 1mol |
| B | 1mol | 1mol | 2mol | 2mol |
| A. | A的轉化率:丁>丙>乙>甲 | B. | A的轉化率:丁>乙>丙>甲 | ||
| C. | B的轉化率:丙>甲>乙>丁 | D. | B的轉化率:甲>乙>丙>丁 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com