
科目: 來源: 題型:選擇題
| 物質 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| 完全沉淀時的pH范圍 | ≥9.6 | ≥6.4 | 3~4 |
| A. | 向該混合溶液中加入少量鐵粉即能觀察到紅色固體析出 | |
| B. | 向該混合溶液中逐滴加入NaOH溶液,最先看到藍色沉淀 | |
| C. | 該混合溶液中c(SO42-):{c(Cu2+)+c(Fe2+)+c(Fe3+)}>5:4 | |
| D. | 向該混合溶液中加入適量氯水,并調節pH為3~4,然后過濾,可得到純凈的CuSO4溶液 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 物質 | CH3OH | CH3OCH3 | H2O |
| c(mol•L-1) | 0.8 | 1.24 | 1.24 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 容器 | 甲 | 乙 |
| 反應物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH(g)和1mol H2O(g) |
| 平衡時c(CH3OH) | c1 | c2 |
| 平衡時能量變化 | 放出29.4kJ | 吸收a kJ |

查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
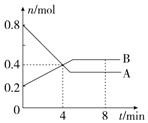 Ⅰ.某溫度時,在2L容器中,某一化學反應中A、B的物質的量隨時間變化的曲線如圖所示,由圖中數據分析得:
Ⅰ.某溫度時,在2L容器中,某一化學反應中A、B的物質的量隨時間變化的曲線如圖所示,由圖中數據分析得:查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:實驗題
| 實驗序號 | 溫度 | 0min | 10min | 20min | 30min | 40min | 50min | 60min |
| 1 | 820℃ | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 820℃ | c1 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
| 3 | 800℃ | c2 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 |
| 4 | 800℃ | 1.0 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 | 0.20 |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com