
科目: 來源: 題型:解答題
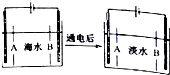 南海諸島是我國固有領土,但多數島上淡水資源匱乏,為檢驗某島上泉水是否達標,取樣品對其進行檢驗:
南海諸島是我國固有領土,但多數島上淡水資源匱乏,為檢驗某島上泉水是否達標,取樣品對其進行檢驗:查看答案和解析>>
科目: 來源: 題型:解答題
 N、C、S元素的單質及化合物在工農業生成中有著重要的應用
N、C、S元素的單質及化合物在工農業生成中有著重要的應用| t/min | n(CO)/mol | n(Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 鍋爐水垢中的CaSO4經飽和碳酸鈉溶液浸泡可轉化為CaCO3 | |
| B. | 常溫下,在含有Ag+和Cl-的溶液中,Ag+和Cl-濃度之積是個常數 | |
| C. | 當醋酸達到電離平衡后,改變某條件電離平衡向正反應方向移動,則溶液的導電能力一定變強 | |
| D. | 將濃度為0.1 mol/L的HF溶液加水不斷稀釋,溶液$\frac{c({F}^{-})}{c({H}^{+})}$始終保持增大 |
查看答案和解析>>
科目: 來源: 題型:解答題
| 時間/min SO2質量/10-3g 溫度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| T1 | 2100 | 1052 | 540 | 199 | 8.7 | 0.06 | 0.06 |
| T2 | 2100 | 869 | 242 | x | x | x | x |
查看答案和解析>>
科目: 來源: 題型:解答題
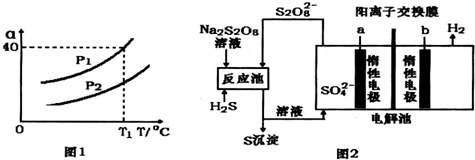
查看答案和解析>>
科目: 來源: 題型:解答題
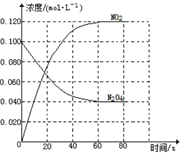
查看答案和解析>>
科目: 來源: 題型:選擇題
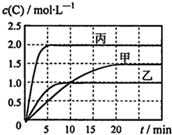 向甲、乙、丙三個密閉容器中充入一定量的A和B,發生反應:A(g)+хB(g)?2C(g).各容器的反應溫度、反應物起始量,反應過程中物質C的濃度隨時間變化關系分別用表和圖表示:
向甲、乙、丙三個密閉容器中充入一定量的A和B,發生反應:A(g)+хB(g)?2C(g).各容器的反應溫度、反應物起始量,反應過程中物質C的濃度隨時間變化關系分別用表和圖表示:| 容器 | 甲 | 乙 | 丙 |
| 容積 | 0.5L | 0.5L | 1.0L |
| 溫度/℃ | T1 | T2 | T3 |
| 反應物起始量 | 1.5molA 0.5molB | 1.5molA 0.5molB | 6.0molA 2.0molB |
| A. | 達平衡時A(g)的濃度:乙=丙>甲 | |
| B. | 甲容器中達平衡時B(g)的轉化率為75% | |
| C. | 溫度分別為T1、T2時,該反應的平衡常數:K(T1)<K(T2) | |
| D. | 丙容器中達到平衡后,若同時向容器中再充入1mol A(g)、1mol B(g)、1molC(g),則平衡向逆反應方向移動 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | c(Ag+) | B. | $\frac{c(C{l}^{-})}{c(B{r}^{-})}$ | C. | c(Cl-) | D. | $\frac{c(A{g}^{+})•c(B{r}^{-})}{c(C{l}^{-})}$ |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
 碳是形成物種最多的元素之一,許多含碳物質對人類極其重要.
碳是形成物種最多的元素之一,許多含碳物質對人類極其重要.| 時間/min | 0 | 10 | 20 | 30 |
| n(C8H10)/mol | 0.40 | 0.30 | 0.26 | n2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com