
科目: 來源: 題型:選擇題
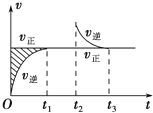 恒溫密閉容器發生可逆反應:Z(?)+W(?)?X(g)+Y(?);△H,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態后未再改變條件.下列有關說法中正確的是( )
恒溫密閉容器發生可逆反應:Z(?)+W(?)?X(g)+Y(?);△H,在t1時刻反應達到平衡,在t2時刻縮小容器體積,t3時刻再次達到平衡狀態后未再改變條件.下列有關說法中正確的是( )| A. | Z和W在該條件下有一種是為氣態 | |
| B. | t1~t2時間段與t3時刻后,兩時間段反應體系中氣體的平均摩爾質量不可能相等 | |
| C. | 若在該溫度下此反應平衡常數表達式為K=c(X),則t1~t2時間段與t3時刻后的X濃度不相等 | |
| D. | 若該反應只在某溫度T0以上自發進行,則該反應的平衡常數K隨溫度升高而增大 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | (m+n)必定小于 p | B. | (m+n)必定大于 p | C. | m 必定小于 p | D. | n 必定大于 p |
查看答案和解析>>
科目: 來源: 題型:解答題
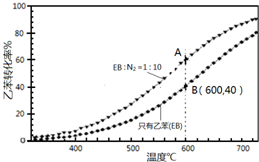 苯乙烯(
苯乙烯(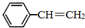 )是生產各種塑料的重要單體,可通過乙苯催化脫氫制得:
)是生產各種塑料的重要單體,可通過乙苯催化脫氫制得: CH2CH3(g)$\stackrel{催化劑}{?}$
CH2CH3(g)$\stackrel{催化劑}{?}$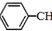 =CH2(g)+H2(g)△=+QkJ.mol-1
=CH2(g)+H2(g)△=+QkJ.mol-1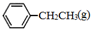 、
、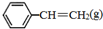 、H2(g)的燃燒熱(△H)分別為-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,寫出Q與Q1、Q2、Q3的關系式Q2+Q3-Q1.
、H2(g)的燃燒熱(△H)分別為-Q1 kJ•mol-1、-Q2kJ•mol-1、-Q3 kJ•mol-1,寫出Q與Q1、Q2、Q3的關系式Q2+Q3-Q1.查看答案和解析>>
科目: 來源: 題型:解答題
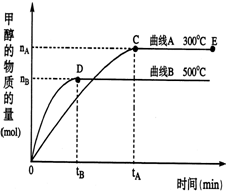 一定條件下,在體積為2L的密閉容器中,一氧化碳與氫氣在催化劑作用反應生成甲醇:CO(g)+2H2(g)?CH3OH(g).根據題意完成下列各題:
一定條件下,在體積為2L的密閉容器中,一氧化碳與氫氣在催化劑作用反應生成甲醇:CO(g)+2H2(g)?CH3OH(g).根據題意完成下列各題:查看答案和解析>>
科目: 來源: 題型:解答題
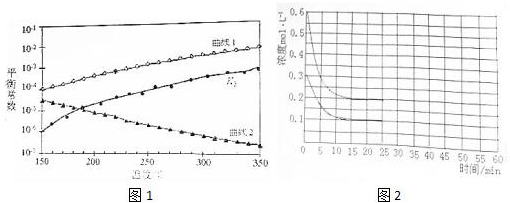
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
| 碳 | 氮 | Y | |
| X | 硫 | Z |
 ,其中氮的化合價為②-2,實驗室可用次氯酸鈉溶液與氨反應制備聯氨,反應的化學方程式為③NaClO+2NH3=N2H4+NaCl+H2O .
,其中氮的化合價為②-2,實驗室可用次氯酸鈉溶液與氨反應制備聯氨,反應的化學方程式為③NaClO+2NH3=N2H4+NaCl+H2O .查看答案和解析>>
科目: 來源: 題型:多選題
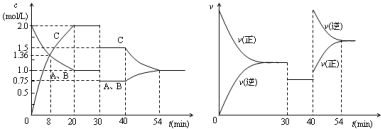
| A. | 30min時降低溫度,40min時升高溫度 | |
| B. | 8min前A的平均反應速率為0.17mol/(L•min) | |
| C. | 反應方程式中的x=1,正反應為放熱反應 | |
| D. | 20min~40min間該反應的平衡常數均為4 |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com