
科目: 來源: 題型:選擇題
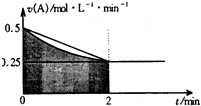 某溶液中發生反應:A═2B+C,A的反應速率v(A)與時間t的圖象如圖所示.若溶液的體積為2L,且起始時只加入A物質,下列說法錯誤的是( )
某溶液中發生反應:A═2B+C,A的反應速率v(A)與時間t的圖象如圖所示.若溶液的體積為2L,且起始時只加入A物質,下列說法錯誤的是( )| A. | 圖中陰影部分的面積表示0-2min內A的物質的量濃度的減小值 | |
| B. | 反應開始的前2min,A的平均反應速率小于0.375mol•L-1•min-1 | |
| C. | 至2min時,A的物質的量減小值介于0.5mol至1mol之間 | |
| D. | 至2min時,c(B)介于1mol•L-1 至1.5mol•L-1 之間 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 有氣體參加的化學反應,若增大壓強(即縮小反應容器的體積),可增加活化分子的百分數,從而使反應速率增大 | |
| B. | 活化分子間的碰撞一定能導致化學鍵斷裂 | |
| C. | 在FeCl3+3KSCN═Fe(SCN)3+3KCl平衡體系中,加入KCl固體,平衡逆向移動 | |
| D. | NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g)△H=+185.57kJ/mol,能自發進行,原因是體系有自發地向熵增的方向轉變的傾向 |
查看答案和解析>>
科目: 來源: 題型:實驗題
查看答案和解析>>
科目: 來源: 題型:多選題
| A. | 容器內氣體壓強保持不變 | |
| B. | 吸收ymolH2只需1 mo1MHx | |
| C. | 若向容器內通入少量氫氣,則V(放氫)>V(吸氫) | |
| D. | 若降溫,該反應的平衡常數增大 |
查看答案和解析>>
科目: 來源: 題型:實驗題
查看答案和解析>>
科目: 來源: 題型:選擇題
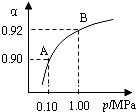
| A. | 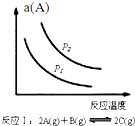 如圖反應:△H<0,P2>P1 | |
| B. |  如圖反應:△H<0,T1>T2 | |
| C. |  如圖反應:△H>0,T2>T1 | |
| D. |  如圖反應:△H>0,T2>T1或△H<0,T2<T1 |
查看答案和解析>>
科目: 來源: 題型:實驗題
查看答案和解析>>
科目: 來源: 題型:實驗題
查看答案和解析>>
科目: 來源: 題型:解答題
 工業上以硫為原料生產硫酸,已知4g硫完全可放出aKJ的熱,則
工業上以硫為原料生產硫酸,已知4g硫完全可放出aKJ的熱,則查看答案和解析>>
科目: 來源: 題型:選擇題
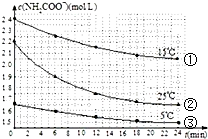 已知氨基甲酸銨發生的水解反應為:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,某研究小組得到c(NH2COO-)隨時間變化曲線如圖所示.下列有關說法一定正確的是( )
已知氨基甲酸銨發生的水解反應為:NH2COONH4+2H2O?NH4HCO3+NH3•H2O,某研究小組得到c(NH2COO-)隨時間變化曲線如圖所示.下列有關說法一定正確的是( )| A. | 對比①與③,可知濃度越大水解速率越快 | |
| B. | 對比①與②,可知溫度越高水解速率越快 | |
| C. | 加水稀釋,平衡向正反應方向移動,K值增大 | |
| D. | 氨基甲酸銨在堿性條件下比在酸性條件下水解程度大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com