
科目: 來源: 題型:解答題
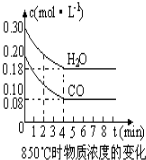 在一體積為10L的容器中,通入一定量的CO和H2O,在850℃時發生如下反應:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,CO和H2O濃度變化如圖.
在一體積為10L的容器中,通入一定量的CO和H2O,在850℃時發生如下反應:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0,CO和H2O濃度變化如圖.| 時間(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:解答題
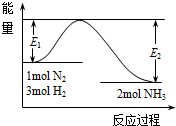 氨是氮循環過程中的重要物質,氨的合成是目前普遍使用的人工固氮方法.
氨是氮循環過程中的重要物質,氨的合成是目前普遍使用的人工固氮方法.查看答案和解析>>
科目: 來源: 題型:解答題
| 溫度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
查看答案和解析>>
科目: 來源: 題型:實驗題
| 實驗次數 | 待測氫氧化鈉溶液體積(mL) | 標準鹽酸體積(mL) | NaOH溶液濃度(mol/L) | ||
| 初讀數 | 末讀數 | 體積 | |||
| 1 | 20.00 | 0.50 | 20.70 | 20.20 | 0.1059 |
| 2 | 20.00 | 6.00 | 26.00 | 20.00 | |
查看答案和解析>>
科目: 來源: 題型:填空題
查看答案和解析>>
科目: 來源: 題型:解答題
查看答案和解析>>
科目: 來源: 題型:實驗題
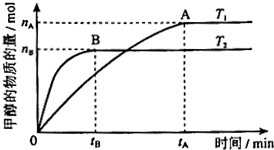 科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃燒熱△H分別為-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.
科學家利用太陽能分解水生成的氫氣在催化劑作用下與二氧化碳反應生成甲醇.已知H2(g)、CO(g)和CH3OH(l)的燃燒熱△H分別為-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1.查看答案和解析>>
科目: 來源: 題型:實驗題
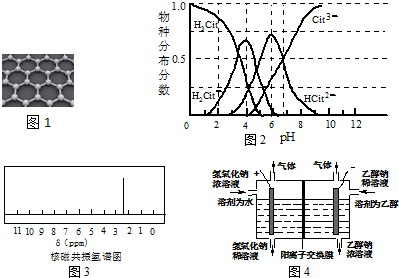
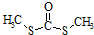 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com