
科目: 來源: 題型:解答題
 氮是重要的非金屬元素,其單質用途之一是制取氨氣,反應方程式為:N2(g)+3H2(g)?2NH3(g):回答下列問題:
氮是重要的非金屬元素,其單質用途之一是制取氨氣,反應方程式為:N2(g)+3H2(g)?2NH3(g):回答下列問題: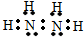 .
.查看答案和解析>>
科目: 來源: 題型:解答題
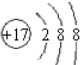 ;
;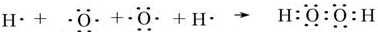 ;
;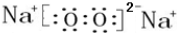 ,該化合物和B與D形成的某化合物反應的化學方程式為:2Na2O2+2CO2=2Na2CO3+O2,lmolH發生該反應轉移電子數為6.02×1023或NA;
,該化合物和B與D形成的某化合物反應的化學方程式為:2Na2O2+2CO2=2Na2CO3+O2,lmolH發生該反應轉移電子數為6.02×1023或NA;查看答案和解析>>
科目: 來源: 題型:填空題
查看答案和解析>>
科目: 來源: 題型:多選題
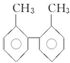
 某分子的球棍模型如圖所示.已知分子中所有原子的最外層均達到 8 電子穩定結構,原子間以單鍵相連.下列有關說法中一定錯誤的是( )
某分子的球棍模型如圖所示.已知分子中所有原子的最外層均達到 8 電子穩定結構,原子間以單鍵相連.下列有關說法中一定錯誤的是( )| A. | X原子可能為第VA族元素 | |
| B. | 該分子中既含有極性共價鍵又含有非極性共價鍵 | |
| C. | Y 原子可能為第ⅠA 族或第ⅦA 族元素元素 | |
| D. | 從圓球的大小分析,該分子可能為 N2F4 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | ①②③⑥ | B. | ②③⑤⑥ | C. | ②③④⑤ | D. | ①③⑤⑥ |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | ①⑥⑦ | B. | ③⑤⑧ | C. | ③⑦⑧ | D. | ③⑥⑦⑧ |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 1molCl2 與過量乙烷在光照下反應,生成的有機物中含有氯原子的總數為2NA | |
| B. | 1molC3H8 中含有的共用電子對數為11NA | |
| C. | 1.5g 甲基含有的質子數和電子數之和為1.8NA | |
| D. | 標況下,11.2 L癸烷含有的原子個數為16 NA |
查看答案和解析>>
科目: 來源: 題型:解答題
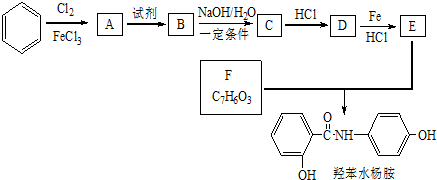
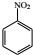 $→_{HCl}^{Fe}$
$→_{HCl}^{Fe}$
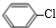 +HNO3$→_{△}^{濃H_{2}SO_{4}}$
+HNO3$→_{△}^{濃H_{2}SO_{4}}$ +H2O.
+H2O.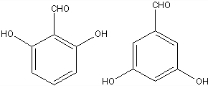 、
、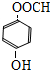 .
.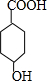 $\stackrel{一定條件下}{→}$
$\stackrel{一定條件下}{→}$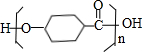 +(n-1)H2O.
+(n-1)H2O.查看答案和解析>>
科目: 來源: 題型:解答題

| 陽離子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
| 開始沉淀時的pH | 2.7 | - | - | - |
| 沉淀完全時的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com