
科目: 來源: 題型:選擇題
| A. | 0.02mol/(L•s) | B. | 1.8mol(L•s) | C. | 1.2mol/(L•s) | D. | 0.18mol/(L•s) |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 決定化學反應速率的主要因素是參加反應的物質的性質 | |
| B. | 催化劑可以使不起反應的物質發生反應 | |
| C. | 升溫可讓吸熱反應加快速率,而會讓放熱反應減慢速率 | |
| D. | 通過增大濃度、升高溫度、增大壓強都可以使反應速率加快 |
查看答案和解析>>
科目: 來源: 題型:實驗題

查看答案和解析>>
科目: 來源: 題型:實驗題
| 實驗序號 | 實驗 | 實驗現象 | 結論 |
| 實驗Ⅱ | 將實驗Ⅰ中收集到的氣體點燃 | 安靜燃燒,火焰呈淡藍色 | 氣體成分為氫氣 |
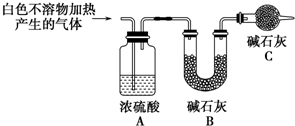
| 實驗Ⅲ | 將實驗Ⅰ中的白色不溶物濾出、洗滌,取少量加入足量稀鹽酸 | 產生氣泡沉淀全部溶解 | 白色不溶物中含有MgCO3 |
| 實驗Ⅳ | 取實驗Ⅲ中的濾液,向其中加入適量CaCl2或BaCl2稀溶液 | 產生白色沉淀,溶液紅色變淺 | 溶液中存在CO${\;}_{3}^{2-}$ |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 46 g鈉與氧氣完全反應生成Na2O和Na2O2,轉移電子數可能為3NA | |
| B. | 向含2 mol FeI2的溶液中通入足量Cl2,消耗氯氣分子數為NA | |
| C. | 2 mol Cu與足量硫粉完全反應,轉移電子數為2NA | |
| D. | 1 mol Al2Fe(SO4)4固體中含Fe3+的數目為NA |
查看答案和解析>>
科目: 來源: 題型:實驗題
查看答案和解析>>
科目: 來源: 題型:選擇題
 某有機物的結構簡式如圖,取Na、NaOH、新制Cu(OH)2分別與等物質的量的該物質恰好反應(反應時可加熱煮沸)則Na、NaOH、新制Cu(OH)2三種物質的物質的量之比為( )
某有機物的結構簡式如圖,取Na、NaOH、新制Cu(OH)2分別與等物質的量的該物質恰好反應(反應時可加熱煮沸)則Na、NaOH、新制Cu(OH)2三種物質的物質的量之比為( )| A. | 6:4:5 | B. | 4:6:5 | C. | 2:3:2 | D. | 2:1:2 |
查看答案和解析>>
科目: 來源: 題型:推斷題
 $→_{FeCl_{3}}^{Cl_{2}}$分離得A$→_{過氧化苯甲酰}^{NBS}$
$→_{FeCl_{3}}^{Cl_{2}}$分離得A$→_{過氧化苯甲酰}^{NBS}$ $\stackrel{NaCN}{→}$B$→_{50%NaOH}^{CH_{3}CHClCH_{3}}$
$\stackrel{NaCN}{→}$B$→_{50%NaOH}^{CH_{3}CHClCH_{3}}$ $→_{②SOCl_{2}}^{①H+}$C
$→_{②SOCl_{2}}^{①H+}$C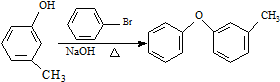 $→_{Co(OAc)_{2}}^{O_{2}}$
$→_{Co(OAc)_{2}}^{O_{2}}$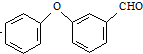 $→_{H+}^{NaCN}$D
$→_{H+}^{NaCN}$D +HCl
+HCl 中的官能團有醚鍵和醛基(填名稱).
中的官能團有醚鍵和醛基(填名稱).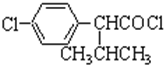 ;合成3中的有機反應類型為取代反應.
;合成3中的有機反應類型為取代反應. .
. )合成一種抗早產藥的重要中間體.根據已有知識并結合相關信息,寫出以CH3Br和
)合成一種抗早產藥的重要中間體.根據已有知識并結合相關信息,寫出以CH3Br和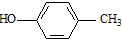 為有機原料(無機試劑和反應條件任選)合成E的路線流程圖.合成路線流程圖示例如下:CH2═CH2$→_{催化劑}^{O_{2}}$CH3CHO$→_{催化劑}^{O_{2}}$CH3COOH.
為有機原料(無機試劑和反應條件任選)合成E的路線流程圖.合成路線流程圖示例如下:CH2═CH2$→_{催化劑}^{O_{2}}$CH3CHO$→_{催化劑}^{O_{2}}$CH3COOH.查看答案和解析>>
科目: 來源: 題型:推斷題
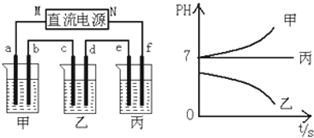
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com