
科目: 來源: 題型:填空題
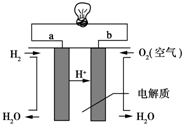 人們應用原電池原理制作了多種電池,以滿足不同的需要.以下每小題中的電池廣泛使用于日常生活、生產和科學技術等方面,請根據題中提供的信息,填寫空格.
人們應用原電池原理制作了多種電池,以滿足不同的需要.以下每小題中的電池廣泛使用于日常生活、生產和科學技術等方面,請根據題中提供的信息,填寫空格.查看答案和解析>>
科目: 來源: 題型:填空題
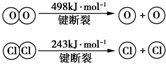 用Cl2生產某些含氯有機物時會產生副產物HCl.利用反應A,可實現氯的循環利用.反應A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反應A中,4mol HCl被氧化,放出115.6kJ的熱量.
用Cl2生產某些含氯有機物時會產生副產物HCl.利用反應A,可實現氯的循環利用.反應A:4HCl+O2$\frac{\underline{\;CuO/CuCl_{2}\;}}{400℃}$Cl2+H2O,已知:反應A中,4mol HCl被氧化,放出115.6kJ的熱量.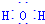 .
.查看答案和解析>>
科目: 來源: 題型:實驗題
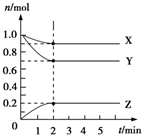 Ⅰ.控制變量法是化學實驗的一種常用方法.如表是某學習小組研究等物質的量濃度的稀硫酸和鋅反應的實驗數據,分析以下數據,回答下列問題:
Ⅰ.控制變量法是化學實驗的一種常用方法.如表是某學習小組研究等物質的量濃度的稀硫酸和鋅反應的實驗數據,分析以下數據,回答下列問題:| 序號 | 硫酸的體積/mL | 鋅的質量/g | 鋅的形狀 | 溫度/℃ | 完全溶于酸的時間/s | 生成硫酸鋅的質量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 顆粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 顆粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 100 mL 2 mol/L鹽酸與鋅反應時,加入100 mL氯化鈉溶液,生成氫氣的速率不變 | |
| B. | 對于可逆反應2CO+2NO?N2+2CO2,使用合適的催化劑,CO的生成速率和消耗速率都加快 | |
| C. | 二氧化硫的催化氧化是一個放熱反應,升高溫度,正反應速率減慢 | |
| D. | 用鐵片和稀硫酸反應制取氫氣時,改用鐵片和濃硫酸可以加快氫氣的產生 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 某些花崗石產生氡($\stackrel{222}{86}$Rn),從而對人體產生傷害,$\stackrel{222}{86}$Rn的質量數是222 | |
| B. | Se是人體必需的微量元素,$\stackrel{78}{34}$Se和$\stackrel{80}{34}$Se互為同位素 | |
| C. | $\stackrel{13}{6}$C-NMR(核磁共振)可用于含碳化合物的結構分析,$\stackrel{13}{6}$C的中子數為6 | |
| D. | 原子結構示意圖 既可以表示16O,也可以表示18O 既可以表示16O,也可以表示18O |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 全部 | B. | ②③④ | C. | ①②④ | D. | ②③④⑤ |
查看答案和解析>>
科目: 來源: 題型:實驗題
溫度/℃ 化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-38 |
查看答案和解析>>
科目: 來源: 題型:實驗題
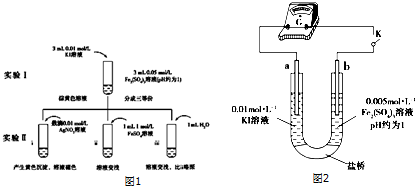
查看答案和解析>>
科目: 來源: 題型:推斷題
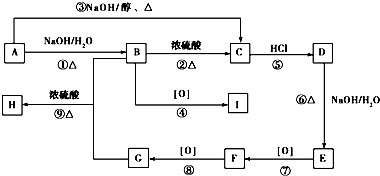
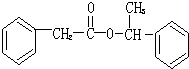 .
. .
. ,用化學方程式表示檢驗 F 中官能團的常用方法
,用化學方程式表示檢驗 F 中官能團的常用方法 .
.查看答案和解析>>
科目: 來源: 題型:填空題
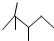 ,有機物 B 與等物質的量的 H2發生加成反應可得到有機物 A.則:
,有機物 B 與等物質的量的 H2發生加成反應可得到有機物 A.則:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com