
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:選擇題
已知1 g氫氣完全燃燒生成液態水時放出熱量143 kJ,18 g水蒸氣變成液態水放出44 kJ的熱量。其他相關數據如下表:
O==O | H—H | H—O(g) | |
1 mol化學鍵斷裂時需要吸收的能量/kJ | 496 | 436 | x |
則表中 x為( )
x為( )
A.920 B.557 C.463 D.188
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:選擇題
硫代硫酸鈉溶液與稀硫酸反應的化學方程式為Na2S2O3+H2SO4==Na2SO4+SO2↑+S↓+H2O,下列各組實驗中最先出現渾濁的是( )
選 項 | 反應溫度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:選擇題
下列說法正確的是( )
A.增大反應物濃度,可增大單位體積內活化分子的百分數,從而增大有效碰撞的次數
B.有氣體參加的化學反應,若增大壓強(即縮小反應容器的體積),可增加活化分子的百分數,從而使反應速率增大
C.升高溫度能使化學反應速率增大,主要原因是增加了反應物分子中活化分子的百分數
D.催化劑不影響反應活化能但能增大單位體積內活化分子的百分數,從而增大反 應速率
應速率
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:選擇題
足量塊狀鐵與100 mL 0.01 mol/L的稀硫酸反應,反應速率太慢。為了加快此反應速率而不改變H2的產量,可以使用如下方法中的( )。
①加H2O②加NaOH固體③加CH3COONa固體
④加Na2CO3固體⑤加入NaNO3固體⑥加NaCl溶液
⑦滴入幾滴硫酸銅溶液⑧升高溫度⑨將塊狀鐵改為鐵粉
⑩將稀硫酸改用98%的濃硫酸
A.⑧⑨⑩ B.⑦⑧⑨ C.③⑦⑩ D.⑦⑧⑩
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:選擇題
為了應對能源危機,滿足不斷增大的能源需求,當今國際能源研究的另一熱點就是尋找新能源,下列有關新能源的敘述不正確的是( )
A.氫能燃燒熱值高,資源豐富,無毒,無污染
B.風能是太陽能的一種轉換形式,能量巨大
C.世界上地熱能蘊藏豐富,且已被用于采暖、溫室、發電等方面
D.太陽能能量巨大,取之不盡,用之不竭,而且清潔、無污染,但需要開采、運輸
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:選擇題
下列說法正確的是( )
A.人們把能夠發生有效碰撞的分子叫做活化分子,同時把活化分子具有的能量叫活化能
B.化學反應不一定都有能量變化
C.活化能接近于零的反應,當反應物相互接觸時,反應瞬間完成,而且溫度對其反應速率幾乎沒有什么影響
D.活化能的大小不僅意味著一般分子成為活化分子的難易,也會對化學反應前后的能量變化產生影響
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:填空題
CH4、H2、C都是優質的能源物質,它們燃燒的熱化學方程式為:
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
(1)在深海中存在一種甲烷細菌,它們依靠酶使甲烷與O2作用產生的能量存活,甲烷細菌使1 mol甲烷生成CO2氣體與液態水,放出的能量____________(填“>”“<”或“=”)890.3 kJ。
(2)甲烷與CO2可用于合成合成氣(主要成分是一氧化碳和氫氣):CH4+CO2=2CO+2H2,1 g CH4完全反應可釋放15.46 kJ的熱量,則:
①能表示該反應過程中能量變化的是____________(填字母)。
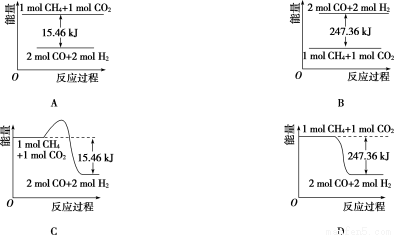
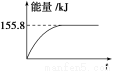
②若將物質的量均為1 mol的CH4與CO2充入某恒容密閉容器中,體系放出的熱量隨著時間的變化如圖所示,則CH4的轉化率為____________。
(3)C(s)與H2(g)不反應,所以C(s)+2H2(g)=CH4(g)的反應熱無法直接測量,但通過上述反應可求出C(s)+2H2(g)=CH4(g)的反應熱ΔH=____________。
(4)目前對于上述三種物質的研究是燃料研究的重點,下列關于上述三種物質的研究方向中可行的是_______________(填字母)。
A.尋找優質催化劑,使CO2與H2O反應生成CH4與O2,并放出熱量
B.尋找優質催化劑,在常溫常壓下使CO2分解生成碳與O2
C.尋找優質催化劑,利用太陽能使大氣中的CO2與海底開采的CH4合成合成氣(C O、H2)
O、H2)
D.將固態碳合成為C60,以C60作為燃料
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:填空題
研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義。
(1 )一定溫度下,在2L的密閉容器中,SO2、O2、SO3三種氣體的物質的量隨時間變化的曲線如下圖所示,請回答下列問題:
)一定溫度下,在2L的密閉容器中,SO2、O2、SO3三種氣體的物質的量隨時間變化的曲線如下圖所示,請回答下列問題:
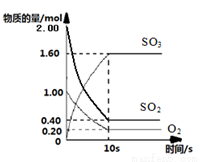
①反應的化學方程式為
②反應開始到10s,用SO2表示的反應速率為
③O2的平衡轉化率為
(2)對于反應:2SO2(g)+O2(g) 2SO3(g),當反應達到平衡時,如果反應速率υ(SO2)為0.05 mol·L-1·min-1,則υ(O2)= ;υ(SO3)= 。
2SO3(g),當反應達到平衡時,如果反應速率υ(SO2)為0.05 mol·L-1·min-1,則υ(O2)= ;υ(SO3)= 。
(3)已知:2SO2(g)+O2(g) 2SO3(g)ΔH=-196.6kJ·mol-1
2SO3(g)ΔH=-196.6kJ·mol-1
2NO(g)+O2(g) 2NO2(g)ΔH=-113.0kJ·mol-1
2NO2(g)ΔH=-113.0kJ·mol-1
則反應NO2(g)+SO2(g)  SO3(g)+NO(g)的ΔH=_________kJ·mol-1。
SO3(g)+NO(g)的ΔH=_________kJ·mol-1。
(4)一定條件下,將NO2與SO2以體積比1:2置于密閉容器中發生上述反應,下列能說明反應達到平衡狀態的是_________
a、體系壓強保持不變 b、混合氣體顏色保持不變
c、SO3和NO的體積比保持不變 d、每消耗1 mol SO3的同時生成1 mol NO2
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:實驗題
某實驗小組用0.50 mol·L-1NaOH溶液和0.50 mol·L-1硫酸溶液進行中和熱的測定。
Ⅰ.配制0.50 mol·L-1NaOH溶液
(1)若實驗中大約要使用245mLNaOH溶液,至少需要稱量NaOH固體 g。
(2)從下圖中選擇稱量NaOH固體所需要的儀器是(填字母): 。
名稱 | 托盤天平 (帶砝碼) | 小燒杯 | 坩堝鉗 | 玻璃棒 | 藥匙 | 量筒 |
儀器 |
|
|
|
|
|
|
序號 | a | b | c | d | e | f |
Ⅱ.測定稀硫酸和稀氫氧化鈉中和熱的實驗裝置如圖所示。
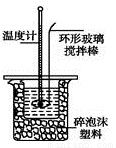
(1)不能用銅絲攪拌棒代替環形玻璃攪拌棒的理由是 。
(2)在操作正確的前提下,提高中和熱測定準確性的關鍵是_____________。大燒杯如不蓋硬紙板,求得的中和熱數值將 (填“偏大”、“偏小”或“無影響”)。結合日常生活實際該實驗在 中(家用產品)效果更好。
(3)寫出該反應中和熱的熱化學方程式:(中和熱為57.3 kJ·mol-1) 。
(4)取50 mLNa OH溶液和30 mL硫酸溶液進行實驗,實驗數據如下表。
OH溶液和30 mL硫酸溶液進行實驗,實驗數據如下表。
試驗次數 | 起始溫度t1/℃ | 終止溫度 t2/℃ | 溫度差平均值 (t2-t1)/℃ | ||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 29.6 | |
2 | 27.0 | 27.4 | 27.2 | 31.2 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
①表中的溫度差平均值為 ℃。
②近似認為0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比熱容c = 4.18 J·(g·℃)-1。則中和熱ΔH= (取小數點后一位)。
③上述實驗數值結果與57.3 kJ·mol-1有偏差,產生偏差的原因可能是(填字母) 。
a.實驗裝置保溫、隔熱效果差
b.量取NaOH溶液的體積時仰視讀數
c.分多次把NaOH溶液倒入盛有硫酸的小燒杯中
d.用溫度計測定NaOH溶液起始溫度后直接測定H2SO4溶液的溫度
④實驗中改用60mL0.5mol/L鹽酸跟50mL0.55 mol·L-1氫氧化鈉進行反應,與上述實驗相比,所放出的熱量 (填相等或不相等,下同),所求的中和熱無偏差時 簡述理由 。
查看答案和解析>>
科目: 來源:2016-2017學年天津市高二上9月調研化學試卷(解析版) 題型:填空題
某同學在用稀硫酸與鋅制取氫氣的實驗中,發現加入少量硫酸銅溶液可加快氫氣的生成速率。請回答下列問題:
(1)上述實驗中發生反應的化學方程式有________________________;
(2)硫酸銅溶液可以加快氫氣生成速率的原因是_______________________;
(3)實驗室中現有Na2SO4、MgSO4、Ag2SO4、K2SO4等4種溶液,可與上述實驗中CuSO4溶液起相似作用的是____________;
(4)要加快上述實驗中氣體產生的速率,還可采取的措施有______________(答兩種);
(5)為了進一步研究硫酸銅的量對氫氣生成速率的影響,該同學設計了如下一系列的實驗。將表中所給的混合溶液分別加入到6個盛有過量Zn粒的反應瓶中,收集產生的氣體,記錄獲得相同體積的氣體所需的時間。
實驗 混合溶液 | A | B | C | D | E | F |
4mol·L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
飽和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①請完成此實驗設計,其中:V1=_________,V6=________,V9=________。
②反應一段時間后,實驗A中的金屬呈________色,實驗E中的金屬呈________色;
③該同學最后得出的結論為:當加入少量CuSO4溶液時,生成氫氣的速率會大大提高,但當加入的CuSO4溶液超過一定量時,生成氫氣的速率反而會下降。請分析氫氣生成速率下降的主要原因______________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com