
科目: 來源: 題型:解答題
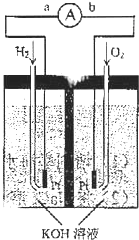 氫氧燃料電池是符合綠色化學理念的新型發電裝置.下圖為電池示意圖,該電池電極表面鍍一層細小的鉑粉,附氣體的能力強,性質穩定,請回答:
氫氧燃料電池是符合綠色化學理念的新型發電裝置.下圖為電池示意圖,該電池電極表面鍍一層細小的鉑粉,附氣體的能力強,性質穩定,請回答:查看答案和解析>>
科目: 來源: 題型:選擇題
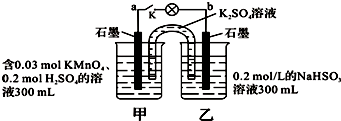
| A. | 當電路中有1.204×1022個電子轉移時,乙燒杯中溶液的C(H+)約為0.1 mol•L-1 | |
| B. | 電池工作時,鹽橋中的K+移向甲燒杯 | |
| C. | 電池工作時,外電路的電子方向是從a到b | |
| D. | 乙池中的氧化產物為SO42- |
查看答案和解析>>
科目: 來源: 題型:選擇題
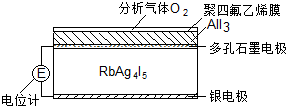 固體電解質是具有與強電解質水溶液的導電性相當的一類無機固體.這類固體通過其中的離子遷移進行電荷傳遞,因此又稱為固體離子導體.目前固體電解質在制造全固態電池及
固體電解質是具有與強電解質水溶液的導電性相當的一類無機固體.這類固體通過其中的離子遷移進行電荷傳遞,因此又稱為固體離子導體.目前固體電解質在制造全固態電池及| A. | 4AlI3+3O2=2Al2O3+6I2 | B. | I2+2Ag++2e-=2AgI | ||
| C. | Ag-e-=Ag+ | D. | I2+2Rb++2e-=2RbI |
查看答案和解析>>
科目: 來源: 題型:解答題
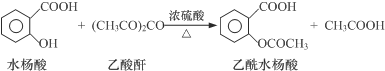
| 試劑 | 沸點(℃) | 溶解度 | 化學性質 |
| 水楊酸 | 211 | 微溶于冷水,易溶于熱水 | |
| 乙酸酐 | 139 | 在水中逐漸分解 | |
| 乙酰水楊酸 | 微溶于水 | 與碳酸鈉反應生成水溶性鹽 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| t/min | 0 | 2 | 4 | 6 |
| n(Cl2)/10-3 mol | 0 | 1.8 | 3.7 | 5.4 |
| A. | 0~2 min的反應速率小于4~6 min的反應速率 | |
| B. | 2~6 min用Cl2表示的反應速率為0.9 mol/(L•min) | |
| C. | 增大壓強可以提高HCl轉化率 | |
| D. | 平衡常數K(200℃)<K(400℃) |
查看答案和解析>>
科目: 來源: 題型:解答題
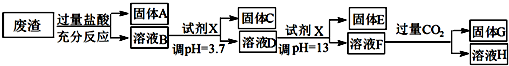
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| pH | 3.4 | 5.2 | 11 |
查看答案和解析>>
科目: 來源: 題型:解答題

查看答案和解析>>
科目: 來源: 題型:解答題
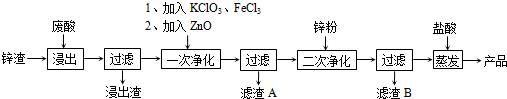
查看答案和解析>>
科目: 來源: 題型:選擇題
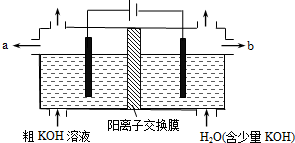 ( )
( )| A. | 陽極反應式為4OH--4e-=2H2O+O2↑ | B. | 通電后陰極區附近溶液pH會增大 | ||
| C. | K+通過交換膜從陰極區移向陽極區 | D. | 純凈的KOH溶液從b出口導出 |
查看答案和解析>>
科目: 來源: 題型:解答題
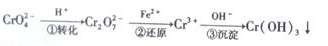
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com