
科目: 來源: 題型:選擇題
| A. | 原子半徑:Na>Al | |
| B. | 若把鋁鈉合金投入一定量的水中只得到無色溶液,則n(Al)≤n(Na) | |
| C. | m g不同組成的鋁鈉合金投入足量鹽酸中,若放出H2越多,則鋁的質量分數越小 | |
| D. | 鋁鈉合金投入到足量氯化銅溶液中,肯定有氫氧化銅沉淀生成 |
查看答案和解析>>
科目: 來源: 題型:解答題

| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
查看答案和解析>>
科目: 來源: 題型:解答題
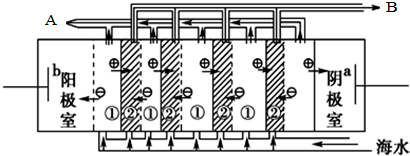 ,電滲陰極室可獲得的重要化工原料有氫氣、氫氧化鈉.
,電滲陰極室可獲得的重要化工原料有氫氣、氫氧化鈉.| CaSO4 | CaCO3 | BaSO4 | BaCO3 |
| 2.6×10-2 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 反應A(g)?2B(g)△H,若正反應的活化能為Ea kJ•mol-1,逆反應的活化能為Eb kJ•mol-1,則△H=-(Ea-Eb)kJ•mol-1 | |
| B. | 某溫度下,氯化鈉在水中的溶解度是20g,則該溫度下的飽和氯化鈉溶液溶質的質量分數為20% | |
| C. | 將濃度為0.1 mol•L-1HF溶液加水不斷稀釋過程中,電離平衡常數Ka(HF)保持不變,$\frac{{c({F^-})}}{{c({H^+})}}$始終保持增大 | |
| D. | 將0.2 mol•L-1的CH3COOH溶液與0.1 mol•L-1的NaOH溶液等體積混合后,溶液中有關粒子的濃度滿足下列關系:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
查看答案和解析>>
科目: 來源: 題型:選擇題
| 選項 | 實驗操作 | 現象 | 結論 |
| A | 廢FeCl3蝕刻液中加入少量鐵粉、振蕩 | 得到澄清溶液 | 蝕刻液中一定不含Cu2+ |
| B | 將Fe(NO3)2樣品溶于稀H2SO4,滴加KSCN溶液 | 溶液變紅 | 稀硫酸能氧化Fe2+ |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2,充分振蕩,靜置 | 有機相呈現橙色 | 氧化性:Cl2>Br2 |
| D | 葡萄糖溶液與新制Cu(OH)2混合加熱 | 生成磚紅色沉淀 | 葡萄糖分子中含有醛基 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 來源: 題型:選擇題
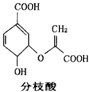
| A. | 可與乙醇、乙酸反應,且反應類型相同 | |
| B. | 1 mo1分枝酸最多可與3 mol NaOH發生中和反應 | |
| C. | 分枝酸的分子式為C10H8O6 | |
| D. | 分枝酸分子中含有2種官能團 |
查看答案和解析>>
科目: 來源: 題型:解答題
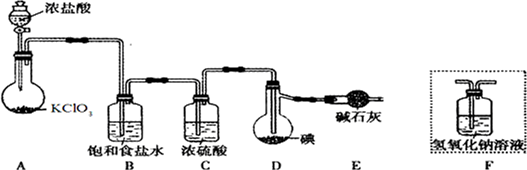
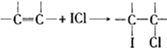
查看答案和解析>>
科目: 來源: 題型:解答題
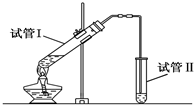 實驗室用如圖所示裝置制備少量乙酸乙酯.
實驗室用如圖所示裝置制備少量乙酸乙酯. .
.查看答案和解析>>
科目: 來源: 題型:解答題
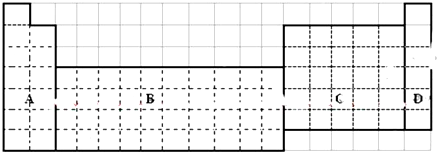
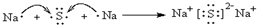 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com