
科目: 來源: 題型:選擇題
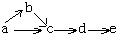 a、b、c、d、e五種物質均含有一種相同的元素,在一定條件下可發生如圖所示轉化,其中a 是單質;b在通常狀況下是氣體; c、d都是氧化物;e是該元素的最高價
a、b、c、d、e五種物質均含有一種相同的元素,在一定條件下可發生如圖所示轉化,其中a 是單質;b在通常狀況下是氣體; c、d都是氧化物;e是該元素的最高價| A. | N2 | B. | C12 | C. | Si | D. | C |
查看答案和解析>>
科目: 來源: 題型:多選題
| A. | 離子半徑:K+>Cl->Na+>F- | B. | 酸性:H2SO4>H3PO4>H2CO3>H2SiO3 | ||
| C. | 熔點:石英>食鹽>鉀>干冰 | D. | 還原性:NaCl>NaBr>NaI>Na2S |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 若2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,則H2燃燒熱為241.8 kJ•mol-1 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若將含0.6 mol H2SO4的稀硫酸與含1 mol NaOH的溶液混合,放出的熱量大于57.3 kJ | |
| C. | 已知C(石墨,s)═C(金剛石,s)△H>0,則金剛石比石墨穩定 | |
| D. | 由BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H1=+571.2kJ•mol-1①BaSO4(s)+2C(s)═2CO2(g)+BaS(s)△H2=+226.2kJ•mol-1②可得反應C(s)+CO2(g)═2CO(g) 的△H=+172.5kJ•mol-1 |
查看答案和解析>>
科目: 來源: 題型:選擇題
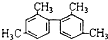 的烴,下列說法正確的是( )
的烴,下列說法正確的是( )| A. | 分子中至少有9個碳原子處于同一平面上 | |
| B. | 分子中至少有11個碳原子處于同一平面上 | |
| C. | 該有機物不能使酸性KMnO4溶液褪色 | |
| D. | 該烴屬于苯的同系物 |
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | X與Y形成原子個數比1:1的化合物只有2種 | |
| B. | Y、W的氧化物均為酸性氧化物 | |
| C. | 最高價氧化物對應水化物的酸性:Y<W | |
| D. | X與Z形成的化合物中,各原子均滿足8電子穩定結構 |
查看答案和解析>>
科目: 來源: 題型:解答題
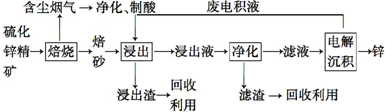
查看答案和解析>>
科目: 來源: 題型:選擇題
| A. | 離子半徑:丁>丙>乙 | |
| B. | 81號元素鉈與丙元素處同主族,則鉈的最高價氧化物對應水化物呈兩性 | |
| C. | 電解法可以用乙與丙形成的化合物制得丙單質 | |
| D. | 同周期元素中丁的最高價氧化物對應水化物的酸性最強 |
查看答案和解析>>
科目: 來源: 題型:解答題
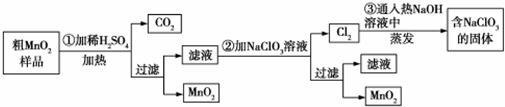
查看答案和解析>>
科目: 來源: 題型:解答題
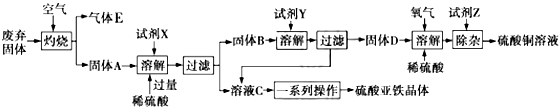
查看答案和解析>>
科目: 來源: 題型:解答題
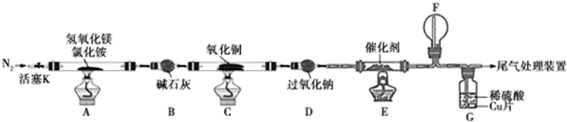
| 實驗步驟 | 預期現象和結論 |
| 步驟1:取裝置C中反應后的少許固體于試管中 | \ |
| 步驟2:向試管中加入2mol/LH2SO4溶液 | 液中出現藍色,說明紅色固體中含有Cu2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com