
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | �_�l�����|�������ʯȼ�� | B�� | ��߿��ŷŽ���ұ���a���ķۉm | ||
| C�� | �ô��D�����g̎����܇β�� | D�� | �����ƏV���a��ʹ�ßo������ |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}

�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
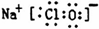 ��
���鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
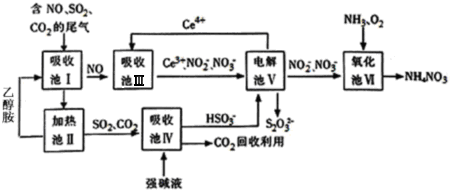
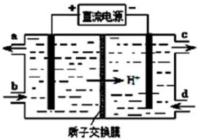
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
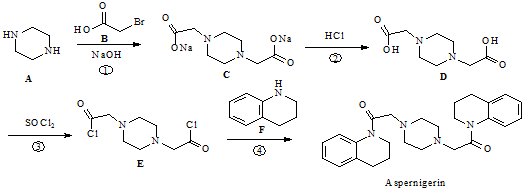
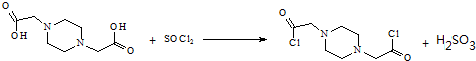 ��
��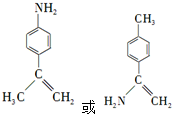 ��
��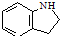 ��ԭ�ϣ������������P��Ϣ�������Ƃ�
��ԭ�ϣ������������P��Ϣ�������Ƃ�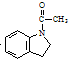 �ĺϳ�·�����̈D���o�Cԇ�����ã����ϳ�·�����̈D�����£�CH2�TCH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH
�ĺϳ�·�����̈D���o�Cԇ�����ã����ϳ�·�����̈D�����£�CH2�TCH2$\stackrel{HBr}{��}$CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH ��
���鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
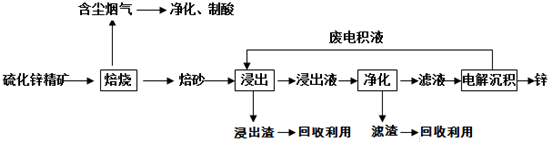
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
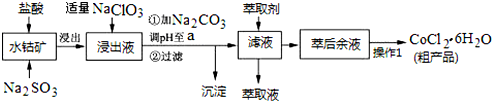
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| �_ʼ���� | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| ��ȫ���� | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
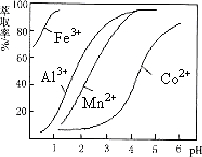
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
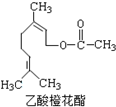 ijʳ����������Ȼ����ĽY����ʽ��D��ʾ���P��ԓ�ЙC������Д��������_���ǣ�������
ijʳ����������Ȼ����ĽY����ʽ��D��ʾ���P��ԓ�ЙC������Д��������_���ǣ�������| A�� | �٢ڢ� | B�� | �٢ڢ� | C�� | �٢ڢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ��x���}
| A�� | SiO2����ˮ���@���� | |
| B�� | �cȼ��H2��Cl2���ϵ�Ωһ�l�� | |
| C�� | SiO2���������������������� | |
| D�� | Һ�Ⱥ���ˮ����ͬһ���| |
�鿴�𰸺ͽ���>>
��Ŀ�� ��Դ�� �}�ͣ�����}
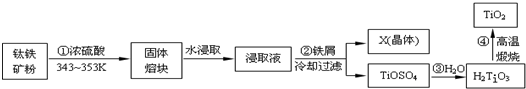
�鿴�𰸺ͽ���>>
����ʡ���W�`���Ͳ�����Ϣ�e��ƽ�_ | �W���к���Ϣ�e�^ | ����p�_�e�^ | ��vʷ̓�o���x�к���Ϣ�e�^ | �����֙��e�^
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com