
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:選擇題
某溫度下,Fe(OH)3(s)、Cu(OH)2(s)分別在溶液中達到沉淀溶解平衡后,改變溶液pH,金屬陽離子濃度的變化如圖所示。據圖分析,下列判斷錯誤的是
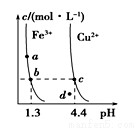
A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2]
B.加適量NH4Cl固體可使溶液由a點變到b點
C.c 、d兩點代表的溶液中c(H+)與c(OH-)乘積相等
D.Fe(OH)3、Cu(OH)2分別在b、c兩點代表的溶液中達到飽和
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:選擇題
下列說法中正確的是
A.常溫下,稀釋0.1 mol·L-1的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均下降
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.常溫下,c(NH4+)相等的①(NH4)2SO4 ②(NH4)2Fe(SO4)2 ③NH4Cl ④(NH4)2CO3溶液中,溶質物質的量濃度大小關系是:②<①<④<③
D.當溶液中存在的離子只有Cl-、OH-、NH4+、H+時,該溶液中離子濃度大小關系可能為c(Cl-)>c(NH4+)>c(OH-)>c(H+)
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:選擇題
室溫下,將1.000mol/L鹽酸滴入20.00mL1.000mol/L氨水中,溶液pH和溫度隨加入鹽酸體積變化曲線如下圖所示。下列有關說法正確的是

A.a點由水電離出的c(H+)=1.0×10-14mol/L
B.b點時c(NH4+)+c(NH3·H2O)=c(Cl-)
C.c點時消耗的鹽酸體積:V(HCl)<20.00mL
D.d點后,溶液溫度略下降的主要原因是NH3·H2O電離吸熱
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:選擇題
如下圖裝置,在盛有水的燒杯中,鐵圈和銀圈的相接處吊著一根絕緣的細絲,使之平衡,小心地從燒杯中央滴入CuSO4溶液,片刻后可觀察到的現象是(指懸吊的金屬圈)
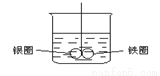
A.鐵圈和銀圈左右搖擺不定
B.保持平衡狀態不變
C.鐵圈向下傾斜
D.銀圈向下傾斜
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:選擇題
把a、b、c、d四塊金屬片浸入稀硫酸,分別用導線兩兩連接,可以組成原電池。a、b相連時,a為負極;c、d相連時,電流方向為d→c;a、c相連時,c極產生大量氣泡;b、d相連時,d極上發生氧化反應。這四種金屬的活動性由強到弱的順序是
A.a b c d B.a c d b C.c a b d D.b d c a
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:選擇題
一種燃料電池,一極通入空氣,另一極通入丁烷(C4H10)氣體;電解質是摻雜氧化釔(Y2O3)的氧化鋯(ZrO2)晶體,在熔融狀態下能傳導O2-。下列對該燃料說法正確的是
A.在熔融電解質中,O2-由負極移向正極
B.放電時每轉移4 mol電子,正極有1mol O2被氧化
C.通入空氣的一極是正極,電極反應為:O2 + 4e- = 2O2-
D.通入丁烷的一極是正極,電極反應為:C4H10 + 26e- + 13O2 = 4CO2 + 5H2O
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:選擇題
某原電池裝置如下圖所示,電池總反應為2Ag+Cl2===2AgCl 。下列說法正確的是

A.正極反應為AgCl+e-===Ag+Cl-
B.放電時,交換膜右側溶液中有大量白色沉淀生成
C.若用NaCl溶液代替鹽酸,則電池總反應隨之改變
D.當電路中轉移0.01 mol e-時,交換膜左側溶液中約減少0.02 mol離子
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:填空題
隨原子序數遞增,八種短周期元素(用字母x等表示)原子半徑的相對大小、最高正價或最低負價的變化如下圖所示。
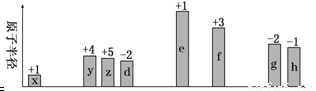
根據判斷出的元素回答問題:
(1)f在周期表中的位置是 。
(2)比較d、e常見離子的半徑大小(用化學式表示,下同):__________________;比較g 、h的最高價氧化物對應水化物的酸性強弱:____________________。
(3)任選上述元素組成一種四原子共價化合物,寫出其電子式:____________________。
(4)已知1mol e的單質在足量d2中燃燒,恢復至室溫,放出255.5 kJ熱量,寫出該反應的熱化學方程式:_____________________________________________________。
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:填空題
醋酸是一種常見的弱酸,回答下列問題:
(1)醋酸的電離方程式是 ;下列哪些措施能夠使醋酸溶液中c(H+) / c(CH3COO-) 增大的是 。
a.升溫 b.通入HCl氣體 c.加入NaOH固體 d.加入NaHSO4固體
(2)向100ml 0.1mol·L-1的醋酸中加入Vml0.1mol·L-1的NaOH溶液完全反應后,溶液呈中性,則V 100ml( 填“>”,“<”或“=” )。
(3)在CH3COOH與CH3COONa的混合溶液中,測得某一時刻混合溶液中:c(CH3COO-) / c(CH3COOH) = 18,則此時溶液的pH = 。(已知:CH3COOH的電離常數Ka=1.8×10-5)
(4)為測定食用醋中醋酸含量(用每升食醋中所含醋酸的質量表示,單位:g/L),設計如下實驗:a.取20ml食醋于錐形瓶中,滴加2—3滴酚酞作指示劑。b.向堿式滴定管中加入1mol·L-1的NaOH溶液,調整液面,并記下初始刻度。c.開始滴定,并記錄滴定終點時堿式滴定管的刻度,重復試驗2—3次。
① 達到滴定終點時的現象是_______________________。
② 經過測定,消耗NaOH溶液的體積為10mL,則該食醋中醋酸的含量是 。
③ 以下哪些操作會導致測定的結果偏低________(填字母編號)。
a.裝入NaOH溶液前未潤洗滴定管
b.滴定結束后俯視讀數
c.滴定結束后,滴定管尖端部分有氣泡
查看答案和解析>>
科目: 來源:2015-2016學年內蒙古高一下期末化學試卷(解析版) 題型:填空題
根據下列原電池的裝置圖,回答問題:

(1)若C為稀H2SO4溶液,電流表指針發生偏轉,B電極材料為Fe且做負極,則A電極上發生的電極反應式為____________________;反應進行一段時間后溶液C的pH將________(填“升高”“降低”或“基本不變”)。
(2)若需將反應:Cu+2Fe3+===Cu2++2Fe2+設計成如上圖所示的原電池裝置,則負極A極材料為 ,正極B極材料為 ,溶液C為 。
(3)用CH4和O2組合形成的質子交換膜燃料電池的結構示意圖如下:

①則d電極是________(填“正極”或“負極”),c電極的反應方程式為:_____ 。
②若線路中轉移2 mol電子,則上述燃料電池,消耗的O2在標況下的體積為______ L。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com