
科目: 來源: 題型:
| 物質 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸點(℃) | 56.2 | 77.06 | 78 | 117.9 |
查看答案和解析>>
科目: 來源: 題型:

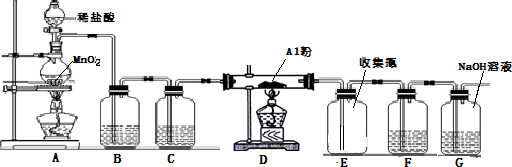
查看答案和解析>>
科目: 來源: 題型:
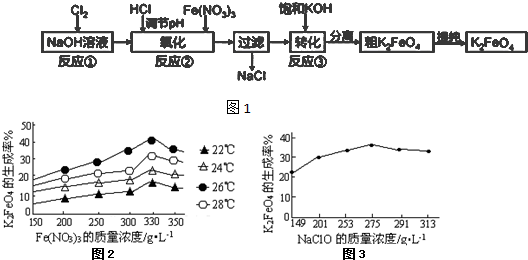
查看答案和解析>>
科目: 來源: 題型:
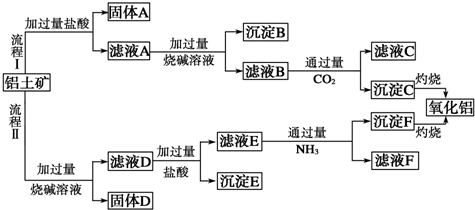
查看答案和解析>>
科目: 來源: 題型:
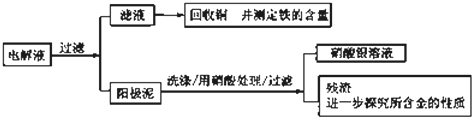
| 序號 | 反應 | 平衡常數 |
| 1 | Au+6HNO3?Au(NO3)3+3NO2↑+3H20 | <<1 |
| 2 | Au3++4Cl-?AuCl4 _ | >>1 |
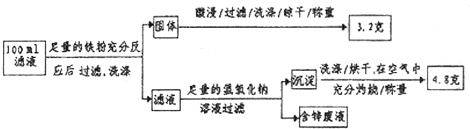
查看答案和解析>>
科目: 來源: 題型:
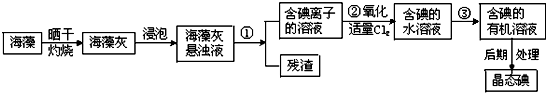
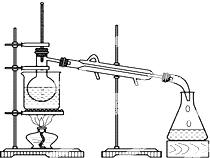
查看答案和解析>>
科目: 來源: 題型:
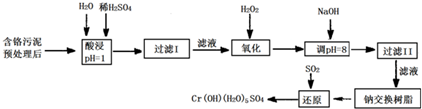
| 氫氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
科目: 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com