
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
NOx是汽車尾氣中的主要污染物之一。通過NOx傳感器可監測NOx的含量,其工作原理示意圖如下。下列說法正確的是
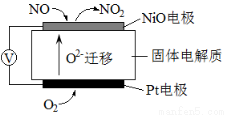
A.Pt電極作負極,NiO電極作正極
B.Pt電極上發生的是氧化反應
C.NiO電極上發生的是還原反應
D.NiO電極的電極反應式為NO+O2–-2e–=NO2
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
下列解釋事實的反應方程式正確的是
A.氨水使酚酞溶液變紅:NH4+ + H2O NH3·H2O + H+
NH3·H2O + H+
B.向FeCl3溶液中加入Mg(OH)2,溶液中有紅褐色沉淀生成:3Mg(OH)2+2Fe3+=2Fe(OH)3+3Mg2+
C.鉛蓄電池放電時的正極反應為:PbO2+2e–+4H+=Pb2++2H2O
D.鋼鐵的析氫腐蝕與吸氧腐蝕的負極電極反應相同:Fe-3e–=Fe3+
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.KClO3和SO3溶于水后均能導電,故KClO3和SO3都是電解質
B.常溫下將pH=4的醋酸溶液稀釋后,溶液中所有離子的濃度均降低
C.常溫下,等濃度的Na2S與NaHS溶液相比,Na2S溶液的pH大
D.25℃時,用pH=3的鹽酸滴定等濃度的氨水至溶液的pH=7,V(氨水)<V(鹽酸)
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
常溫下,在c(H+)/c(OH?)=1×1012的溶液中,下列各組離子能大量共存的是
A.Fe2+、Mg2+、NO3?、SO42? B.Fe3+、Na+、Cl?、SCN?
C.NH4+、Al3+、NO3?、Cl? D.Ca2+、K+、Cl?、HCO3?
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
下列實驗操作導致所讀出數值比真實值小的是(假設其他操作均正確)
A.對滴定管仰視讀數:18.80 mL
B.用蒸餾水潤濕pH試紙測定某濃度的硫酸溶液的pH=5
C.用量筒量取飽和食鹽水時,俯視讀數:8.8 mL
D.中和熱測定時,用銅棒代替環形玻璃攪拌棒攪拌,測定反應的最高溫度:38.8℃
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
取五等份NO2 ,分別加入溫度不同、容積相同的恒容密閉容器中,發生反應:2NO2(g) N2O4(g) ΔH<0 反應相同時間后,分別測定體系中NO2的百分量(NO2%),并作出其隨反應溫度(T)變化的關系圖。下列示意圖中,可能與實驗結果相符的是
N2O4(g) ΔH<0 反應相同時間后,分別測定體系中NO2的百分量(NO2%),并作出其隨反應溫度(T)變化的關系圖。下列示意圖中,可能與實驗結果相符的是

A.②④ B.② C.①② D.③④
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
中和滴定是一種操作簡單,準確度高的定量分析方法。實際工作中也可以利用物質間的氧化還原反應、沉淀反應進行類似的滴定分析,這些滴定分析均需要通過指示劑來確定滴定終點,下列對幾種具體的滴定分析(待測液置于錐形瓶內)中所用指示劑及滴定終點時的溶液顏色的判斷不正確的是
A.用標準NaOH溶液滴定鹽酸溶液以測定其濃度:酚酞試液——淺紅色
B.用標準FeCl3溶液滴定KI以測定其濃度:淀粉溶液——藍色
C.用標準酸性KMnO4溶液滴定Na2SO3溶液以測定其濃度:KMnO4溶液——紫紅色
D.利用“Ag++SCN-=AgSCN↓”原理,用標準KSCN溶液滴定AgNO3溶液以測定其濃度:FeCl3溶液——紅色
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:選擇題
常溫下,用0.1000mol/LNaOH溶液分別滴定25.00mL0.1000mol/L鹽酸溶液和
25.00mL0.1000mol/LCH3COOH溶液,滴定過程中pH變化曲線如下圖所示。下列判斷不正確的是
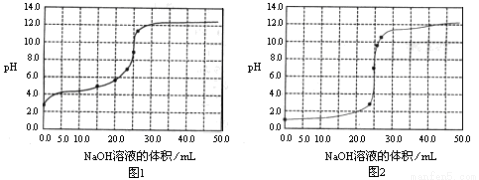
A.滴定鹽酸的pH變化曲線為圖2
B.在滴定CH3COOH溶液的過程中,始終都有c(Na+)+ c(H+)=c(CH3COO–)+c(OH–)
C.滴定CH3COOH溶液的過程中,當滴加12.5mLNaOH溶液時,溶液中離子濃度由大到小的順序為c(CH3COO–)>c(Na+)>c(H+)>c(OH–)
D.當c(Na+)=c(CH3COO–)+ c(CH3COOH)時,溶液的pH<7
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:填空題
研究NO2、SO2、CO等大氣污染氣體的處理具有重要意義。
(1)利用反應:6NO2+8NH3 7N2+12H2O可處理NO2。當轉移1.2mol電子時,消耗的NO2在標準狀況下的體積是 L。
7N2+12H2O可處理NO2。當轉移1.2mol電子時,消耗的NO2在標準狀況下的體積是 L。
(2)①已知:2SO2(g)+O2(g) 2SO3(g) ΔH=?196.6 kJ·mol–1
2SO3(g) ΔH=?196.6 kJ·mol–1
2NO(g)+O2(g) 2NO2(g) ΔH=?113.0 kJ·mol–1
2NO2(g) ΔH=?113.0 kJ·mol–1
請寫出NO2與SO2反應生成SO3(g)和NO的熱化學方程式 。
②一定條件下,將NO2與SO2以體積比1:2置于密閉容器中發生上述反應,下列能說明反應達到平衡狀態的是 。
a.體系壓強保持不變 b.混合氣體顏色保持不變
c.SO3和NO的體積比保持不變 d.每消耗1 mol SO2的同時生成1 molNO2
③測得上述反應平衡時NO2與SO2體積比為1:6,則該反應的平衡常數K= 。
(3)汽車尾氣中的一氧化碳可通過如下反應降低其濃度:CO(g)+1/2O2(g) CO2(g)。已知某溫度下,在兩個恒容密閉容器中進行該反應,容器中各物質的起始濃度及正、逆反應速率關系如下表所示。請用“>”或“<”或“=”填寫表中的空格。
CO2(g)。已知某溫度下,在兩個恒容密閉容器中進行該反應,容器中各物質的起始濃度及正、逆反應速率關系如下表所示。請用“>”或“<”或“=”填寫表中的空格。
容器編號 | c(CO)/mol·L–1 | c(O2)/mol·L–1 | c(CO2)/mol·L–1 | υ(正)和υ(逆) 大小比較 |
① | 2.0×10–4 | 4.0×10–4 | 4.0×10–4 | υ(正)=υ(逆) |
② | 1.0×10–3 | 4.0×10–4 | 5.0×10–4 | υ(正) υ(逆) |
查看答案和解析>>
科目: 來源:2015屆湖北省三校高二上學期期末聯考化學試卷(解析版) 題型:填空題
某同學用工業硫酸銅(含硫酸亞鐵等雜質)制備純凈的CuSO4·5H2O。工藝流程如下
(部分操作和條件略):
I.取工業硫酸銅固體,用稀硫酸溶解,過濾。
II.向濾液中滴加H2O2溶液,稍加熱。
III.向II的溶液中加入CuO粉末至pH=4。
IV.加熱煮沸,過濾,濾液用稀硫酸酸化至pH=1。
V.蒸發濃縮、冷卻結晶、過濾、洗滌、干燥,得晶體。
已知部分陽離子生成氫氧化物的pH、Ksp(25℃)如下表:
物質 | Fe(OH)3 | Fe (OH)2 | Cu(OH)2 |
開始沉淀時pH | 2.7 | 7.6 | 4.7 |
完全沉淀時pH | 3.7 | 9.6 | 6.7 |
Ksp | 4.0×10–38 | 8.0×10–16 | 2.2×10–20 |
(1)II中發生反應的離子方程式是 。
(2)II中將Fe2+氧化為Fe3+的目的是 。
(3)用K3[Fe(CN)6](鐵氰化鉀)驗證II中Fe2+是否轉化完全的現象是 。
(4)III中發生反應的離子方程式是 。
通過計算說明在此條件下的溶液中Fe3+是否沉淀完全________________________(提示:當溶液中某離子濃度小于1.0×10–5 mol/L時可認為該離子沉淀完全)。
(5)應用化學平衡移動原理解釋IV中“濾液用稀硫酸酸化”的原因 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com