
科目: 來源:不詳 題型:實驗題
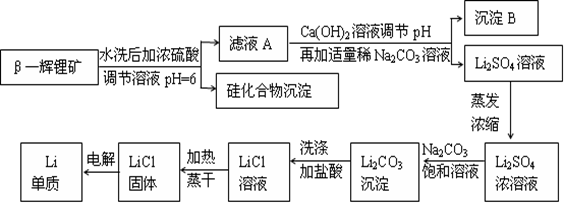
查看答案和解析>>
科目: 來源:不詳 題型:填空題
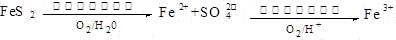
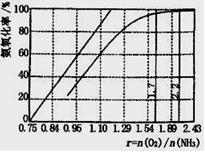
查看答案和解析>>
科目: 來源:不詳 題型:問答題
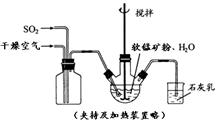
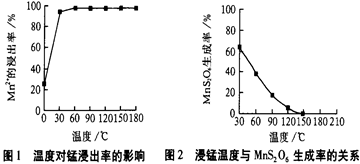
| 物質 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 開始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
查看答案和解析>>
科目: 來源:不詳 題型:單選題
| A.高溫加熱氧化鎂和碳的混合物可以制單質鎂 |
| B.鐵的冶煉過程是通過置換反應得到單質鐵 |
| C.海水提溴的過程中不發生氧化還原反應 |
| D.利用電解的方法可以從海水中獲得淡水 |
查看答案和解析>>
科目: 來源:不詳 題型:填空題

 Li7Ti5O12+3FePO4
Li7Ti5O12+3FePO4 查看答案和解析>>
科目: 來源:不詳 題型:填空題
查看答案和解析>>
科目: 來源:不詳 題型:填空題
查看答案和解析>>
科目: 來源:不詳 題型:填空題
 溴蒸氣
溴蒸氣
 液溴
液溴 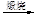
 石灰乳
石灰乳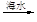
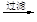
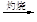 MgO
MgO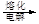 鎂
鎂
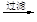 濾液
濾液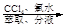 含碘有機溶液
含碘有機溶液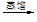 碘晶體
碘晶體
 精鹽
精鹽
 濾液
濾液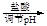
 食鹽晶體
食鹽晶體查看答案和解析>>
科目: 來源:不詳 題型:填空題
| A.可以利用某些煉鋼廢渣來生產磷肥 |
| B.具有永久硬度的水主要用加熱的方法來進行軟化 |
| C.硫酸工業中,在接觸室安裝熱交換器是為了利用S03轉化為H2S04時放出的熱量 |
| D.合成氨工業原料氣凈化時,常用碳酸鉀溶液吸收除去二氧化碳 |
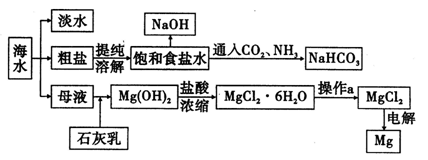
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com