
| c(Na2SO3)×103 | 3.65 | 5.65 | 7.65 | 11.65 |
| v×106 | 10.2 | 24.4 | 44.7 | 103.6 |
| 反應階段 | 速率方程 | $\frac{k(297.0K)}{k(291.5K)}$ |
| 富氧區 | v=kc(SO32-)•c(O2) | 1.47 |
| 貧氧區 | v=kca(SO32-)•cb(O2) | 2.59 |
分析 (1)已知:2Na2SO3(aq)+O2(aq)=2Na2SO4(aq)△H=m kJ•mol-1①
O2(g)?O2(aq)△H=nkJ•mol-1②
將方程式①+②得2Na2SO3(aq)+O2(g)=2Na2SO4(aq)△H進行相應的改變;
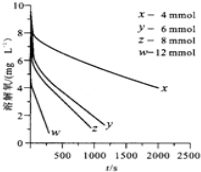
(2)0-20s內溶解氧濃度變化量=(9.60-6.40)mg/L=3.20mg/L=3.20×10-3 g/L,則△c(O2)=$\frac{3.20×1{0}^{-3}g/L}{32g/mol}$=10-4 mol/L,根據方程式得△c(Na2SO3)=2△c(O2)=2×10-4 mol/L,0-20s內Na2SO3的平均反應速率=$\frac{△c}{△t}$;
(3)①當溶解氧濃度為4.0mg•L-1時,c(Na2SO3)與速率數值關系如表,v1:v2=c1a(SO32-):c2a(SO32-);
②當溶解氧濃度小于4.0mg•L-1時,圖中曲線皆為直線,說明該方程為一次函數;
(4)該函數隨著Ea的增大而增大;
(5)從圖知Na2SO3初始濃度不同,溶解氧濃度與時間呈線性關系的起始溶解氧濃度不同;
(6)富氧區的化學反應速率與SO32-和溶解氧的濃度有關,貧氧區的化學反應速率與氧濃度無關.
解答 解:(1)已知:2Na2SO3(aq)+O2(aq)=2Na2SO4(aq)△H=m kJ•mol-1①
O2(g)?O2(aq)△H=nkJ•mol-1②
將方程式①+②得2Na2SO3(aq)+O2(g)=2Na2SO4(aq)△H=(m+n)kJ•mol-1;
故答案為:2Na2SO3(aq)+O2(g)=2Na2SO4(aq)△H=(m+n)kJ•mol-1;
(2)0-20s內溶解氧濃度變化量=(9.60-6.40)mg/L=3.20mg/L=3.20×10-3 g/L,則△c(O2)=$\frac{3.2×1{0}^{-3}g/L}{32g/mol}$=10-4 mol/L,根據方程式得△c(Na2SO3)=2△c(O2)=2×10-4 mol/L,0-20s內Na2SO3的平均反應速率v=$\frac{2×1{0}^{-4}mol/L}{20s}$=1.00×10-5mol•L-1•s-1;
故答案為:1.00×10-5;
(3)①當溶解氧濃度為4.0mg•L-1時,c(Na2SO3)與速率數值關系如表,v1:v2=c1a(SO32-):c2a(SO32-),$\frac{24.4}{10.2}$=$\frac{5.6{5}^{a}}{3.6{5}^{a}}$,解得a=2;
故答案為:2;
②當溶解氧濃度小于4.0mg•L-1時,圖中曲線皆為直線,說明該方程為一次函數,k為常數,v與c(SO32-)有關,溶解氧濃度對v無影響,所以b=0;
故答案為:0;
(4)ln$\frac{K2}{K1}$隨著Ea的增大而增大,富氧區的ln$\frac{K2}{K1}$較小,故Ea(富氧區)<Ea(貧氧區);
故答案為:<;
(5)從圖表可知Na2SO3初始濃度不同,溶解氧濃度與時間呈線性關系的起始溶解氧濃度不同;
答:不同;因為Na2SO3初始濃度不同,溶解氧濃度與時間呈線性關系的起始溶解氧濃度不同;
(6)富氧區的化學反應速率與SO32-和溶解氧的濃度有關,故富氧區與的決速步為①,貧氧區的化學反應速率與氧濃度無關,決速步為③;
故答案為:①;③.
點評 本題考查了蓋斯定律、化學反應速率的計算、以及函數結合圖象等知識,題目難度很大,需要學生對圖象圖表的充分理解,并運用學科綜合知識解題.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題


 )的廢水可以通過構成微生物電池除去,其原理如圖5所示.
)的廢水可以通過構成微生物電池除去,其原理如圖5所示.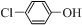 +2e-+H+═
+2e-+H+═ -OH+Cl-.
-OH+Cl-.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
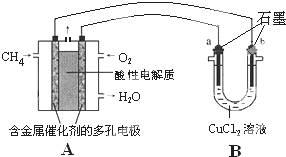 (3)甲烷燃料電池可以提升能量利用率.如圖是利用甲烷燃料電池電解50mL 2mol/L的氯化銅溶液的裝置示意圖.
(3)甲烷燃料電池可以提升能量利用率.如圖是利用甲烷燃料電池電解50mL 2mol/L的氯化銅溶液的裝置示意圖.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24 L水中含有的分子數約為0.l NA | |
| B. | 在常溫常壓下,1 mol He含有的原子數為NA | |
| C. | 2.4g金屬鎂變為鎂離子時失去的電子數為0.1NA | |
| D. | 物質的量濃度為0.5mol/L FeCl3溶液中Cl-的數目為1.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Q1>Q3>Q2 | B. | Q1>Q2>Q3 | C. | Q2>Q1>Q3 | D. | Q3>Q1>Q2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 可用NaOH和濕潤的紅色的石蕊試紙檢驗NH4+ | |
| B. | 該方法會導致水體pH下降 | |
| C. | 該方法中O2做氧化劑,微生物做還原劑 | |
| D. | 處理后的廢水需進一步處理才能排放 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;Al與NaOH溶液反應的離子方程式為2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
;Al與NaOH溶液反應的離子方程式為2Al+2NaOH+2H2O=2NaAlO2+3H2↑.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com