
| A. | 標準狀況下,2.24L氯氣與足量的鐵反應,轉移電子數為0.2NA | |
| B. | 標準狀況下,2.24L NO2所含電子總數為3.9 NA | |
| C. | 7.8gNa2S和Na2O2的混合物中含有的陰離子總數大于0.1 NA | |
| D. | 常溫常壓下,將0.1mol氯氣通入水中發生化學反應,轉移電子數為0.1 NA |
分析 A.2.24L氯氣的物質的量是0.1mol,其與足量的鐵反應,轉移電子數為0.2NA;
B.NO2氣體會有一部分發生反應轉化為N2O4;
C.每個Na2S和Na2O2都含有1個陰離子;
D.反應是可逆反應.
解答 解:A.標準狀況下,2.24L氯氣的物質的量是0.1mol,其與足量的鐵反應,轉移電子數為0.2NA,故A正確;
B.NO2氣體會有一部分發生反應轉化為N2O4,所以標準狀況下,2.24L NO2氣體中所含電子總數為在2.3NA與4.6NA之間,不一定是3.9 NA,故B錯誤;
C.7.8gNa2S和Na2O2的物質的量是0.1mol,由于兩種物質都是離子化合物,每個Na2S和Na2O2都含有1個陰離子,所以0.1mol Na2S和Na2O2的混合物中含有的陰離子總數等于0.1 NA,故C錯誤;
D.常溫常壓下,將0.1mol氯氣通入水中發生化學反應,由于反應是可逆反應,所以轉移電子數小于0.1 NA,故D錯誤.
故選A.
點評 本題考查了阿伏伽德羅常數的有關計算,熟練掌握公式的使用和物質的結構是解題關鍵,難度不大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 打開反應釜,將Na 暴露在空氣中與氧氣反應 | |
| B. | 向反應釜通入Cl2,Na 在Cl2中燃燒生成NaCl | |
| C. | 向反應釜加大量H2O,通過化學反應“除掉”金屬鈉 | |
| D. | 向反應釜滴加C2H5OH,并設置放氣管,排出氫氣和熱量 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
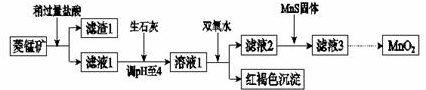
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 開始沉淀時 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀時 | 9.8 | 8.3 | 3.7 | 6.7 |
 紙置于陽極附近,若試紙變藍則證明有Cl2生成.
紙置于陽極附近,若試紙變藍則證明有Cl2生成.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子式為C5H10的烯烴 | B. | 分子式為C4H8O2的酯 | ||
| C. | 甲苯(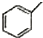 )的一氯代物 )的一氯代物 | D. | 立體烷( 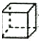 )的二氯代物 )的二氯代物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 編號 | NaOH/mol•L-1 | HA/mol•L-1 | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.2 | pH<7 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 當a>2b時,發生的離子反應為:2OH-+CO2=CO32-+H2O | |
| B. | 當a<b時,發生的離子反應為:OH-+CO2=HCO3- | |
| C. | 當2a=3b時,發生的離子反應為:3OH-+2CO2=CO32-+HCO3-+H2O | |
| D. | 當0.5a<b<a時,溶液中HCO3-與CO32-的物質的量之比為(a-b):(2b-a) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$ | B. | $\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$ | ||
| C. | $\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ | D. | c(H+)•c(CH3COO-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com