
| 鹵素 | 氰 | 硫氰 | ① | |
| “單質” | X2 | (CN)2 | (SCN)2 | (OCN)2 |
| 酸 | HX | HCN | ② | HOCN |
| 鹽 | KX | KCN | KSCN | ③ |
分析 (1)根據元素組成和物質的分類結合表中信息判斷;
(2)①HSCN與二氧化錳共熱反應類似于濃鹽酸和二氧化錳共熱反應;
②根據氯氣和KOH反應書寫(CN)2和KOH溶液反應方程式;
③因陰離子還原性強弱順序為:Br-<CN-<SCN-<I-.所以在NaBr和KSCN溶液中加入少量(CN)2時,(CN)2只與SCN-反應.
解答 解:(1)從(CN)2和(SCN)2類推即可得出(OCN)2和(SCN)2的名稱區別是元素S和O的區別,①應為氧氰,②應為HSCN,③為KOCN,
故答案為:氧氰;HSCN;KOCN;
(2)①HSCN與二氧化錳共熱反應類似于濃鹽酸和二氧化錳共熱反應,所以該離子反應方程式為4H++2SCN-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++(SCN)2↑+2H2O,
故答案為:4H++2SCN-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++(SCN)2↑+2H2O;
②(CN)2和KOH溶液反應類似氯氣和氫氧化鉀的反應:Cl2+2KOH=KCl+KClO+H2O,則(CN)2和KOH溶液反應的化學方程式為(CN)2+2KOH=KCN+KOCN+H2O,
故答案為:(CN)2+2KOH=KCN+KOCN+H2O;
③由還原能力的大小信息可知:(CN)2只能氧化SCN-而不能氧化Br-,在NaBr和KSCN的混合溶液中加入(CN)2只發生(CN)2+2SCN-=2CN-+(SCN)2,
故答案為:(CN)2+2SCN-=2CN-+(SCN)2.
點評 本題考查鹵族元素性質遞變規律,為高頻考點,側重考查學生知識遷移能力,根據鹵素單質性質采用知識遷移方法來分析解答即可,關鍵是找出物質之間的相似性,題目難度不大.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24L甲醇中含有的原子總數為0.6NA | |
| B. | 室溫下,500mL pH=1的稀硫酸中含有的H+總數約為0.05NA | |
| C. | 7.8g Na2O2晶體中含有的離子總數為0.4NA | |
| D. | 電解精煉銅時,若陰極得到電子總數為2NA,則陽極質量減少64g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A,B用導線連接后浸入電解質溶液,結果電子從B流向A | |
| B. | A從酸中置換出H2比B從酸中置換H2難 | |
| C. | 1 mol A從酸中置換出H十生成的H2比1mol B從酸中置換出H十生成的H2多 | |
| D. | 常溫時,A能從水中置換出氫氣,而B不能 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯分子里所有的原子在同一平面上 | |
| B. | 乙烯的結構簡式為CH2CH2,電子式為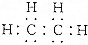 | |
| C. | 乙烯分子中碳氫鍵之間的夾角約為120° | |
| D. | 乙烯分子中既含有極性鍵又含有非極性鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
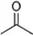 根據鍵線式回答下列問題:
根據鍵線式回答下列問題: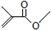 分子式:C5H8O2,
分子式:C5H8O2,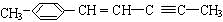 分子中最多有4個原子共直線;
分子中最多有4個原子共直線;
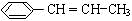 )在催化劑作用下生成聚苯丙烯的反應方程式:
)在催化劑作用下生成聚苯丙烯的反應方程式: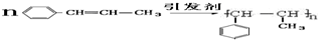 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
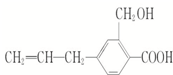 某有機物的結構簡式為如右圖所示,其可能具有的性質是( )
某有機物的結構簡式為如右圖所示,其可能具有的性質是( ) | A. | 全部 | B. | 僅能發生①②③④ | C. | 除⑤外都能 | D. | 除④⑤外都能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 molAl3+含有的核外電子數為3NA | |
| B. | 將58.5g NaCl溶于1.00 L水中,所得NaCL溶液的濃度為1.00mol•L-1 | |
| C. | 1 molCl2與足量的鐵反應,轉移的電子為數3Na | |
| D. | 常溫下,10LpH=1的硫酸溶液中含有的H+離子數為NA. |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 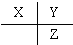 | B. | 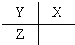 | C. | 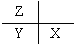 | D. | 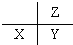 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com