
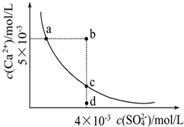
 常溫下,Ksp(CaSO4)=9×10-6,常溫下CaSO4在水中的沉淀溶解平衡曲線見圖.下列敘述正確的是
常溫下,Ksp(CaSO4)=9×10-6,常溫下CaSO4在水中的沉淀溶解平衡曲線見圖.下列敘述正確的是| A. | 2句 | B. | 3句 | C. | 4句 | D. | 5句 |
分析 ①處于曲線上的點為飽和溶液的平衡狀態;
②Ksp與溫度有關,a和c的Ksp相等;
③依據圖示讀數判斷是否有沉淀生成即可;
④蒸發使離子濃度增大,d點不可能到c點;
⑤常溫下CaSO4飽和溶液中,c(Ca2+)=c(SO42-);
⑥根據混合后溶液中硫酸根離子的濃度偏低.
解答 解:①處于曲線上的點為飽和溶液的平衡狀態,故①正確;
②a、c兩點溫度相同,Ksp是一常數,溫度不變Ksp不變,在曲線上的任意一點Ksp都相等,故②錯誤;
③根據圖示數據,可以看出b點Qc=2×l0-5>Ksp,所以會生成沉淀,故③正確;
④升高溫度,有利于溶解平衡正向移動,所以硫酸根的濃度會增大,不可能由d點變為c點,故④錯誤;
⑤常溫下CaSO4飽和溶液中,c(Ca2+)=c(SO42-),而曲線上的點所表示的c(Ca2+)與c(SO42-),不一定相同,故⑤錯誤;
⑥常溫下,向100mL飽和CaSO4溶液中加入400mL0.01mol/L Na2SO4溶液,混合液中硫酸根離子濃度約為$\frac{0.01mol/L×0.4L}{0.1L+0.4L}$=0.008mol/L,而b點硫酸根離子的濃度為0.004mol/L,則無法使溶液由a點變為b點,故⑥錯誤;
根據分析可知,正確的有2句,
故選A.
點評 本題考查了沉淀溶解平衡的應用,圖象分析應用,溶度積計算分析,平衡移動方向的判斷,關鍵是計算混合溶液中鈣離子濃度和硫酸根離子濃度,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.36×10-5 mol•L-1 | B. | 8.90×10-6 mol•L-1 | ||
| C. | 4.45×10-2 mol•L-1 | D. | 1×10-5 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 黑色沉淀完全轉化為白色沉淀 | B. | 既有 Ag2S 也有 AgCl | ||
| C. | 不能由黑色沉淀轉變為白色沉淀 | D. | 只有 AgCl 白色沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
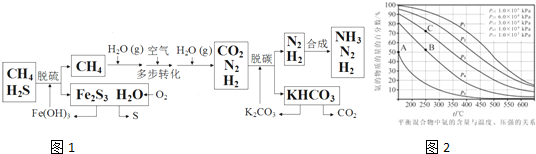
 N、C、S元素的單質及化合物在工農業生成中有著重要的應用
N、C、S元素的單質及化合物在工農業生成中有著重要的應用| t/min | n(CO)/mol | n(Cl2)/mol |
| 0 | 1.20 | 0.60 |
| 1 | 0.90 | |
| 2 | 0.80 | |
| 4 | 0.20 |
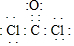
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
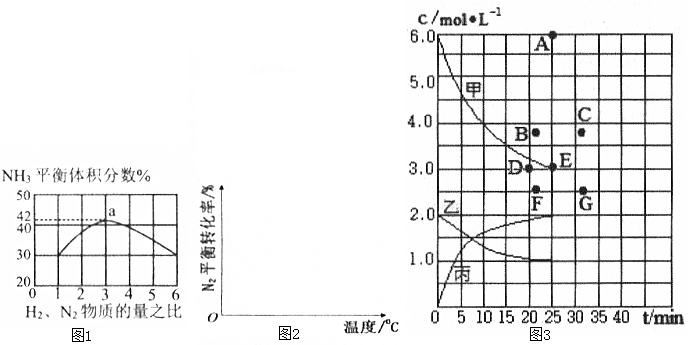

| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| N(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| N(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com