
 甲醇可作為燃料電池的原料.以CH4和H2O為原料,通過下列反應來制備甲醇.
甲醇可作為燃料電池的原料.以CH4和H2O為原料,通過下列反應來制備甲醇.分析 (1)依據蓋斯定律將已知熱化學方程式變形運算解答;
(2)列三段式表示各物質起始量、轉化量、平衡量;依據反應速率計算公式V=$\frac{△C}{△t}$計算解答;
(3)負極發生氧化反應,甲醇在負極失去電子,堿性條件下生成碳酸根與水;
(4)①通電后,將Co2+氧化成Co3+,電解池中陽極失電子發生氧化反應,電極反應為Co2+-e-=Co3+;
②以Co3+做氧化劑把水中的甲醇氧化成CO2而凈化,自身被還原為Co2+,原子守恒與電荷守恒可知,還原生成H+,配平書寫為:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.
解答 解:(1)Ⅰ:CH4(g)+H2O(g)═CO(g)+3H2(g)△H=+206.0kJ•mol-1
Ⅱ:CO(g)+2H2(g)═CH3OH(g)△H=-129.0kJ•mol-1
依據蓋斯定律,Ⅰ-Ⅱ得:CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+206.0kJ/mol-(-129.0kJ/mol)=+77.0 kJ/mol;
故答案為:CH4(g)+H2O(g)=CH3OH(g)+H2(g)△H=+77.0 kJ/mol;
(2)將1.0mol CH4和2.0mol H2O ( g )通入容積固定為100L的反應室,在一定條件下發生反應I,由圖象可知100℃甲烷轉化率為50%,故參加反應的甲烷為1mol×50%=0.5mol,則:
CH4 (g)+H2O (g)=CO (g)+3H2 (g)
起始量(mol):1.0 2.0 0 0
變化量(mol):0.5 0.5 0.5 1.5
平衡量(mol):0.5 1.5 0.5 1.5
假設100℃時達到平衡所需的時間為5min,則用H2表示該反應的平衡反應速率V(H2)=$\frac{\frac{1.5mol}{100L}}{15min}$=0.001 mol•L-1•min-1,
故答案為:0.001 mol•L-1•min-1;
(3)負極發生氧化反應,甲醇在負極失去電子,堿性條件下生成碳酸根與水,負極電極反應式為:CH3OH-6e-+8OH-═CO32-+6H2O,故答案為:CH3OH-6e-+8OH-═CO32-+6H2O;
(4)①通電后,將Co2+氧化成Co3+,電解池中陽極失電子發生氧化反應,電極反應為Co2+-e-=Co3+,故答案為:Co2+-e-=Co3+;
②以Co3+做氧化劑把水中的甲醇氧化成CO2而凈化,自身被還原為Co2+,結合原子守恒與電荷守恒可知,還原生成H+,配平書寫離子方程式為:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+,
故答案為:6Co3++CH3OH+H2O=CO2↑+6Co2++6H+.
點評 本題考查熱化學方程式書寫、化學平衡圖象、影響化學平衡因素、平衡常數與反應速率計算、原電池等,掌握基礎是解本題的關鍵,題目難度中等.


 期末100分闖關海淀考王系列答案
期末100分闖關海淀考王系列答案 小學能力測試卷系列答案
小學能力測試卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
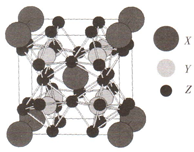 某種能實現熱電效應的晶體的晶胞模型如右圖.已知晶胞的六個面的原子數相同,Y原子位于Z原子圍成的八面體中心.下列說法正確的是( )
某種能實現熱電效應的晶體的晶胞模型如右圖.已知晶胞的六個面的原子數相同,Y原子位于Z原子圍成的八面體中心.下列說法正確的是( )| A. | 距離X最近的Y原子有8個 | B. | 距離X最近的X原子有6個 | ||
| C. | 距離X最近的Z原子有3個 | D. | 該晶體的化學式為X2Y8Z12 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=0的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| B. | c(H+)=1×10-14mol•L-1的溶液中:Mg2+、NO3-、Fe2+、ClO- | |
| C. | 含有大量Fe3+的溶液中:Na+、I-、K+、NO3- | |
| D. | 由水電離出的c(OH-)=1×10-13mol/L的溶液中:Na+、[Al(OH)4]-、S2-、CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩者電子數相差1 | B. | 兩者質量數相差1 | C. | 兩者中子數相差1 | D. | 兩者互為同位素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
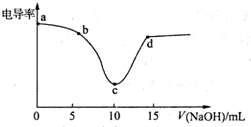 利用電導率傳感器可繪制電導率曲線圖,下圖為用0.1mol•L-1NaOH溶液滴定10mL,0.1mol•L-1鹽酸過程中的電導率曲線.下列說法錯誤的是( )
利用電導率傳感器可繪制電導率曲線圖,下圖為用0.1mol•L-1NaOH溶液滴定10mL,0.1mol•L-1鹽酸過程中的電導率曲線.下列說法錯誤的是( )| A. | 電導率傳感器能用于判斷酸堿中和滴定的終點 | |
| B. | 該過程中,a點所示溶液的導電性最強 | |
| C. | c點電導率最小是因為此時溶液中導電微粒的數目最少 | |
| D. | d點所示溶液中存在:c(Cl-)+c(OH-)=c(H+)+c(Na+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下在強堿性的溶液中:Na+、Ba2+、Cl-、NO3- | |
| B. | 能使紫色石蕊試液變藍的溶液中:Ca2+、Fe2+、AlO2-、Cl- | |
| C. | 與鋁反應產生無色無氣味氣體的溶液中:Na+、K+、HCO3-、SO42- | |
| D. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4:5:2 | B. | 2:5:4 | C. | 1:3:2 | D. | 3:2:1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com